Вещество-«О3-–-ОЗОН».-Третьяков
advertisement
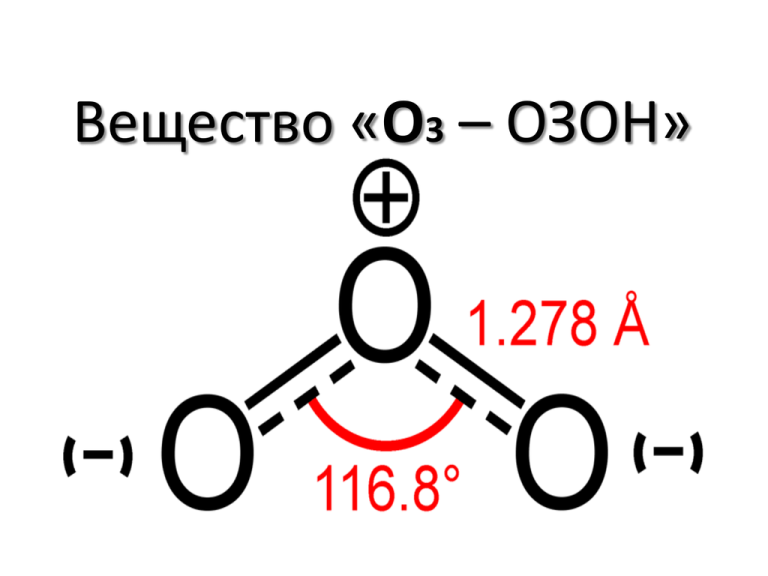
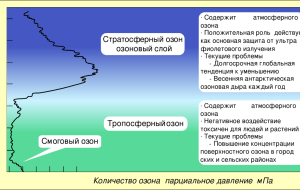
Вещество «О3 – ОЗОН» Физические Свойства: • Молекулярная масса — 48 а.е.м. • Плотность газа при нормальных условиях — 2,1445 г/дм³. Относительная плотность газа по кислороду 1,5; по воздуху — 1,62 (1,658). • Плотность жидкости при −183 °C — 1,71 г/см³ • Температура кипения — −111,9 °C. Жидкий озон — тёмнофиолетового цвета. • Температура плавления — −197,2 ± 0,2 °С (приводимая обычно т.пл. −251,4 °C ошибочна, так как при её определении не учитывалась большая способность озона к переохлаждению). В твёрдом состоянии — чёрного цвета с фиолетовым отблеском. • Растворимость в воде при 0 °С — 0,394 кг/м³ (0,494 л/кг), она в 10 раз выше по сравнению с кислородом. • В газообразном состоянии озон диамагнитен, в жидком — слабопарамагнитен. • Запах — резкий, специфический «металлический» (по Менделееву — «запах раков»). При больших концентрациях напоминает запах хлора. Запах ощутим даже при разбавлении 1 : 100000. История Открытия • Впервые озон обнаружил в 1785 году голландский физик М. ван Марум по характерному запаху и окислительным свойствам, которые приобретает воздух после пропускания через него электрических искр, а также по способности действовать на ртуть при обыкновенной температуре, вследствие чего она теряет свой блеск и начинает прилипать к стеклу. Однако как новое вещество он описан не был, ван Марум считал, что образуется особая «электрическая материя». • Термин озон был предложен немецким химиком X. Ф. Шёнбейном в 1840 году за его пахучесть, вошёл в словари в конце XIX века. Многие источники именно ему отдают приоритет открытия озона в 1839 году. В 1840 году Шёнбейн показал способность озона вытеснять иод из иодида калия: • Факт уменьшения объёма газа при превращении кислорода в озон экспериментально доказали Эндрюс и Тэт при помощи стеклянной трубки с манометром, наполненной чистым кислородом, со впаянными в неё платиновыми проволками для получения электрического разряда. Биологические Свойства: • Высокая окисляющая способность озона и образование во многих реакциях с его участием свободных радикалов кислорода определяют его высокую токсичность. Воздействие озона на организм может приводить к преждевременной смерти. • Наиболее опасное воздействие: • на органы дыхания прямым раздражением и повреждением тканей • на холестерин в крови человека с образованием нерастворимых форм, приводящим к атеросклерозу • на органы размножения у самцов всех видов животных, в том числе и человека (вдыхание этого газа убивает мужские половые клетки и препятствует их образованию). При долгом нахождении в среде с повышенной концентрацией этот газ может стать причиной мужского бесплодия. • Озон в Российской Федерации отнесён к первому, самому высокому классу опасности вредных веществ. Нормативы по озону: • максимальная разовая предельно допустимая концентрация (ПДК м.р.) в атмосферном воздухе населённых мест 0,16 мг/м³ • среднесуточная предельно допустимая концентрация (ПДК с.с.) в атмосферном воздухе населённых мест 0,03 мг/м³ • предельно допустимая концентрация (ПДК) в воздухе рабочей зоны 0,1 мг/м³ • При этом, порог человеческого обоняния приближённо равен 0,01 мг/м³. • Озон эффективно убивает плесень и бактерии. Озон в Атмосфере. Атмосферный озон играет важную роль для всего живого на планете. Образуя озоновый слой в стратосфере, он защищает растения и животных от жёсткого ультрафиолетового излучения. Поэтому проблема образования озоновых дыр имеет особое значение. Однако тропосферный озон является загрязнителем, который может угрожать здоровью людей и животных, а также повреждать растения.