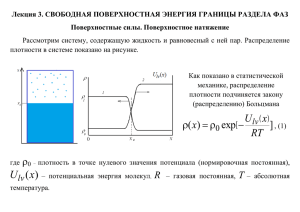
поверхностное натяжение σ
advertisement
Молекулярнокинетические свойства дисперсных систем 1 Высокодисперсные системы или ультрамикрогетерогенные, наряду с поверхностными свойствами, обладают и молекулярно-кинетическими свойствами, связанными с тепловым движением частиц. К ним относятся: осмотические явления, диффузия, броуновское движение, седиментационное равновесие. Особенностью является то, что высокодисперсные системы (нано-системы) могут обладать двумя видами свойств одновременно: поверхностными свойствами и2 молекулярно-кинетическими. В истинных растворах отсутствуют поверхностные явления, но они обладают молекулярнокинетическими свойствами, причем в значительно большей степени, чем дисперсные системы. В системах с достаточно большими частицами тепловое движение отсутствует, поэтому там исчезают молекулярно-кинетические свойства, а остаются лишь поверхностные. Итак, при рассмотрении молекулярно-кинетических свойств дисперсных систем мы будем иметь в виду только высокодисперсные системы, частицы которых настолько малы, что способны принимать участие в тепловом движении. 3 ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ Свойства вещества в тонком поверхностном слое на границе раздела фаз существенно отличаются от его состояния внутри объема. Это обусловлено тем, что силы взаимодействия между частицами (молекулами, атомами, ионами) поверхностного слоя и частицами внутренних слоев каждой фазы неодинаковы из-за различной природы или агрегатного состояния этих фаз. Возникающая несимметричность силовых полей вблизи границы раздела фаз приводит к проявлению5 на ней ряда поверхностных явлений. Поверхностные явления могут иметь чисто физический характер или сопровождаться химическими превращениями. Физические и химические превращения сильно влияют на характер и скорость гетерогенных процессов, а также на объемные свойства веществ (например, на их прочность). Поверхностные явления проявляются тем сильнее, чем больше поверхность раздела фаз, т.е. в случае пористых или тонко измельченных тел. 6 Нефтяные и газоносные пласты, сложенные осадочными горными породами, имеют огромное количество капиллярных каналов и трещин, поверхность которых очень велика. Поверхность поровых каналов 1м3 нефтегазоносных пластов может достигать 10м . Эта поверхность контактирует с насыщающими пласт водой, нефтью или газом. Газ и не смешивающиеся жидкости - вода и нефть в порах пласта находятся в контакте между собой. Суммарная поверхность их контакта также очень велика. В таких условиях возрастает роль поверхностных явлений, протекающих на границах раздела нефть-порода, вода-порода, газ-порода, нефть-вода, нефть-газ, в процессах формирования и7 разработки нефтяных, и газовых месторождений. Поверхностные явления, происходящие в пласте в процессе формирования залежи, обусловливают строение поверхностей раздела порода-вода-нефть-газ, взаимное расположение жидкостей и газов в пористой среде, количество, связанной воды и некоторые другие свойства пласта. Они существенно влияют на движение нефти, газа и воды в пластах, на вытеснение нефти водой и газом, на загрязнение приствольной зоны скважины фильтратом промывочной жидкости при бурении. Поверхностные явления имеют место при образовании и разрушении водонефтяных эмульсий, при отложении гипсово-углеводородных отложений в скважинах и призабойной зоне пласта, при приготовлении и в процессах использования тампонажных растворов. 8 В конечном счете, поверхностные силы определяют нефтеотдачу пластов, продолжительность освоения и производительность скважин, качество подготовки нефти к переработке. Поэтому знание теории поверхностных явлений имеет большое значение в нефтепромысловой практике, увеличения количества и улучшения качества добываемой нефти. 9 Поверхностная энергия может превращаться в другие виды энергии, и эти превращения сопровождают возникновение различных поверхностных явлений, таких как смачивание, адгезия, капиллярность, адсорбция и т. д. Учение о поверхностных явлениях рассматривает строение и свойства границы раздела вне зависимости от степени дисперсности в системе, так как поверхностные явления существуют везде, где есть поверхность. Учение о дисперсных системах, об их получении и свойствах во многом определяется поверхностными явлениями. Без рассмотрения поверхностных явлений изучение свойств дисперсных систем становится невозможным. В то же время теория поверхностных явлений становится всеобъемлющей лишь в том случае, если она прилагается к реальным дисперсным системам. 10 Поверхностные явления удобно рассматривать и классифицировать на основе понятий и представлений химической термодинамики. Рассмотрим классификацию поверхностных явлений в соответствии с объединенным уравнением I и II начал термодинамики. Запишем его для поверхностного слоя: dG = -sdT + VdP + σdS + Σμidni + φdq, (1) где G - энергия Гиббса; s - энтропия; T - температура; V — объем; Р давление; σ - поверхностное натяжение; S - площадь поверхности; μi химический потенциал компонента i; ni - число молей компонента i; φ электрический потенциал; q - количество электричества. В уравнении приращение свободной энергии Гиббса представлено как алгебраическая сумма приращений различных видов энергии: тепловой, механической, поверхностной, химической и электрической. Выделим из всей суммы поверхностную энергию σdS, которая представлена в уравнении как произведение поверхностного натяжения σ (интенсивный фактор). Роль удельной поверхностной энергии играет 11 величина σ. Дадим подробную характеристику поверхностному натяжению. Термодинамическое определение поверхностного натяжения вытекает из уравнения (1) при постоянных Т, Р, п и q имеем: 𝜎= 𝛿𝐺 〔 〕T,P,n,q 𝛿𝑆 (2) Поверхностное натяжение - есть частная производная от энергии Гиббса по величине поверхности раздела фаз при постоянных значениях температуры, давления, числа12 молей компонентов и заряда. Поверхностному натяжению можно дать и другие характеристики силовую и энергетическую. Рассмотрим молекулярные силы по границе жидкости с собственным паром. Водяной пар (1) и вода (2). Молекулы воды увеличены примерно в 5·107 раз. 13 СХЕМА ОБРАЗОВАНИЯ ПОВЕРХНОСТНОГО НАТЯЖЕНИЯ: 1 – ГАЗ, 2 – ЖИДКОСТЬ, 3 – ПОВЕРХНОСТЬ РАЗДЕЛА 14 Равнодействующая сила всех молекул поверхностного слоя жидкости называется внутренним или молекулярным давлением. Молекулярное давление зависит от силы взаимодействия между молекулами, то есть от природы жидкости. Силы взаимодействия тем выше, чем полярнее молекулы. Так для воды межмолекулярное взаимодействие (внутреннее давление) - равно 1480 МПа, для бензола -380 МПа, для эфира всего 27 МПа. 15 Сила, отнесенная к единице длины контура, ограничивающего данную поверхность, называется поверхностным натяжением σ. Размерность силы и в системе СИ измеряется в Н/м. 16 17 Растяжение пленки (рамка Дюпре) 18 Если обозначить длину границы поверхности жидкости l, силу поверхностного натяжения одной пленки, действующей на этой границе, – F, то коэффициент поверхностного натяжения будет F σ= . l или σ=mg/2l Таким образом, σ может быть представлена как стягивающая сила, направленная тангенциально и отнесенная к единице длины контура. 19 В то же время молекулы на поверхности, не полностью реализуя свою способность к взаимодействию, обладают избытком энергии. При образовании новой поверхности необходимо совершить работу по созданию этой избыточной энергии. Для единицы площади поверхности она равна удельной свободной поверхностной энергии Gуд, которая имеет размерность энергии на единицу площади и измеряется в системе СИ в Дж/м2. Таким образом величины GS и σ имеют совпадающие размерности: Дж/м2 = Н⦁м/м2 = Н/м и близкие или совпадающие численные значения. Поэтому они равнозначны, а граничные свойства фаз принято характеризовать с помощью поверхностного натяжения σ, которое чаще выражают в единицах энергии. Иными словами, можно считать, что поверхностное натяжение σ - мера избытка свободной поверхностной энергии на 1 м2 поверхности раздела фаз, удельная свободная поверхностная энергия: σ=Gs/S или σ=dGs/dS 20 Опыт Плато 21 Поверхностное натяжение можно представить и как работу, необходимую для разрыва столбика вещества, состоящего из одной фазы с поперечным сечением в 0,5 м2. После разрыва образуются две новые поверхности общей площадью 1 м: S1+S2=0,5 м2 +0,5 м2 =1 м2 22 Поскольку поверхностное натяжение связано с энергией разрыва межмолекулярных связей, то оно ими и обусловлено. Чем сильнее взаимодействие молекул в данном теле, тем больше его поверхностное натяжение. Так, наименьшим значением σ обладают сжиженные газы, затем идут жидкости, причем, как правило, чем выше полярность жидкости, тем выше ее поверхностное натяжение. Еще больше поверхностное натяжение у твердых тел. Поверхностное натяжение у алмаза достигает десятков тысяч23 мДж/м2. Поверхностное натяжение некоторых веществ на границе с водой и воздухом [27] Вещество Вода (20 °С) Бензол (20 °С) Толуол (20 °С) н-гексан (20 °С) Ртуть (20 °С) Бензин (20 °С) Нефть ромашкинская (20 °С) Нефть тюменская (20 °С) Мазут-100 (20 °С) Платина (2000 °С) Алмаз (25 °С) Свинец(350 °С) Гелий (– 270 °С) Азот (– 193 °С) Гептановая кислота (20 °С) Поверхностное натяжение на Поверхностное натяжение на границе с воздухом, мН/м границе с водой, мН/м 72,80 – 28,88 35,0 28,43 36,1 18,43 51,1 465,0 375,0 19,3 48,3 28,0 30,5 28,5 28,7 32,0 1819,0 11400,0 442,0 0,22 8,27 35,6 н.д. н.д. н.д. н.д. н.д. н.д. 6,6 24 Величина поверхностного натяжения зависит от природы жидкости и граничащей с ней фазы. Чем больше отличаются друг от друга по полярности соприкасающийся фазы, тем больше поверхностное натяжение на их контакте. Это объясняется тем, что силы взаимодействия между молекулами различных фаз меньше, чем между молекулами внутри каждой фазы. Молекулы н-бутанола так же, как и молекулы воды, полярны, поэтому поверхностное натяжение н-бутанола на границе с водой невысокое и значительно выше на границе с воздухом. Молекулы углеводородов неполярны, вследствие чего поверхностное натяжение выше на границе их раздела с водой. Нефти различных месторождений отличаются величиной поверхностного натяжения. Это определяется различием химического состава нефтей, количеством растворенного в них газа и, в основном, содержанием полярных компонентов 25 Степень различия в напряженности межмолекулярных сил, действующих в соприкасающихся фазах, т. е. степень различия полярности соприкасающихся фаз, в разных системах различна. Полярностью жидкости принято называть интенсивность поля молекулярных сил. Эта характеристика межмолекулярного сцепления связана в основном с такими параметрами жидкости, как дипольный момент μ, поляризуемость α и диэлектрическая проницаемость ε. Однако сопоставление значений σ для различных веществ показывает, что полярность, в общем, растет с увеличением значений μ и ε, но простой связи между ними нет. Это указывает, что наряду с электростатической существуют и другие компоненты молекулярных сил, проявляющиеся, в частности, для молекул с двойными связями. Отметим, что ртуть не является электрически полярной (дипольной) жидкостью, однако интенсивность силового поля для Hg весьма велика. Внутреннее давление жидкости – это следствие межмолекулярного взаимодействия. Чем полярнее вещество, тем 26 силы взаимодействия молекул выше и тем больше поверхностное натяжение системы. С ростом полярности жидкости, а, следовательно, и с ростом ее молекулярного давления, степень ассоциации ее и диэлектрическая постоянная возрастают, а сжимаемость – уменьшается. Чем больше отличаются друг от друга по полярности соприкасающиеся фазы, тем больше поверхностное натяжение на их границе раздела. При равной полярности двух соприкасающихся фаз поверхностное натяжение их становится равным нулю и граница раздела отсутствует – происходит полное взаимное растворение обеих фаз. С уменьшением взаимной растворимости соприкасающихся фаз поверхностное натяжение увеличивается. 27 Характеристика межфазной поверхности Форма и строение межфазной поверхности зависит от агрегатного состояния граничащих фаз. На границе жидкость-газ из-за подвижности молекул жидкости межфазная поверхность находится в состоянии постоянного обновления. Все точки такой поверхности энергетически одинаковы, то есть поверхность можно считать эквипотенциальной (т.е. во всех точках поверхности потенциал электрического поля имеет одинаковые значения). На границе твердое тело-газ межфазная поверхность в течение длительного времени остается неизменной. Различные точки такой поверхности имеют разную энергию, то есть она не будет эквипотенциальной. 28 Нефти различных месторождений отличаются величиной поверхностного натяжения. Это определяется различием химического состава нефтей, количеством растворенного в них газа и, в основном, содержанием полярных компонентов. С повышением температуры - поверхностное натяжение жидкости уменьшается за счет ослабления межмолекулярных сил. Зависимость σ от температуры определяется уравнением: σt =σ0⦁(1-γt), σ σ где t и 0 - поверхностное натяжение системы при температурах t и 0° С; γ - температурный коэффициент поверхностного натяжения, зависящий от природы жидкости 29 (колеблется в пределах 0,002-0,004). Вещество Молекулярная масса Поверхностное натяжение ∙10–3, Дж/м2 при температуре, °С 0 10 20 30 40 60 Пентан 72,15 18,2 17,1 16,0 14,9 13,8 – Гексан 86,18 20,6 19,5 18,5 17,4 16,3 14,2 Гептан 100,21 – – 20,9 19,5 18,7 16,4 Октан 114,24 23,7 22,7 21,8 20,8 19,8 17,8 Циклогекса н 84,16 – 26,2 24,9 23,7 22,5 — Бензол 78,11 – 30,2 28,9 27,5 26,1 23,7 Толуол 92,14 30,9 29,7 28,5 27,3 26,1 23,9 30 о-Ксилол 106,17 32,3 31,2 30,0 28,9 27,9 25,7 С увеличением давления поверхностное натяжение жидкости на границе с газом также понижается. Это связано с уменьшением величины внутреннего давления и свободной поверхностной энергии вследствие сжатия газа и его растворения в жидкости. Чем выше растворимость газа, тем значительнее уменьшение поверхностного натяжения с ростом давления. Подобный характер изменения поверхностного натяжения от давления и температуры наблюдается и для нефти на границе её с газом 31 Давление, кг/см2 Поверхностное натяжение, (дин/см) 25 °С 65 °С 0 74,1 67,5 7,1 71,1 17,6 35,2 Давление, кг/см2 Поверхностное натяжение, (дин/см) 25 °С 65 °С 70,5 55,9 50,4 63,2 105,0 51,6 46,5 66,5 58,8 140,0 47,9 42,3 61,6 55,5 190,0 44,1 39,5 32 Зависимость поверхностного натяжения туймазинской нефти на границе с газом (азотом) от давления при разных температурах: 1 – t = 20°C; 2 – t = 60°C; 3 – t= 80°C 33 Поверхностное натяжение туймазинской нефти на границе с водой при различных давлениях, при t = 20°C 34 Известно, что в пластовых условиях нефть содержит в себе то или иное количество растворенного газа, зависящее от давления. Чем больше давление, тем выше растворимость газа в нефти. С увеличением количества растворенного газа в нефти поверхностное натяжение ее на границе с газом будет понижаться. То же самое будет происходить с водой, но в значительно меньшей степени, так как растворимость углеводородных газов при прочих равных условиях в воде меньше, чем в нефти. Поскольку разница в поверхностных натяжениях у воды и нефти на границе с газом в этом случае возрастает, то должно расти и поверхностное натяжение на границе их раздела с ростом газового35 фактора. На границе раздела двух жидкостей в той или иной степени происходит их взаимное растворение, поверхностное натяжение на этой границе устанавливается не сразу, а только после полного взаимного насыщения жидкостей друг другом. Поэтому различают поверхностное натяжение статическое, отвечающее состоянию равновесия, и динамическое, полученное в некоторый момент времени, когда система не пришла еще в равновесное состояние. Динамическое поверхностное натяжение жидкостей всегда36 больше статического. Существование аддитивности действия молекулярных сил выражается правилом Антонова, согласно которому межфазное натяжение равно разности поверхностных натяжений этих жидкостей (на границах с воздухом) в условиях взаимного насыщения. Применяя индексы агрегатного состояния, можно записать это правило следующим образом жж 1 жг 2 жг Например, для границы вода – бензол σ1жг относится к насыщенному раствору бензола в воде, σ2жг – к насыщенному раствору воды в бензоле 37 С уменьшением разности полярностей взаимная растворимость жидкостей чаще всего увеличивается, свойства сосуществующих фаз, и, следовательно, значения σ1жг и σ2жг, становятся все более близкими и σжж уменьшается – в пределе до нуля с исчезновением межфазной границы Последнее наступает при достижении неограниченной растворимости. 38 Поверхностное натяжение на границе нефть – газ Разгазирование нефтей следует рассматривать как процесс кипения, при котором отдельные компоненты (молекулы растворенных газов), обладающие наибольшей кинетической энергией, преодолевают некоторый активационный барьер (силы молекулярного притяжения) и выходят из объема нефти через поверхностный слой в газообразную фазу Чтобы молекулы газообразных компонентов могли проникнуть через поверхностный слой нефть – газ их кинетическая энергия, равная где m – масса молекулы; с – средняя скорость движения молекулы; Т – абсолютная температура; k – постоянная Больцмана, 39 Замечено, что чем легче нефти подвергаются процессу разгазирования, тем меньшим поверхностным натяжением они обладают на границе с газом (паром). При рассмотрении характера изменения поверхностного натяжения нефтей на границе с газом (паром) следует учитывать, что в данном случае образуется граница раздела двух сред, на которой энергетически выгодным является концентрирование молекул жидких углеводородов парафинового ряда со сравнительно небольшой молекулярной массой, имеющих по сравнению с другими углеводородами нефти наиболее низкое значение поверхностного 40 натяжения на границе с газом (паром) На любой границе раздела различный характер межмолекулярных сил взаимодействия обеспечивает наличие переходной области от одной объемной фазы к другой. Эта область называется поверхностью разрыва, или поверхностным слоем (ПС). В ней свойства объемных фаз α и β плавно переходят друг в друга по неизвестному закону 41 В общем случае под толщиной поверхностного слоя h следует понимать расстояние по обе стороны от границы раздела фаз, за пределами которого свойства поверхностного слоя перестают отличаться от свойств объемных фаз. Поверхностный слой толщину имеет очень малую (всего несколько молекул), но в нем сосредоточен весь избыток поверхностной энергии и массы вещества. В настоящее время существуют два подхода к количественной оценке свойств поверхностного слоя: метод избыточных величин (Гиббс) и метод слоя конечной толщины (Гугенгейм). 42 По методу избытков Гиббса нет необходимости определять границы поверхностного слоя. Суть метода состоит в том, что Гиббс ввел понятие системы сравнения - идеализированную систему, по отношению к которой определяются избытки параметров в поверхностном слое реальной системы. В идеализированной системе внутри поверхностного слоя проводится условная разделяющая поверхность (РП) "нулевой" толщины, на которой любое свойство системы меняется скачкообразно, а фазы α и β считаются однородными вплоть до РП. Эта разделяющая поверхность обладает избыточными термодинамическими параметрами по сравнению с параметрами43 объемных фаз, но не имеет объема. Общая энергия Гиббса в системе равна сумме энергий Гиббса объемных фаз ΔGα и ΔGβ и поверхностной энергии ΔGs =σS: ΔG = ΔGα + ΔGβ S + ΔG . Поверхностная энергия будет избыточной и равна разности общей энергии в реальной и идеализированной системах (заштрихованные области): ΔGS = ΔG - (ΔGα + ΔGβ). 44 В методе слоя конечной толщины используются две разделяющие поверхности, расположенные на расстоянии h, а поверхностный слой имеет некоторый объем. Границы объемных фаз совпадают с границами поверхностного слоя. Общая энергия Гиббса по этому методу включает, кроме энергии объемных фаз ΔGα ' и ΔGβ ', энергию поверхностного слоя ΔGnc, которая имеет две составляющие: поверхностную энергию ΔGncS и объемную ΔGncV: ΔG = ΔGα ' + ΔGβ '+ ΔGncS + ΔGncV. 45 Объемная составляющая поверхностного слоя содержит избытки со стороны объемных фаз α и β. Этот метод требует знания толщины поверхностного слоя и в расчетах использует сложные уравнения, учитывающие изменения параметров по толщине слоя. При h→О ΔGncV→0, а ΔGnc→ ΔGncS то есть метод слоя конечной толщины сводится к методу Гиббса. Метод избытков Гиббса является более удобным и распространенным. В нем между избыточными термодинамическими функциями существуют те же соотношения, которые связывают функции объемных фаз. По методу Гиббса, математические выражения получаются более простыми, хотя значения избыточных величин зависят от положения разделяющей поверхности. 46