Составитель: преподаватель математики и физики Уральского
advertisement

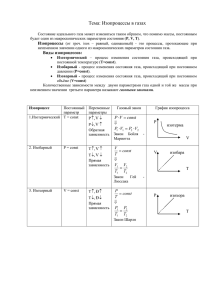
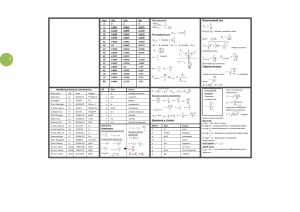
Составитель: преподаватель математики и физики Уральского колледжа газа, нефти и отраслевых технологий Лукпанова Дина Макпозовна, г. Уральск Тема урока:Уравнение состояние идеального газа. Изопроцессы.Уравнение МенделееваКлайперона Цель урока: выяснение условий выполнения изопроцессов; выяснение теоретической зависимости трех макроскопических параметров; практическое доказательство этих параметров. Задачи урока: 1. Диагностика знаний учащихся по темам: “Основы молекулярно-кинетической теории”, “Основное уравнение молекулярно-кинетической теории” “Уравнение состояния идеального газа”. 2. Коррекция теоретических знаний по данным темам. 3. Виртуальное и экспериментальное подтверждение законов “Бойля-Мариотта”, “Гей-Люссака”, “Шарля”. 4. Теоретическое обобщение и подтверждение зависимости макроскопических параметров 5. Разработка алгоритма решения графических задач и перепостроения графиков в различные системы координат. 1. Организация урока 2. Постановка цели и задач урока 3. Презентация 4. Мотивация мысленной деятельности учащихся (работа по тестам и 2 учащихся у доски с аналогичными заданиями по пройденному материалу) 5. Объяснение нового материала А) изотермический процесс (закон Бойля-Мариотта) Б) изобарный процесс (закон Гей-Люссака) В) изохорный процесс (закон Шарля). 6.Закрепление 7.Задание на дом Объяснение нового материала: Для того чтобы устоновить,в каком состоянии находиться газ, нам необходимо знать его термодинамические параметры: давление, температура, объем. Изменение одного из термопараметров приводит к изменению других его параметров. Уравнение, которое связывает между собой термодинамические параметры, называют уравнением состояние N газа. Нам известно, что P nkT .Так как эн концентрация молекул газа n , где NV N kT откуда следует,что PV NkT . Число V m N A . С учетом этого получим: молекул газа найдем, зная количество вещества газа; N M общее число молекул; V- объем. то P PV m N AkT M Величина, равная произведению двух постоянных чисел- постоянной Авогадро и постоянной Больцмана, сама будет постоянной величиной. Ее называли универсальной газовой постоянной-R; N Ak R R 1.38 10 23 Дж 1 Дж 6,02 1023 8,31 К моль К моль 1 ; постояннойАвогадро моль k 1.38 *10 23 Дж / К ; постояннойБольцмана N A 6.02 *10 23 R N A * k 8.31 Дж / моль * К m RT это уравнение называется уравнением M состояние идеального газа.Уравнение носит название Менделеева –Клапейрона. С учетом сказанного получим PV Изопроцессы - процессы изменения состояния газов так, что один из трех макроскопических параметров (объем, давление, температура) остается постоянным, а два других параметра при этом изменяются. а) Изотермический процесс- процесс изменения состояния определенной массы газа при постоянной температуре (m=const, T=const). Из уравнения Менделеева-Клайперона m RT . Это означает, что произведение следует закон Бойля-Мариотта PV Const M начального давления Р1 на его первоначальный объем равно произведению этих P P параметров P2 V2 в произвольной момент времени P1 V1 P2 V2или 1 2 следовательно V1 V2 график гипербола, название - изотерма. б) Изобарный процесс - процесс изменения состояния определенной массы газа при постоянном давлении (m=const, P=const).Из уравнения Менделеева - Клайперона следует V mRT закон Гей-Люссака. const -это означает, что отношение первоначального T MP V объема газа к его температуре T1 равно отношению этих параметров 2 в произвольный T2 момент времени. V1 V2 илиV1T1 V2T2 следует V~T. T1 T2 График - прямая, название - изобара. в) Изохорный процесс - процесс изменения состояния определенной массы при постоянном объеме( m constV const ). Из уравнения Менделеева - Клайперона следует P mR закон Шарля const - это означает, что отношение первоначального давления T MV газа P1 к его температуре равно отношению этих параметров P2 ,T2 - в произвольный момент времени P1 P2 илиP1 T2 P2T1 следует Р пропорционально Т. График - прямая, T1 T2 название- изохора. Контрольные вопросы 1.Какие процессы называют изопроцессами? 2.Как читается закона Бойля-Мариотта? 3. Какие процессы называют изотермическим? Домашняя задания: Упр.20 №4-№7