Тест по теме: «Неметаллы»
advertisement
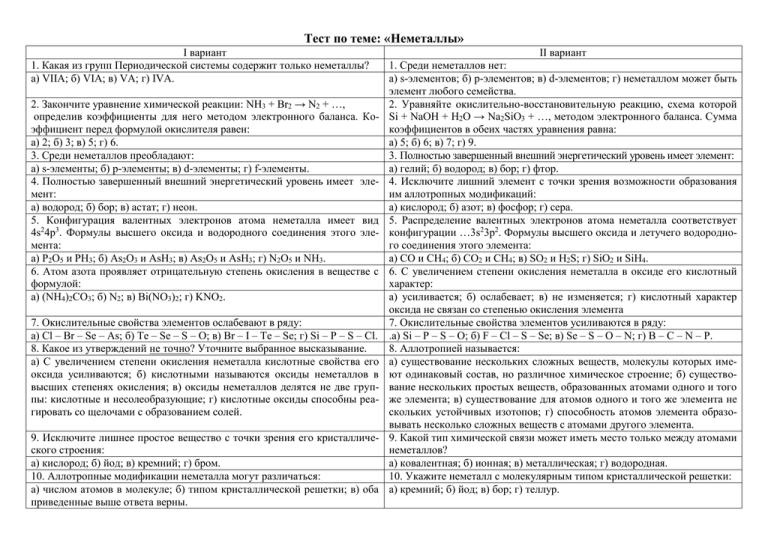
Тест по теме: «Неметаллы» I вариант 1. Какая из групп Периодической системы содержит только неметаллы? а) VIIА; б) VIА; в) VА; г) IVА. 2. Закончите уравнение химической реакции: NH3 + Br2 → N2 + …, определив коэффициенты для него методом электронного баланса. Коэффициент перед формулой окислителя равен: а) 2; б) 3; в) 5; г) 6. 3. Среди неметаллов преобладают: а) s-элементы; б) p-элементы; в) d-элементы; г) f-элементы. 4. Полностью завершенный внешний энергетический уровень имеет элемент: а) водород; б) бор; в) астат; г) неон. 5. Конфигурация валентных электронов атома неметалла имеет вид 4s24p3. Формулы высшего оксида и водородного соединения этого элемента: а) Р2О5 и РН3; б) As2O3 и AsH3; в) As2O5 и AsH3; г) N2O5 и NH3. 6. Атом азота проявляет отрицательную степень окисления в веществе с формулой: а) (NH4)2CO3; б) N2; в) Bi(NO3)2; г) KNO2. 7. Окислительные свойства элементов ослабевают в ряду: а) Cl – Br – Se – As; б) Te – Se – S – O; в) Br – I – Te – Se; г) Si – P – S – Cl. 8. Какое из утверждений не точно? Уточните выбранное высказывание. а) С увеличением степени окисления неметалла кислотные свойства его оксида усиливаются; б) кислотными называются оксиды неметаллов в высших степенях окисления; в) оксиды неметаллов делятся не две группы: кислотные и несолеобразующие; г) кислотные оксиды способны реагировать со щелочами с образованием солей. 9. Исключите лишнее простое вещество с точки зрения его кристаллического строения: а) кислород; б) йод; в) кремний; г) бром. 10. Аллотропные модификации неметалла могут различаться: а) числом атомов в молекуле; б) типом кристаллической решетки; в) оба приведенные выше ответа верны. II вариант 1. Среди неметаллов нет: а) s-элементов; б) p-элементов; в) d-элементов; г) неметаллом может быть элемент любого семейства. 2. Уравняйте окислительно-восстановительную реакцию, схема которой Si + NaOH + H2O → Na2SiO3 + …, методом электронного баланса. Сумма коэффициентов в обеих частях уравнения равна: а) 5; б) 6; в) 7; г) 9. 3. Полностью завершенный внешний энергетический уровень имеет элемент: а) гелий; б) водород; в) бор; г) фтор. 4. Исключите лишний элемент с точки зрения возможности образования им аллотропных модификаций: а) кислород; б) азот; в) фосфор; г) сера. 5. Распределение валентных электронов атома неметалла соответствует конфигурации …3s23p2. Формулы высшего оксида и летучего водородного соединения этого элемента: а) СО и СН4; б) СО2 и СН4; в) SO2 и H2S; г) SiO2 и SiH4. 6. С увеличением степени окисления неметалла в оксиде его кислотный характер: а) усиливается; б) ослабевает; в) не изменяется; г) кислотный характер оксида не связан со степенью окисления элемента 7. Окислительные свойства элементов усиливаются в ряду: .а) Si – P – S – O; б) F – Cl – S – Se; в) Se – S – O – N; г) B – C – N – P. 8. Аллотропией называется: а) существование нескольких сложных веществ, молекулы которых имеют одинаковый состав, но различное химическое строение; б) существование нескольких простых веществ, образованных атомами одного и того же элемента; в) существование для атомов одного и того же элемента не скольких устойчивых изотопов; г) способность атомов элемента образовывать несколько сложных веществ с атомами другого элемента. 9. Какой тип химической связи может иметь место только между атомами неметаллов? а) ковалентная; б) ионная; в) металлическая; г) водородная. 10. Укажите неметалл с молекулярным типом кристаллической решетки: а) кремний; б) йод; в) бор; г) теллур. 11. Какой неметалл обладает молекулярной кристаллической решеткой? 11. Наиболее сильные восстановительные свойства из перечисленных ионов проявляет анион: а) бром; б) кислород; в) белый фосфор; г) все перечисленные выше отве- а) F-; б) Cl- г) Br- д) I-. ты верны. 12. Какова причина того, что число простых веществ-неметаллов превос- 12. Простые вещества – неметаллы при нормальных условиях имеют агходит число элементов-неметаллов? регатное состояние: а) явление аллотропии; б) явление изомерии; в) возможность существо- а) газообразное; б) жидкое; в) твердое; г) все перечисленные выше ответы вания неметаллов в трех агрегатных состояниях; г) элемент-металл может верны. образовывать простое вещество– неметалл. 13. С какими из перечисленных веществ в соответствующих условиях 13. С какими из перечисленных веществ в соответствующих условиях способен взаимодействовать бром: 1) этан, 2) алюминий, 3) хлорид способен взаимодействовать кислород: 1) метан, 2) оксид кремния (IV), натрия, 4) гидроксид калия, 5) оксид углерода (IY), 6) сероводород; 7) 3) серная кислота, 4) сульфид цинка, 5) фосфор, 6) гидроксид магния, 7) сульфат магния? Напишите уравнения возможных реакций. метиламин? Напишите уравнения возможных реакций. а) 1, 2, 6, 7; б) 1, 2, 3, 4; в) 1, 2, 4,5; г) 1, 2, 4, 6. а) 1, 4, 5, 7; б) 1, 2, 5, 6; в) 2, 4, 5, 7; г) 1, 3, 5, 7. 14. При взаимодействии с каким из перечисленных веществ сера прояв- 14. При взаимодействии в каким веществом водород проявляет окислиляет окислительные свойства? тельные свойства? а) О2; б) Zn; в) Н2SО4 (конц.); г) НNО3 (конц.). а) хлор; б) натрий; в) кислород; г) этаналь. 15. В ряду галогеноводородов HF – HCl – HBr – HI длина связи: 15. Какие неметаллы не взаимодействуют друг с другом? а) увеличивается; б) уменьшается; в) не изменяется; г) изменяется перио- а) углерод и водород; б) сера и фосфор; в) углерод и кремний; г) кремний дически. и водород. 16. Пара формул, в которой кислотный оксид не соответствует кислоте: 16. В каком веществе связь Э – О наиболее полярна? а) N2O3 и HNO2; б) SiO2 и H2SiO3; в) SO3 и H2SO3; г) Р2О5 и Н3РО4. а) SO2; б) NO; в) Н2О; г) Cl2O. 17. При взаимодействии цинка с концентрированной серной кислотой 17. Найдите пару, в которой кислотный оксид не соответствует кислоте: образуется сера. Сумма коэффициентов в данном уравнении равна: а) 7; б) 12; в) 15; г) 18. а) В2О3 и Н3ВО3; б) N2O3 и HNO3; в) Cl2O7 и НClO4; г) SO2 и Н2SO3. 18. Напишите уравнения реакций, соответствующих цепочке превращений: 18. Напишите уравнения реакций, с помощью которых можно осущеHNO2 ; H 2O H 2O ; LiOH O2 ( Pt ); H 2O Li ствить превращения: X1 t NH3 X3 X2 X4 O2 СН4 → СО2 → NaHCO3 → Na2CO3 → CaCO3 → CO2 → CO X5 X6. Вещество Х6 имеет формулу: NaOH ,t , p X. Вещество Х имеет формулу: а) N2O; б) NO; в) N2O3; г) NO2; д) N2O5. а) HCOONa; б) NaHCO3; в) Na2CO3; г) Na2C2O4.


