Министерство науки и высшего образования Российской Федерации
Федеральное государственное автономное образовательное
учреждение высшего образования
«НАЦИОНАЛЬНЫЙ ИССЛЕДОВАТЕЛЬСКИЙ
ТОМСКИЙ ПОЛИТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ»
Инженерная школа природных ресурсов
Направление подготовки 18.03.01 «Химическая технология»
Образовательная программа «Химическая технология переработки нефти и газа»
ОТЧЕТ ПО ЛАБОРАТОРНОЙ РАБОТЕ
Название работы
Оценка пористой структуры катализаторов сорбционными методами. Часть 1
Вариант
Вариант 5
По дисциплине
Макрокинетика химических процессов
Студент
Группа
ФИО
Подпись
2Д02
Гладыш Полина Валерьевна
Дата
28.01.24
Руководитель
Должность
ФИО
Ученая степень,
звание
Доцент
Юрьев Е.М.
к.т.н.
Томск – 2024 г.
Подпись
Дата
Часть I
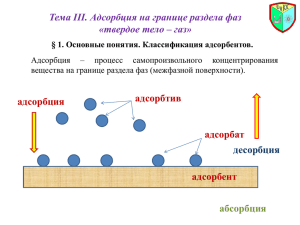
Цель работы: определить удельную поверхность пористого материала
по уравнению Лэнгмюра, уравнению БЭТ и уравнению Гаркинса-Юра и
сравнить их между собой.
Теоретическая часть
I.
В
Определение удельной поверхности твердых тел.
лабораторной
практике
удельная
поверхность
катализатора
оценивается по результатам адсорбционных опытов при постоянной
температуре. В качестве адсорбата используется, как правило, инертный газ –
азот, криптон, аргон. Опыты проводятся при температурах ниже критической
температуры газа и несколько выше температуры кипения газа при
атмосферном давлении.
Площадь удельной поверхности пористого материала определяется по
следующему уравнению:
s уд A s0 N A
,
(1)
где A - максимальная емкость монослоя (т.е. максимальное количество
вещества, которое может сорбировать поверхность материала массой 1 кг, при
допущении, что адсорбционный слой не превышает одну молекулу), моль/кг;
s0 - поверхность, занимаемая одной молекулой адсорбата, м2; N A - постоянная
Авогадро, число структурных единиц веществ в 1 моль вещества,
N A 6,02 1023 моль-1.
Поверхность s0 , занимаемая одной молекулой адсорбата, как правило,
постоянна для пары «адсорбат-адсорбент» и представляет собой справочную
величину.
Максимальная емкость монослоя A определяется по результатам
адсорбционных опытов. Чтобы определить величину A из изотермы
адсорбции, необходимо задаться определенной моделью для ее описания.
2
II.
Определение удельной поверхности по уравнению Лэнгмюра.
В том случае, если наблюдается протекание мономолекулярной
адсорбции (тип I изотермы), т.е. образуется слой в одну молекулу, применима
теория Лэнгмюра. Определение удельной поверхности по уравнению
Лэнгмюра также сводится к определению величины ёмкости монослоя A с
последующим использованием уравнения (1).
Рассмотрим
определение
A
по
теории
адсорбции
Лэнгмюра.
Уравнение изотермы адсорбции Лэнгмюра выглядит следующим образом:
A A
Kp
1 Kp ,
где A - адсорбция, моль/кг; К – постоянная уравнения Лэнгмюра,
характеризующая взаимодействие адсорбата и адсорбента; p – давление пара
адсорбата, Па.
Для нахождения
A
уравнение изотермы адсорбции Лэнгмюра
линеаризуют и представляют в следующем виде:
p
1
p
A A K A
1
p
Строя график в координатах p - A , можно определить величины A K
1
и A :
p
A
1
A K
tg
1
A
p
3
1
— A K - это отрезок, отсекаемый прямой на оси ординат;
1
— A - численно равен тангенсу угла наклона прямой.
Из полученной системы уравнений определяют A и рассчитывают
удельную поверхность
III.
s уд
.
Определение удельной поверхности по уравнению теории
БЭТ.
В настоящее время стандартным методом определения удельной
поверхности является теория адсорбции БЭТ (Брунауэра-Эммета-Теллера).
Уравнение изотермы адсорбции БЭТ выглядит следующим образом:
A
A C p / ps
(1 p / ps ) 1 (C 1) p / ps
,
где A - адсорбция, моль/кг; С – постоянная, характеризующая энергию
взаимодействия сконденсированного адсорбата с поверхностью адсорбента; p
– давление пара адсорбата, Па; ps - давление насыщенных паров адсорбата
(индекс s означает «saturation» — насыщение), Па.
Для нахождения A уравнение изотермы адсорбции БЭТ линеаризуют и
представляют в следующем виде:
p / ps
1
C 1 p
A(1 p / ps ) A C A C ps
p
p / ps
Строя график в координатах ps - A(1 p / ps ) , можно определить
1
C 1
величины A C и A C :
4
p / ps
A(1 p / ps )
tg
p
ps
1
A C
1
𝐴∞ ∙ 𝐶
𝐶−1
𝐴∞ ∙ 𝐶
C 1
A C
- это отрезок, отсекаемый прямой на оси ординат;
- численно равен тангенсу угла наклона прямой.
Из полученной системы уравнений определяют A и рассчитывают
удельную поверхность
IV.
s уд
.
Определение удельной поверхности по уравнению Гаркинса-
Юра.
Для описания полимолекулярной адсорбции возможно использование и
других уравнений, в частности уравнения Гаркинса–Юра, имеющего
термодинамическую природу. Это уравнение получено на основе объединения
уравнения состояния конденсированной плёнки адсорбата на поверхности
адсорбента (состояние которой аналогично состоянию адсорбционных плёнок
поверхностно-активных веществ на поверхности жидкости) и адсорбционного
уравнения Гиббса. Уравнение изотермы адсорбции Гаркинса–Юра имеет вид:
ln
p
C
B 2
ps
A ,
где B и С — константы уравнения Гаркинса-Юра. Для их нахождения
экспериментальные данные представляются в координатах
1
p
ln
2
A
ps .
Отрезок, отсекаемый на оси ординат, соответствует константе В. По тангенсу
5
угла наклона прямой определяют константу С. Значение этой константы
зависит от величины удельной поверхности:
C
2 RT
s
2
уд
2
s уд
2
K ГЮ
,
2
где K ГЮ — константа уравнения Гаркинса-Юра, которая определяется
по данным адсорбции на адсорбенте с известной удельной поверхностью.
По известной константе С можно определить удельную поверхность
образца:
s уд K ГЮ C
Задание:
Получены результаты опыта адсорбции-десорбции азота на пористом
материале при ок. 77,35 К. Рассчитать значение удельной поверхности
пористого материала по различным теориям адсорбции. Принять поверхность,
занимаемую одной молекулой адсорбата, — 0,162 нм2. Область изотермы
адсорбции, рекомендуемая для выбора прямой и проведения расчетов:
p
(0,05;0,35)
ps
. Следует использовать адсорбционную кривую, а не
десорбционную. Константу уравнения Гаркинса-Юра для азота принять
9,09 · 104 м2/моль.
Ход работы:
1.
Ознакомьтесь с исходными данными Вашего варианта.
2.
Постройте
изотерму
адсорбции-десорбции
в
координатах
относительное давление — адсорбция (ммоль/г). Представьте изотерму и в
линейных, и в логарифмических координатах, проверьте, хорошо ли видно на
графиках адсорбционно-десорбционный гистерезис.
3.
По известным результатам опыта с азотом постройте изотерму
p
теории Лэнгмюра в координатах p - A . По полученному графику оцените
6
емкость монослоя A , затем рассчитайте удельную поверхность пористого
материала
4.
s уд
.
По известным результатам опыта с азотом постройте изотерму
p
p / ps
теории БЭТ в координатах ps - A(1 p / ps ) . По полученному графику
оцените емкость монослоя A , затем рассчитайте удельную поверхность
пористого материала
5.
s уд
.
По известным результатам опыта с азотом постройте изотерму
1
p
ln
2
ps . По полученному графику
теории Гаркинса-Юра в координатах A
оцените константу С, затем рассчитайте удельную поверхность пористого
материала
6.
s уд
.
Подготовьте отчет о проделанной работе, в отчете приведите
изотерму адсорбции-десорбции, укажите удельную поверхность пористого
материала, определенную по уравнению Лэнгмюра, уравнению БЭТ и
уравнению
Гаркинса-Юра.
Сравните
поверхности.
7
полученные
значения
удельной
Исходные данные:
Исходные данные представлены в Приложении А.
Результаты
1.
Ознакомились с данными варианта.
2.
Построили изотерму адсорбции-десорбции
логарифмических координатах.
в
линейных
и
6
Адсорбция A, ммоль/ru
5
4
3
2
1
0
0
10
20
30
40
50
60
70
80
90
100
Давление P, кПа
Рисунок 1 – Изотерма адсорбции-десорбции в линейных координатах
По известным результатам опыта с азотом построили изотерму
p
теории Лэнгмюра в координатах p - A .
3.
35
30
Р/А, кПа·г/ммоль
25
20
15
y = 0,4535x + 0,9161
10
5
0
0
10
20
30
40
50
Давление P, кПа
Рисунок 2 – Изотерма теории Лэнгмюра
8
60
70
По полученному графику оценили емкость монослоя 𝐴∞ , затем
рассчитали удельную поверхность пористого материала 𝑠уд .
Из рисунка находим:
1
1
1
моль
→ А∞ = =
= 2,2
А∞ ∙ 𝑘
𝑘 0,45
кг
Площадь удельной поверхности пористого материала определяется по
следующему уравнению:
𝑠уд = 𝐴∞ ∙ 𝑠0 ∙ 𝑁𝐴 = 2,2 ∙ 0,162 ∙ 10−18 ∙ 6,02 ∙ 1023 = 2,15 ∙ 105 м2/кг =
215 м2/г
4.
По известным результатам опыта с азотом построили изотерму
теории БЭТ в координатах
𝑝
𝑝𝑠
-
𝑝/𝑝𝑠
𝐴(1−𝑝/𝑝𝑠 )
.
0,3
,кг/моль
0,25
0,2
0,15
y = 0,7736x - 0,0222
0,1
0,05
0
0,05
0,1
0,15
0,2
0,25
0,3
0,35
0,4
Рисунок 3 – Изотерма теории БЭТ
По полученному графику оценили емкость монослоя A , затем
рассчитали удельную поверхность пористого материала
Из представленного рисунка находим:
1
= 𝑏 = −0,0222
А∞ ∙ С
С−1
= 𝑡𝑔𝛼 = 𝑘 = 0,7736
{А∞ ∙ С
9
s уд
.
А∞ = 1,33
моль
кг
C = -33,85
Площадь удельной поверхности пористого материала определяется по
следующему уравнению:
𝑠уд = 𝐴∞ ∙ 𝑠0 ∙ 𝑁𝐴 = 1,33 ∙ 0,162 ∙ 10−18 ∙ 6,02 ∙ 1023 = 1,29 ∙ 105 м2 /кг
= 129 м2/г
5.
По известным результатам опыта с азотом построена изотерму
1
p
ln
2
ps .
теории Гаркинса-Юра в координатах A
0
0,2
0,22
0,24
0,26
0,28
0,3
0,32
0,34
-1
-2
-3
-4
y = -45,651x + 9,8275
-5
Рисунок 4 – Изотерма теории Гаркинса-Юра
С = 𝑡𝑔𝛼 = 45,65 (
моль 2
)
кг
По известной константе С можно определить удельную поверхность
образца:
𝑠уд = 𝐾ГЮ ∙ √𝐶 = 9,09 ∙ 104 ∙ √45,65 = 6,14 ∙ 105 м2 /кг = 614 м2/г
По полученному графику оценена константу С и рассчитана удельная
поверхность пористого материала 𝑠уд .
10
Вывод
В ходе данной лабораторной работы была проведена оценка пористой
структуры катализаторов сорбционными методами, построена изотерма
адсорбции-десорбции в линейных и логарифмических координатах.
Из графика изотермы теории Лэнгмюра с применением расчетов
получена
удельная
поверхность
пористого
материала,
равная
s уд = 2,15 ∙ 105 м2 /кг = 215 м2/г, оценена емкость монослоя, которая составила
A = 2,2 моль/кг.
По теории БЭТ емкость монослоя составила A =1,33 моль/кг, удельная
поверхность пористого материала s уд = 1,29 ∙ 105 м2 /кг = 129 см2/г.
По графику изотермы теории Гаркинса-Юра было определено значение
константы С, которое составило 45,65. Удельная поверхность по расчетам
составила 6,14 ∙ 105 м2 /кг = 614 м2/г.
По теории БЭТ считается удельная поверхность более точной
𝑠уд , м2/г
По Лэнгмюру
По БЭТ
По Гаркинсу-Юру
215
129
614
11
Приложение А
Таблица 1 – Исходные данные для варианта № 5
Температура
К
77,35
Давление
кПа
0,024272271
0,294023721
0,590530478
1,184779981
2,819149507
6,345771718
7,584127908
9,152473109
11,08981423
13,58234359
15,13340557
17,5974074
20,06449431
22,55866436
25,04331778
27,52718391
30,01260428
32,03163222
34,02355668
37,92462023
41,92181034
45,93042529
49,91219104
53,90745667
57,90016309
61,87198093
65,87041605
69,99943536
73,98129469
77,82521774
81,77937753
85,77923668
88,74919983
90,06920063
91,04716405
92,06696975
93,02042346
94,04845601
94,97749766
Адсорбция
ммоль/г
ДНП
кПа
0,867427055
1,588693077
1,695315362
1,775614949
1,854030144
1,914912167
1,927288015
1,940361239
1,953494354
1,967382953
1,975008479
1,985376181
1,995106264
2,004210973
2,012624498
2,02101999
2,028967882
2,035623904
2,042458254
2,055661058
2,07032926
2,085243046
2,10158007
2,120668375
2,141050113
2,164412072
2,191760066
2,226600075
2,269505049
2,323467505
2,400894782
2,51958168
2,657377679
2,73770785
2,809745624
2,893636631
2,988767837
3,110441155
3,254686964
99,95517377
100,0812132
100,105194
100,1171885
100,1109634
100,1125176
100,1136894
100,1196378
100,1137627
100,1153332
100,1247644
100,1219895
100,1132093
100,1197192
100,1049825
100,1029725
100,1054137
100,1022727
100,1007673
100,097553
100,0917837
100,0953071
100,0966579
100,100393
100,079602
100,0776165
100,0723923
100,0749882
100,0682016
100,0772666
100,0782268
100,0717169
100,0583961
100,0764122
100,0614069
100,0749231
100,0585914
100,0820921
100,0691618
100,0619114
12
Площадь
нм2
молекулы
0,162
95,62524728
96,05519249
96,57172728
97,02883498
97,53246392
98,059561
98,2655581
98,53315497
98,81367396
99,03865551
99,14957577
99,47089545
99,63701139
99,73118498
99,58400467
99,06412542
98,57367085
98,57305241
98,01874403
97,18836779
96,3454112
96,18618761
95,63152932
95,15452579
94,20424565
93,19550676
92,17666127
91,16146946
90,17361915
89,12992219
86,53286954
82,31559657
78,29539403
74,42598478
70,42
66,33437947
62,27210681
58,24597214
54,24694299
50,23060976
46,02512781
42,23333671
36,35113273
32,20682131
28,18014143
3,362394984
3,445734986
3,55196236
3,659592693
3,796703511
3,943440557
4,01971965
4,142664229
4,277466534
4,389205584
4,501701251
4,669339003
5,031079227
5,463544924
5,074975597
4,814912354
4,577971295
4,553774062
4,307295098
4,057943462
3,864260461
3,832065739
3,736190717
3,660680855
3,529668147
3,407765344
3,300158477
3,205348855
3,11846721
3,040223251
2,875748398
2,672825196
2,546606351
2,47030989
2,416932795
2,376422771
2,343567372
2,315679104
2,289203758
2,263506304
2,108259355
2,061958489
2,035332205
2,022094523
2,009386641
13
100,0561014
100,0576312
100,0550761
100,0568663
100,047077
100,0347408
100,0388258
100,0410961
100,0305664
100,0260257
100,0201099
100,0222663
100,0023704
100,0136895
100,0159761
100,019231
100,0214851
100,0260257
100,0317707
100,0463365
100,054596
100,0615615
100,0697314
100,0719773
100,0669322
100,0589413
100,0434315
100,0461412
100,0643771
100,0474758
100,0613662
100,0667613
100,1326495
100,1372796
100,1103775
100,0861282
100,1064879
100,1265546
100,1545796
100,1431955
100,1028179
100,119589
100,1034282
100,0813028
100,101044
25,10927713
20,10818172
15,44340008
10,04108534
2,000007629
1,983712582
1,965965676
1,937670163
14
100,0879021
100,0788371
100,0594865
100,0484767