Измерение плотности вещества с учетом погрешности
advertisement
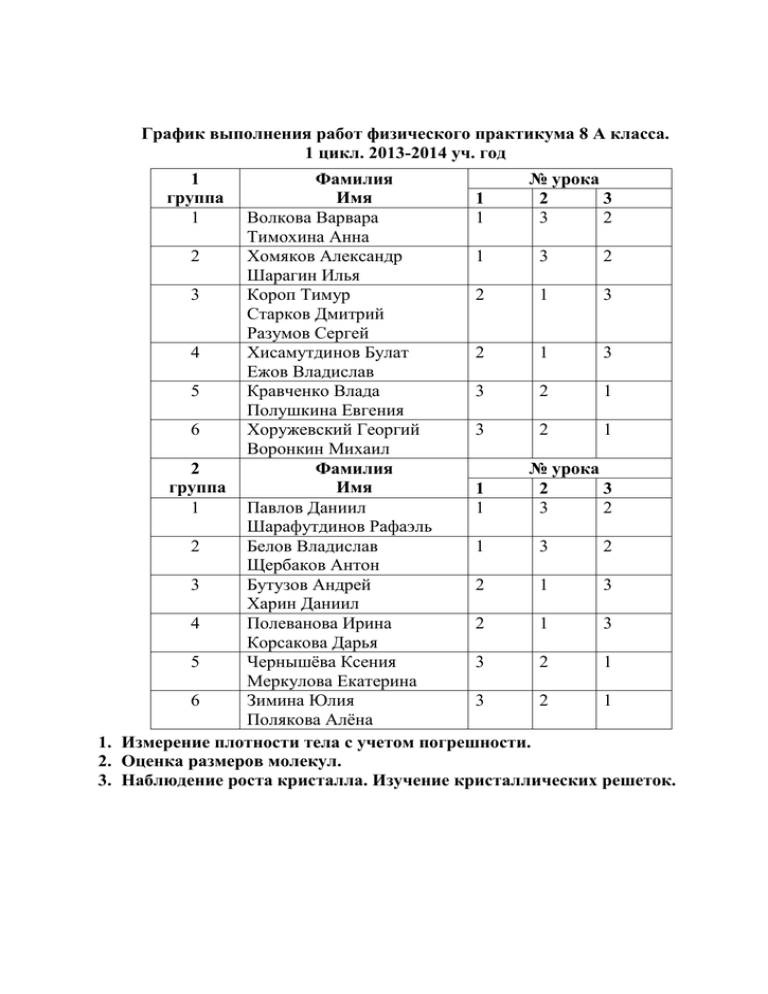
График выполнения работ физического практикума 8 А класса. 1 цикл. 2013-2014 уч. год Фамилия № урока Имя 1 2 3 Волкова Варвара 1 3 2 Тимохина Анна 2 Хомяков Александр 1 3 2 Шарагин Илья 3 Короп Тимур 2 1 3 Старков Дмитрий Разумов Сергей 4 Хисамутдинов Булат 2 1 3 Ежов Владислав 5 Кравченко Влада 3 2 1 Полушкина Евгения 6 Хоружевский Георгий 3 2 1 Воронкин Михаил 2 Фамилия № урока группа Имя 1 2 3 1 Павлов Даниил 1 3 2 Шарафутдинов Рафаэль 2 Белов Владислав 1 3 2 Щербаков Антон 3 Бутузов Андрей 2 1 3 Харин Даниил 4 Полеванова Ирина 2 1 3 Корсакова Дарья 5 Чернышёва Ксения 3 2 1 Меркулова Екатерина 6 Зимина Юлия 3 2 1 Полякова Алёна 1. Измерение плотности тела с учетом погрешности. 2. Оценка размеров молекул. 3. Наблюдение роста кристалла. Изучение кристаллических решеток. 1 группа 1 Лабораторная работа №1 Измерение плотности вещества с учетом погрешности Оборудование и материалы: твердое тело на нити, весы с гирями, мензурка, стакан с водой. Указания к выполнению работы 1. Измерьте массу тела ( m) на рычажных весах. 2. Определите с помощью графика и таблицы абсолютную погрешность измерения массы тела Δm = Δmвесов + Δmгирь 3. Определите относительную погрешность измерения массы εm m m m 4. Измерьте объем воды в мензурке V1. 5. Удерживая тело за нить, осторожно опустите его в воду. Измерьте объем воды вместе с погруженным в него телом V2. 6. Определите объем тела V = V2 - V1 7. Определите абсолютную погрешность измерения объема тела. Так как для определения объема тела нужно было дважды измерить объем жидкости, то ΔV = 2(ΔVмензурки + ΔVотсчета) =2( 0,5 ЦД +0,5 ЦД) = 2ЦД 8. Определите относительную погрешность измерения объема тела V VV 9. Рассчитайте плотность тела m V 10. Рассчитайте относительную погрешность измерения плотности ερ = εm + εV 11. Рассчитайте абсолютную погрешность измерения плотности Δρ=ρ·ερ 12. Результаты измерений и вычислений занесите в таблицу. m,г Δ m,г εm V1,см3 V2,см3 V,см3 ΔV,см3 εV ρ,г/см3 ερ 13. Запишите результат в виде ρ ± Δρ Δρ,г/см3 Лабораторная работа №2 Оценка размеров молекул мыла. Оборудование и материалы: 0,5 % - ный раствор мыла в воде, пипетка, кювета, весы, разновес, небольшой стакан, тальк, сосуд с водой. Метод выполнения работы. Наиболее простой метод оценки размеров молекул основан на свойстве некоторых веществ образовывать на поверхности воды тончайшие пленки толщиной в одну молекулу. Измерив толщину такой пленки, можно принять ее равной диаметру молекулы. Если на поверхность воды капнуть немного водного раствора мыла, то мыло образует на поверхности воды пленку, которую можно считать мономолекулярной. Для наблюдения пленки и измерения ее площади поверхность воды предварительно посыпают тальком. Мыло уменьшает поверхностное натяжение воды, поэтому плавающие частицы талька перемещаются от места падения капли к краям пленки, что приводит к появлению «окна». Порядок выполнения работы. 1.Накапайте в стакан с помощью пипетки n=40 капель мыльного раствора. Определите массу всех капель m1 с помощью весов ( не забудьте учесть массу стакана). Затем найдите массу одной капли m2 m2 m1 n 2.Найдите массу мыла М в капле мыльного раствора m2 - 100% М - 0,5% М= 3. Определите объем мыла в капле V M m2 0,5 100 ρ (мыла) = 1040 кг/м3 4.Посыпьте поверхность D1 воды слоем талька и h -толщина пленки, равная D2 осторожно капните в диаметру одной центр кюветы с высоты молекулы 1-2 мм одну каплю раствора. Измерьте линейкой диаметр «окна» в двух взаимно перпендикулярных направлениях и определите средний диаметр окна D. D D1 D2 2 5. Определите площадь поверхности «окна». S D 2 4 ( формула площади круга) 6. Определите толщину слоя мыльной пленки h V S 7.Результаты измерений и вычислений занесите в отчетную таблицу. Масса 40 капель мыльного раствора, m1(кг) Масса одной капли мыльного раствора, m2(кг) Масса мыла в одной капле раствора, М(кг) Объем Диаметр Площадь Толщина мыла в «окна», поверхности слоя капле, D(м) «окна», мыльной 3 2 V(м ) S(м ) пленки, h(м) Контрольные вопросы. 1. Каков источник ошибок ( не считая инструментальных) в этом методе определения размеров молекул? Лабораторная работа №3 Наблюдение роста кристаллов. Изучение кристаллических решеток некоторых веществ на моделях. Современные методы исследования структуры вещества показали, что кристаллические решетки ряда твердых тел, например металлов, поваренной соли и др., имеют структуру типа плотно упакованных шаров одинаковых или разных размеров. Это позволяет исследовать эти структуры с помощью простых моделей. В данной работе вы на моделях познакомитесь с двумя кристаллическими структурами: кубической решеткой поваренной соли (хлорида натрия) и гранецентрированной кубической решеткой меди, серебра, платины. Приборы и материалы: шарики одинакового диаметра, пластилин, насыщенный раствор поваренной соли, микроскоп, линейка, мензурка, вода. Задание 1. Нанесите на предметное стекло тонкий слой раствора поваренной соли и с помощью микроскопа наблюдайте рост кристаллов. Обратите внимание на углы между гранями кристаллов. Зарисуйте некоторые кристаллы в тетради. Фотографии двух кристаллических веществ. а) Обычная поваренная соль. Обратите внимание на кубическую форму кристаллов. б) Сахар. Кристаллическая структура орторомбическая, каждая из граней отдельных кристаллов является плоскостью плотной упаковки молекул сахара Задание 2. В кристаллических телах частицы располагаются в строгом порядке, образуя пространственные периодически повторяющиеся структуры во всем объеме тела. Для наглядного представления таких структур используются пространственные кристаллические решетки, в узлах которых располагаются центры атомов или молекул данного вещества. Чаще всего кристаллическая решетка строится из ионов (положительно и отрицательно заряженных) атомов, которые входят в состав молекулы данного вещества. Например, решетка поваренной соли содержит ионы Na+ и Cl–, не объединенные попарно в молекулы NaCl. Такие кристаллы называются ионными. Зная что кристаллы поваренной соли состоят из двух типов атомов Na+ и Cl- (натрий и хлор), соберите из пластилиновых шариков различного цвета модель кубической кристаллической решетки хлорида натрия (поваренной соли) NaCl. В простой кубической решетке частицы располагаются в вершинах куба. На рисунках внизу изображены модели строения кристалла поваренной соли. Два левых рисунка показывают одну и ту же модель под разными углами зрения: со стороны грани и со стороны угла. Ионы натрия и хлорид-ионы схематически изображены в виде шариков разного цвета. На правом рисунке изображена немного другая модель строения кристалла соли. Она имеет специальное название – кристаллическая решетка – и состоит из "узлов" и "ребер". Кроме пространственного расположения частиц в кристалле, она показывает и направления наиболее прочных связей между частицами. Задание 3. По типу гранецентрированного куба строится упаковка атомов в таких металлах, как медь, серебро, платина. Пространственная решетка такого типа показана на рисунке. Элементарная ячейка кристалла имеет форму куба, в котором атомы расположены в вершинах куба и в центрах граней, что нашло отражение в названии решетки гранецентрированный куб. Кристаллическая решетка меди - кубическая гранецентрированная. Последнее слово означает, что в ней, помимо 8 атомов меди в вершинах, есть еще 6 атомов в центре каждой грани куба. Такая же кристаллическая решетка у серебра, алюминия, золота, свинца и многих других металлов Чтобы выяснить характер упаковки, возьмите кубическую коробку и уложите в ней шарики послойно. Вы получите плотнейшую упаковку в виде гранецентрированного куба. Важнейшей характеристикой кристаллической решетки является ее степень заполнения: отношение суммарного объема атомов, из которых построена решетка, к объему кристалла. Степень заполнения показывает, какая часть кристалла заполнена частицами. Определите объем одного шарика V0 с помощью мензурки. Подсчитайте число шариков N в кубической коробке. Определите объем кубической решетки V с помощью линейки. Вычислите степень заполнения по формуле N V0 . Результаты измерений и вычислений занесите в таблицу. V Объем одного Длина ребра шарика куба 3 V0, мм L, мм Объем куба V, мм3 Число шариков в кубе N Контрольные вопросы. 1. Какие твердые тела называются кристаллами? 2. Что означает понятие «дальний порядок»? Степень заполнения %
