Календарно-тематическое планирование учебного материала по химии 8 класс
advertisement
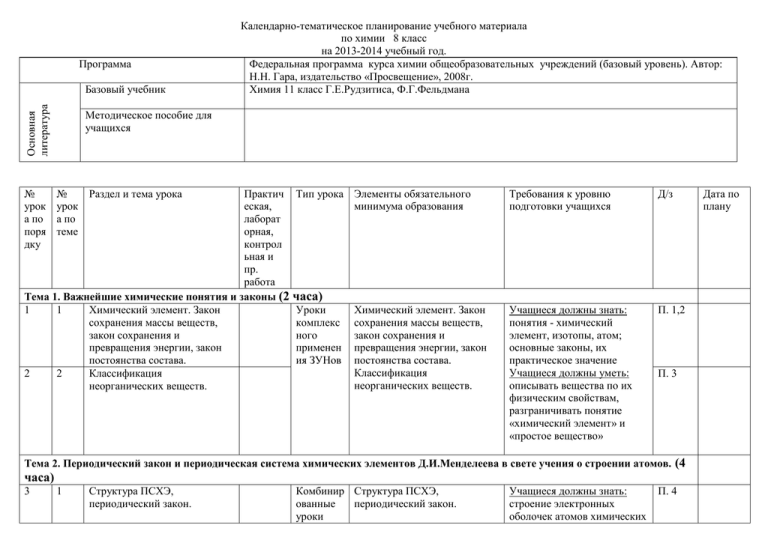
Программа Основная литература Базовый учебник № урок а по поря дку Календарно-тематическое планирование учебного материала по химии 8 класс на 2013-2014 учебный год. Федеральная программа курса химии общеобразовательных учреждений (базовый уровень). Автор: Н.Н. Гара, издательство «Просвещение», 2008г. Химия 11 класс Г.Е.Рудзитиса, Ф.Г.Фельдмана Методическое пособие для учащихся № Раздел и тема урока урок а по теме Практич Тип урока еская, лаборат орная, контрол ьная и пр. работа Тема 1. Важнейшие химические понятия и законы (2 часа) 1 1 Химический элемент. Закон Уроки сохранения массы веществ, комплекс закон сохранения и ного превращения энергии, закон применен постоянства состава. ия ЗУНов 2 2 Классификация неорганических веществ. Элементы обязательного минимума образования Требования к уровню подготовки учащихся Д/з Химический элемент. Закон сохранения массы веществ, закон сохранения и превращения энергии, закон постоянства состава. Классификация неорганических веществ. Учащиеся должны знать: понятия - химический элемент, изотопы, атом; основные законы, их практическое значение Учащиеся должны уметь: описывать вещества по их физическим свойствам, разграничивать понятие «химический элемент» и «простое вещество» П. 1,2 П. 3 Тема 2. Периодический закон и периодическая система химических элементов Д.И.Менделеева в свете учения о строении атомов. (4 часа) 3 1 Структура ПСХЭ, периодический закон. Комбинир Структура ПСХЭ, ованные периодический закон. уроки Учащиеся должны знать: строение электронных оболочек атомов химических П. 4 Дата по плану 4 2 Строение электронных оболочек атомов элементов малых периодов. Комбинир Строение электронных ованные оболочек атомов элементов уроки малых периодов. 5 3 Валентность и валентные возможности атомов. 6 4 Изменение свойств соединений химических элементов в периодах и группах. Уроки комплекс ного применен ия ЗУНов Тема 3. Строение вещества. (8 часов) 7 1 Основные виды химической связи 8 2 Пространственное строение молекул неорганических и органических соединений 9 3 Типы кристаллических решеток и свойства веществ 10 4 Причины разнообразия веществ 11 5 Дисперсные системы 12 6 Подготовка растворов с заданной молярной концентрацией Практическая работа № 1 Уроки комплекс ного применен ия ЗУНов Валентность и валентные возможности атомов. Изменение свойств соединений химических элементов в периодах и группах. Основные виды химической связи. Пространственное строение молекул неорганических и органических соединений. Типы кристаллических решеток и свойства веществ. Причины разнообразия веществ. Массовая доля. Комбинир Концентрация раствора. Дисперсные системы ованные уроки П/Р №1 практику м элементов, положение данных элементов в таблице, определение валентности, валентные возможности различных атомов; состав, строение, свойства оксидов, гидроксидов, водородных соединений элементов. П. 5 П. 6 Учащиеся должны уметь: П. 7 характеризовать s-, p-, d-, fэлектроны и соответствующие подуровни, давать характеристику элементу по плану, доказывать двойственное положение водорода в периодической системе, определять местоположение лантаноидов и актиноидов. Учащиеся должны знать: определение химической связи, виды связей, механизмы их образования, различные формы молекул Учащиеся должны уметь: доказывать зависимость этих характеристик от различных факторов (прочность, насыщаемость и др.), определять тип кристаллической решетки. П. 8 П. 9 П. 10 П. 11 П. 12 ПОУ по темам 1-3 Контрольная работа № 1 по темам 1-3 Глава 4. Химические реакции (15 часов) 15 1 Классификация химических реакций 13 14 7 8 16 2 17 3 18 4 19 5 20 6 21 7 22 8 23 9 24 10 Скорость химической реакции. Катализ Влияние различных факторов на скорость хим. реакции. Практическая работа № 2 Химическое равновесие и условия его смещения. Производство серной кислоты контактным способом. Электролиты и неэлектролиты. Электролитическая диссоциация Сильные и слабые электролиты. Степень и константа диссоциации Реакции ионного обмена Гидролиз органических и неорганических соединений Окислительновостановительные реакции, их классификация К/Р №1 П/Р №2 ПОУ Контроль ный Уроки комплекс ного применен ия ЗУНов Классификация химических реакций Лекция Скорость химической реакции. Катализ практику м Лекция Химическое равновесие и условия его смещения. Лекция Уроки комплекс ного применен ия ЗУНов Электролиты и неэлектролиты. Электролитическая диссоциация Лекция Сильные и слабые электролиты. Степень и константа диссоциации Реакции ионного обмена Уроки комплекс ного применен ия ЗУНов Лекция Гидролиз органических и неорганических соединений Окислительновостановительные реакции, их классификация Учащиеся должны знать: сущность химической реакции, признаки классификации химических реакций понятие скорости химической реакции, сущность и механизм катализа, применение катализатора и ингибитора на практике; условия протекания реакций ионного обмена. П. 13 Учащиеся должны уметь: классифицировать предложенные реакции, самим приводить примеры на разные типы реакций, объяснять механизм реакций на примере органических и неорганических веществ, объяснять действие каждого фактора, влияющего на скорость реакции на примерах; записывать уравнения гидролиза и реакций ионного обмена. П. 16 П. 14 П. 15 П. 17 П. 18 П. 19 П. 20 Лекция 25 11 Составление уравнений ОВР. Метод электронного баланса. Уроки комплекс ного применен ия ЗУНов Метод электронного баланса. карточ ки 26 27 28 29 12 13 14 15 Электронно-ионный метод. Направленность ОВР ПОУ по теме 4 Контрольная работа № 2 по теме 4 Лекция Лекция ПОУ контроль ный Электронно-ионный метод. Направленность ОВР Лекция Лекция Уроки комплекс ного применен ия ЗУНов Лекция Металлы, особенности строения атомов, положение в периодической системе, физические свойства. К/Р №2 Глава 5. Металлы (16 часов) 30 1 Металлы, особенности строения атомов, положение в периодической системе, физические свойства. 31 2 32 3 33 4 34 5 Общие способы получения металлов. Электролиз Общие способы получения металлов. Электролиз Коррозия металлов и ее предупреждение Обзор металлических элементов А-групп 35 6 Обзор металлических элементов Б-групп. 36 37 38 39 40 41 7 8 9 10 11 12 Медь Цинк Титан Хром Марганец Железо, никель, платина Общие способы получения металлов. Электролиз Лекция Лекция Уроки комплекс ного применен ия ЗУНов Уроки комплекс ного применен ия ЗУНов Лекция Лекция Лекция Лекция Лекция Лекция Коррозия металлов и ее предупреждение Учащиеся должны знать: понятие металлической связи и металлической кристаллической решетки, физические и химические свойства металлов; характеристику металлов главных и побочных подгрупп периодической системы; общие способы получения металлов в промышленности; определение коррозии, её виды, способы защиты от коррозии; понятие о сплавах их классификации, составе, свойства, применении. Учащиеся должны уметь: давать общую характеристику металлов, объяснять их физические свойства, доказывать химические свойства, записывать уравнения реакций в молекулярном и окислительновосстановительном виде; П. 21 П. 22 П. 22 П. 23 П. 24 П. 25 П. 26 П. 27 Лекция Лекция Лекция П. 28 42 43 44 12 13 14 Железо, никель, платина Сплавы металлов Оксиды и гидроксиды металлов 45 46 15 16 ПОУ по теме 5 Контрольная работа № 3 по теме 5 К/Р №3 Лекция Лекция Уроки комплекс ного применен ия ЗУНов ПОУ Контроль ный Сплавы металлов Оксиды и гидроксиды металлов записывать химизм процесса коррозии, объяснять сущность химической и электрохимической коррозии. П. 28 П. 29 П. 30 Учащиеся должны знать: состав, строение, свойства и применение простых веществ неметаллов, их оксидов, летучих водородных соединений неметаллов Учащиеся должны уметь: определять вид химической связи, тип кристаллической решетки в простых веществах неметаллах и их соединениях, записывать уравнения реакций в молекулярном, ионном и окислительновосстановительном виде; объяснять изменение кислотно-основных свойств водородных соединений и оксидов неметаллов по периодам и группам; решать качественные и расчетные задачи по данной теме, распознавать вещества по качественным реакциям, правильно проводить опыты, соблюдая правила по П. 30 П. 30 Глава 6. Неметаллы (8 часов) 47 48 1 2 Обзор неметаллов Обзор неметаллов 49 3 Оксиды неметаллов и кислородосодержащие кислоты 50 4 Оксиды неметаллов и кислородосодержащие кислоты 51 5 Водородные соединения неметаллов 52 6 Генетическая связь неорганических и органических веществ Уроки комплекс ного применен ия ЗУНов Уроки комплекс ного применен ия ЗУНов Уроки комплекс ного применен ия ЗУНов Уроки комплекс ного применен ия ЗУНов Уроки комплекс ного применен ия ЗУНов Оксиды неметаллов и кислородосодержащие кислоты Водородные соединения неметаллов Генетическая связь неорганических и органических веществ П. 31 П. 31 П. 32 П. 33, 34 технике безопасности. 53 54 7 8 ПОУ по теме 6 Контрольная работа № 4 по теме 6 К/Р №4 ПОУ Контроль ный Глава 7. Химический практикум (4 часа) Решение экспериментальных задач по неорганической химии. Практическая работа № 3 56 2 Решение экспериментальных задач по органической химии. Практическая работа № 4 57 3 Решение практических расчетных задач Практическая работа № 5 58 4 Получение, собирание и распознание газов. Практическая работа № 6 Тема 7. Химия и жизнь. (3 часа) 59 1 Бытовая химическая грамотность. 60 2 Химическое загрязнение окружающей среды. П/Р №3 практику м П/Р №4 практику м П/Р №5 практику м П/Р №6 практику м Итоговая контрольная работа К/Р №5 55 61 1 3 62-68 РЕЗЕРВНЫЕ УРОКИ Учащийся должен уметь обращаться с лабораторным оборудованием и посудой, реагентами. Должен знать правила техники безопасности при работе в химической лаборатории Бытовая химическая грамотность. Виды химического загрязнения окружающей среды. контроль ный Учащиеся должны знать: правила выбора продуктов питания, правильное использование средств бытовой химии, лекарственных препаратов, о последствиях загрязнения окружающей среды и способах ее защиты. П. 35 П. 35