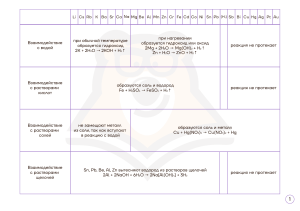
Качественные реакции для определения катионов и анионов электролитов (кислот, солей... Определяемый
advertisement
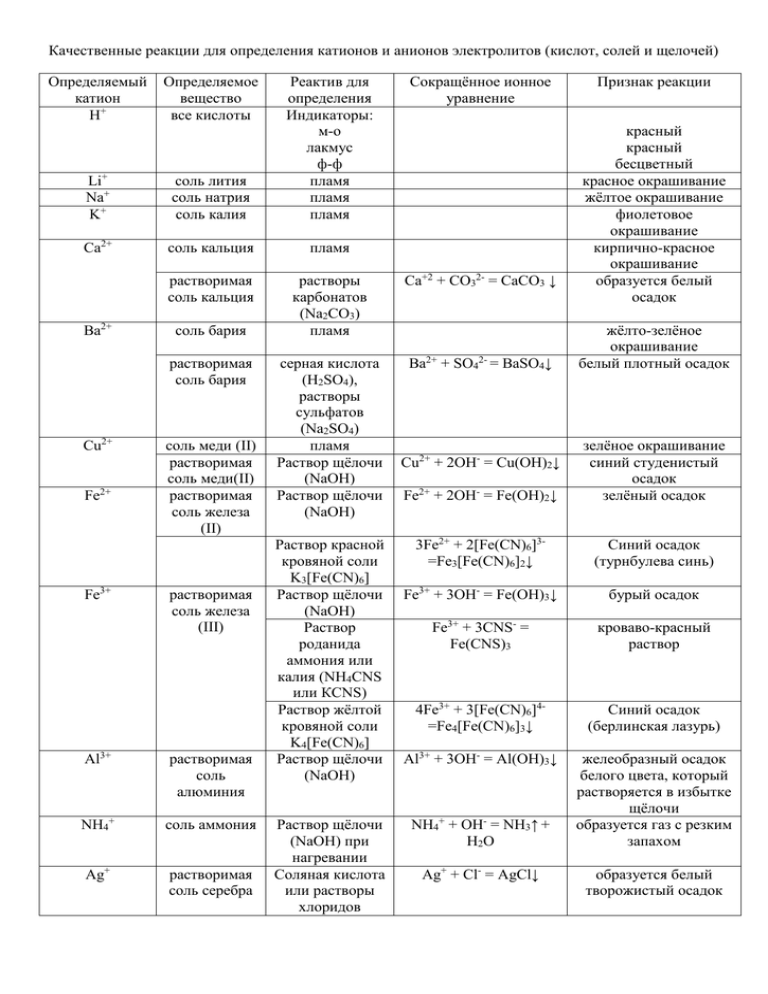
Качественные реакции для определения катионов и анионов электролитов (кислот, солей и щелочей) Определяемый катион Н+ Li+ Na+ K+ соль лития соль натрия соль калия Реактив для определения Индикаторы: м-о лакмус ф-ф пламя пламя пламя Ca2+ соль кальция пламя растворимая соль кальция растворы карбонатов (Na2CO3) пламя Ca+2 + CO32- = CaCO3 ↓ серная кислота (H2SO4), растворы сульфатов (Na2SO4) пламя Раствор щёлочи (NaOH) Раствор щёлочи (NaOH) Ba2+ + SO42- = BaSO4↓ Ba2+ Определяемое вещество все кислоты соль бария растворимая соль бария Cu2+ Fe2+ Fe3+ соль меди (II) растворимая соль меди(II) растворимая соль железа (II) растворимая соль железа (III) Al3+ растворимая соль алюминия NH4+ соль аммония Ag+ растворимая соль серебра Раствор красной кровяной соли K3[Fe(CN)6] Раствор щёлочи (NaOH) Раствор роданида аммония или калия (NH4CNS или КСNS) Раствор жёлтой кровяной соли K4[Fe(CN)6] Раствор щёлочи (NaOH) Раствор щёлочи (NaOH) при нагревании Соляная кислота или растворы хлоридов Сокращённое ионное уравнение Признак реакции красный красный бесцветный красное окрашивание жёлтое окрашивание фиолетовое окрашивание кирпично-красное окрашивание образуется белый осадок жёлто-зелёное окрашивание белый плотный осадок Fe2+ + 2OH- = Fe(OH)2↓ зелёное окрашивание синий студенистый осадок зелёный осадок 3Fe2+ + 2[Fe(CN)6]3=Fe3[Fe(CN)6]2↓ Синий осадок (турнбулева синь) Fe3+ + 3OH- = Fe(OH)3↓ бурый осадок Fe3+ + 3CNS- = Fe(CNS)3 кроваво-красный раствор 4Fe3+ + 3[Fe(CN)6]4=Fe4[Fe(CN)6]3↓ Синий осадок (берлинская лазурь) Al3+ + 3OH- = Al(OH)3↓ желеобразный осадок белого цвета, который растворяется в избытке щёлочи образуется газ с резким запахом Cu2+ + 2OH- = Cu(OH)2↓ NH4+ + ОН- = NH3↑ + Н2О Ag+ + Cl- = AgCl↓ образуется белый творожистый осадок Определяемый анион OH- Определяемое вещество щёлочи Реактив для определения индикаторы: фенолфталеин м-о лакмус раствор нитрата серебра (AgNO3) Сокращённое ионное уравнение SO42- + Ba2+ = BaSO4↓ малиновый жёлтый синий образуется белый творожистый осадок образуется желтоватый творожистый осадок образуется жёлтый творожистый осадок образуется газ с неприятным запахом образуется чёрный осадок белый осадок Cu + NO3- + 2Н+ = Cu2+ + NO2↑ + H2O образуется бурый газ 3Ag+ + PO43- = Ag3PO4 ↓ образуется жёлтый осадок образуется жёлтый осадок образуется бесцветный газ без запаха образуется газ с резким запахом Cl- соляная кислота и хлориды Br- бромоводородная кислота и бромиды раствор нитрата серебра (AgNO3) Ag+ + Br- = AgBr↓ I- йодоводородная кислота и йодиды раствор нитрата серебра (AgNO3) Ag+ + I- = AgI↓ S2- сульфиды Сильные кислоты (HCl, HNO3, H2SO4) растворимые соли меди (II) растворимые соли бария медь (Cu) и концентрированная серная кислота для определения азотной кислоты используется только медь раствор нитрата серебра (AgNO3) растворимые соли бария Сильные кислоты (HCl, HNO3, H2SO4) Сильные кислоты (HCl, HNO3, H2SO4) S2- + 2H+ = H2S↑ SO42- сульфаты NO3- нитраты PO43- ортофосфаты CrO42- хроматы CO32- карбонаты SO32- сульфиты Признак реакции Ag+ + Cl- = AgCl↓ S2- + Cu2+ = CuS↓ Ba2+ + CrO42- = BaCrO4 ↓ CO32- + 2Н+ = СO2↑ + H2O SO32- + 2Н+ = SO2↑ + H2O