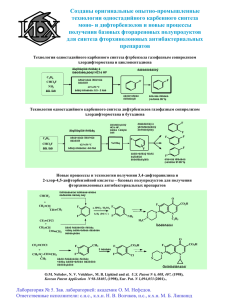
(дикарбоновые кислоты, трикарбоно- вые кислоты
advertisement

№ 13. * Поли- и гетерофункциональные соединения, участвующие в процессах жизнедеятельности Полифункциона- Гетерофункциональные соединения льные соединения Полиолы: гликоли, глицерины, тетриты, пентиты, гекситы Полиамины Поликарбоновые кислоты (дикарбоновые кислоты, трикарбоновые кислоты) Аминоспирты Аминокислоты Оксикислоты Альдегидокислоты Кетокислоты Гетероциклические соединения (азотсодержащие гетероциклы, гетероциклы с разными гетероатомами) *Особенности химического поведения полифункциональных соединений 1. Кислотно-основные свойства полифункциональных соединений Кислотные свойства спиртов C2H5OH → H+ + C2H5O– этанол Вицинальные (от лат. vicinus соседний) диолы (гликоли) - этиленгликоль CH2 CH2 OH O H Антифриз H + CH2 CH2 CH2 CH2 OH O O HO . *Кислотность полиолов Полиолы алифатического ряда СН2ОНСНОНСН2ОН НОСН2СН2ОН СН3СН2ОН рКа 13,3 15,1 18 Кислотность полиолов растёт в ряду спирты < гликоли < глицерины снизу вверх. * Макрогетероциклические полиэфиры – краун-эфиры содержат в своих циклах более 11 атомов, из которых не менее четырёх — гетероатомы, которые связаны между собой этиленовыми мостиками. образуют устойчивые липофильные комплексы с катионами металлов, перспективные комплексообразователи, ловушки катионов, облегчают транспорт ионов через клеточные мембраны *Глицерин слезоточивое действие 1% в этаноле – сосудорасширяющее средство Кислотные свойства фенолов уменьшаются по мере увеличения числа гидроксильных групп. — OH + H2O H3O+ + — O- : феноксид-анион группа -ОН (+М-эффект > -I-эффект!) Пирокатехин. орто-дигидроксибензол - катехол . Восстановитель. (проявитель, в производстве красителей и лекарственных веществ. Катехоламины (адреналин) * Катехоламины – биогенные амины, нейромедиаторы и гормоны *регуляция функций эндокринных желез (надпочечников, щитовидной железы) и передача нервных импульсов. * катехоламины * Гормо́ны •Гормоны служат гуморальными (переносимыми с кровью) регуляторами определённых процессов в различных органах и системах. адреналин *Нейромедиа́торы (нейротрансмиттеры, посредники) — биологически активные химические вещества, посредством которых осуществляется передача электрического импульса с нервной клетки через синаптическое пространство между нейронами. медиация нервных процессов норадреналин *Резорцин — мета-дигидроксибензол, применяется в производстве синтетических красителей; некоторых полимеров; в медицине- как обеззараживающее средство при лечении кожных заболеваний (дубящие свойства) *Гидрохинон пара-дигидроксибензол —легко окисляется Применяется в фотографии как проявитель, в синтезе органических красителей; как антиоксидант. * Система переноса электронов с помощью гидрид-ионов Система хинон гидрохинон. ацетон : енол 0,00025% 1,3-дикарбонильные соединения Кислотно-основные свойства дикарбоновых кислот O=C O H (CH2)n O=C OH O=C k1 O (CH2)n O=C OH O=C k2 O (CH2)n O=C O -I 1. k1 > k2 2. k1 тем больше, чем n меньше 3. k2 тем больше, чем n больше +I . 2. Циклизация полифункциональных соединений Циклизация диолов: а) внутримолекулярная дегидратация цикл. простой эфир б) межмолекулярная дегидратация цикл. простой эфир, токсичен Циклизация дикарбоновых кислот. С2 – С3 Щавелевая и малоновая кислоты – - декарбоксилирование 140-150o С НООС–СООН = НСООН + СО2 щавелевая кислота ( соли оксалаты) НООС–СН2–СООН = СН3–СООН + СО2 малоновая кислота * Янтарная и глутаровая кислоты циклодегидратацию С4 – С5 Соли - сукцинаты, янтарь - Кислоты с более длинной цепью циклизуются с одновременными дегидратацией и декарбоксилированием С6 – С7 δ AN 3. Хелатообразование хелаты, от греческого - клешня - процесс возникновения дополнительных нековалентных связей в тех структурах, в которых атом водорода (или металла), связанный ковалентной (или ионной) связью, ориентирован между двумя электронодонорными фрагментами одной и той же молекулы, предоставляющими этому атому водорода (или металла) дополнительное электронное облако. Комплексный глицерат меди: HO CH2 H2C OH Cu2+ + + HC OH HO CH H2C OH HO CH2 HO CH2 H2C OH HC O Cu2+ O CH HO CH2 . H2C OH * Гетерофункциональные соединения Гидроксикислоты 1. Кислотно-основные свойства гидроксикислот α RCH C=O OH OH +H H RCH C=O OH O . -I Гидроксикислоты диссоциируют сильнее соответствующих незамещённых кислот. Название Формула рКа Гликолевая HOCH2–COOH 3,82 Уксусная СН3–СООН 4,76 Молочная СН3–CH(OH)–COOH 3,85 Пропионовая СН3–CH2–COOH 4,87 Винная НООС–С(ОН)–СН(ОН)– СООН HOOC–CH2–CH2–COOH 2,96 Янтарная 5,64 *Молочная кислота Гидроксикислоты H H H HH C O C C H H H + C H C COOH H зигзагообразная конформация H H C H H O + OH C O клешевидная конформация Гидроксикислоты α-Гидроксикислоты O C O H OH CH3 CH + O H t O CH CH3 HO C O молочная кислота C O CH3 CH CH CH3 O C O лактид Межмолекулярная циклизация. сложноэфирные группы Гидроксикислоты β-Гидроксикислоты O CH3 CH OH CH C H H t -H2O CH3CH CHCOOH 2-бутеновая кислота 3-гидроксибутановая кислота внутримолекулярная дегидратация Гидроксикислоты γ- Гидроксикислоты + CH2 O t C H2C CH2 O O OH H -гидроксимасляная кислота -H2O CH2 C H2C Сложноэфирная группа O CH2 -бутиролактон внутримолекулярная этерификация δ- Гидроксикислоты CH2 CH2 CH2 Ñ=O CH2 OH OH - H2O CH2 CH2 Í àãðåâàí èå CH2 C=O CH2 O . Ëàêòî í внутримолекулярная этерификация ε-Гидроксикислоты и кислоты с более удалёнными ОН- группами HO–CH –(CH )n–COOH + HO–CH –(CH )n–COOH → HO–CH –(CH )n–(C=O)–O–CH –(CH )n– COOH 2 2 2 2 2 2 2 2 межмолекулярно сконденсированные линейные полиэфиры Хелатообразование KOOCCHCHCOONa HO OH + Cu(OH)2 HO OH KOOCCHCHCOONa Реактив Фелинга, который KOOCCHCHCOONa O OH 2+Cu HO O KOOCCHCHCOONa . образуется при смешивании калий, натриевой соли винной (2,3-дигидроксибутандиовой) кислоты с гидроокисью двухвалентной меди Гидроксикислоты Разложение -гидроксикислот H R α C OH O H2SO4 C R + H C H OH -гидроксикислота O O альдегид C OH муравьиная кислота