ИЗМЕНЕНИЕ АГРЕГАТНОГО СОСТОЯНИЯ ВЕЩЕСТВА.pps
advertisement

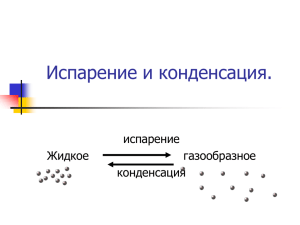
Изменение агрегатного состояния вещества Взаимные превращения газов, жидкостей и твердых тел Испарение – это парообразование, происходящее при любой температуре со свободной поверхности жидкости • Ф-10-А Испарение Парообразование • происходит с поглощением энергии. Энергия расходуется на разрыв межмолекулярных связей. • С поверхности жидкости вылетают молекулы, кинетическая энергия которых превышает потенциальную энергию взаимодействия молекул. • Папка: Простые научные эксперименты Конденсация • Конденсация – это переход вещества из газообразного в жидкое состояние. • Молекулы жидкости, покинувшие ее в процессе испарения, находятся в воздухе в состоянии непрерывного теплового движения. Так как движение молекул хаотичное, то какая-то часть молекул вновь попадает в жидкость. Ф-10-А Конденсация Удельная теплота парообразования Динамическое равновесие в системе жидкость-пар: • Число молекул, испаряющихся с поверхности жидкости в единицу времени, равно числу возвращающихся молекул конденсируемого пара. Насыщенный пар - •это пар, находящийся в динамическом равновесии со своей жидкостью. •Давление Рн насыщенного пара зависит только от температуры. Точка росы – •это температура, при которой водяной пар становится насыщенным. • Ф-10-А Насыщенный пар Ненасыщенный пар – •это пар, находящийся при давлении ниже давления насыщенного пара ( Р < Рн) Относительная влажность воздуха: • отношение давления Р водяного пара, содержащегося в воздухе при данной температуре, к давлению Рн насыщенного водяного пара при той же температуре, выраженное в процентах: Папка:Влажность воздуха. Измерение влажности. Кипение – •это процесс парообразования во всем объеме жидкости при определенной температуре Т (температуре кипения). • Ф-10-А Кипение Температура кипения– •это температура, при которой давление насыщенного пара в пузырьках внутри жидкости равно внешнему давлению. Критическая температура (Ткр ): •для каждого вещества (газообразного) существует критическая температура Ткр при которой исчезает разница между жидкостью и ее насыщенным паром. • Ф-10-А Зависимость давления от объёма Плавление – • это процесс перехода вещества из твердого состояния в жидкое при нагревании. • Удельная теплота плавления численно равна количеству теплоты, необходимому для превращения 1 кг твердого вещества в жидкость при неизменной температуре. • Ф-10-А Молекулярная картина теплообмена • Ф-10-В Плавление испарение Кристаллиза́ция • процесс перехода— вещества из жидкого состояния в твёрдое с образованием кристаллов. • Кристаллизация начинается при достижении некоторого предельного условия, например, переохлаждения жидкости или пересыщения пара, когда практически мгновенно возникает множество мелких кристалликов — центров кристаллизации. • Кристаллики растут,присоединяя атомы или молекулы из жидкости или пара. • Зависимость скорости роста от условий кристаллизации приводит к разнообразию форм роста и структуры кристаллов • Папка: Кристаллизация пересыщенного раствора Сублима́ция — • переход вещества из твёрдого состояния сразу в газообразное, минуя жидкое. • Обратным процессом является десублимация. Примером десублимации являются такие атмосферные явления, как иней на поверхности земли и изморозь на ветвях деревьев и проводах. • Папка: Физические явления Сублимация йода Изменение внутренней энергии и количества теплоты ПРОЦЕСС КОЛИЧЕСТВО ТЕПЛОТЫ ВНУТРЕННЯЯ ЭНЕРГИЯ Нагревание тела Q = c m ( t- t), где с удельная теплоемкость Увеличивается Охлаждение тела Q = c m ( t- t) Уменьшается Парообразование Q = r m, где r удельная теплота парообразования Увеличивается Конденсация Q= -rm Уменьшается Плавление Q = λ m, где λ удельная теплота плавления Увеличивается Кристаллизация Q= -λm Уменьшается • Папка: 16 Изменение агрегатных состояний вещества