Молекулярная физика. Тепловые явления. Уравнение состояния
advertisement

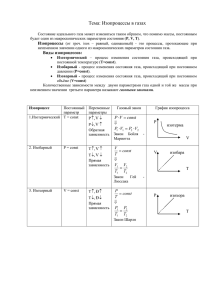
Тема: Изопроцессы в газах. Газовые законы. Цель урока: • сформировать понятие «изопроцесс»; • изучить газовые законы. Процесс, протекающий при неизменном значении одного из параметров, называют изопроцессом. Постоянная величина T = const p = const V = const Название процесса Изотермический процесс Изобарный процесс Изохорный процесс Процесс Изотерми ческий Постоянная величина m=const Т = const m=const Изобарный P = const m=const Изохорный V = const Определе ние Закон Формулировка Графики Какая величина сохраняется? Название изопроцесса? Как изменяются остальные величины? Изотермический процесс – процесс изменения состояния газа, происходящий при постоянной температуре. Для газа данной массы произведение давления газа на его объем постоянно, если температура газа не меняется. pV = const (закон Бойля-Мариотта) Р. Бойль 1662 г. р, Па р, Па Т2 изотермы Т2 > Т1 Т1 0 Э. Мариотт 1676 г. 0 Т, К V, м³ V, м³ 0 Т, К Постоянная величина Определение Изотерми ческий Т = const Процесс изменения состояния газа, происходящий при постоянной температуре. Изобарный P = const Изохорный V = const Процесс Закон Формулировка pV = const закон Бойля – Мариотта Для газа данной массы произведение давления газа на его объем постоянны, если температура газа не меняется . Графики p0 p0 p1<p0 p0 p1 p0 p1 вдох p0 p2>p0 p0 p2 выдох p2 Какая величина сохраняется? Название изопроцесса? Как изменяются остальные величины? Изобарный процесс процесс изменения состояния газа, происходящий при постоянном давлении. pV pV Из уравнения Клапейрона T1 1 T2 2 const следует: 1 2 Для газа данной массы отношение объема газа к температуре постоянно, если давление газа не меняется. p = const, V/T = const (закон Гей-Люссака) р, Па V, м³ р2 изобары 0 р1 р 2 < р 1 Ж. Гей-Люссак 1802 г. 0 Т, К р, Па Т, К 0 V, м³ Постоянная величина Определение Т = const Процесс изменения состояния газа, происходящий при постоянной температуре. Изобарный P = const Процесс изменения состояния газа, происходящий при постоянном давлении Изохорный V = const Процесс Изотерми ческий Закон Формулировка pV = const закон Бойля – Мариотта Для газа данной массы произведение давления газа на его объем постоянны, если температура газа не меняется . V/Т = const закон ГейЛюссака Для газа данной массы отношение объема газа к температуре постоянно, если давление газа не меняется. Графики Какая величина сохраняется? Название изопроцесса? Как изменяются остальные величины? Изохорный процесс процесс изменения состояния газа, происходящий при постоянном объеме. Из уравнения Клапейрона p1V1 p2V2 const T1 T2 следует: Для газа данной массы отношение давления газа к температуре постоянно, если объем газа не меняется. V = const, p/T = const (закон Шарля) р, Па P, Па V2 Изохоры 0 V, м³ V1 V2 < V1 Ж. Шарль 1787 г. V, м³ 0 Т, К 0 Т, К Процесс Изотерми ческий Изобарный Изохорный Постоянная величина Определение Т = const Процесс изменения состояния газа, происходящий при постоянной температуре. P = const Процесс изменения состояния газа, происходящий при постоянном давлении. V = const Процесс изменения состояния газа, происходящий при постоянном объеме. Закон Формулировка pV = const закон Бойля – Мариотта Для газа данной массы произведение давления газа на его объем постоянны, если температура газа не меняется . V/Т = const закон ГейЛюссака Для газа данной массы отношение объема газа к температуре постоянно, если давление газа не меняется. p/Т = const закон Шарля Для газа данной массы отношение давления газа к температуре постоянно, если объем газа не меняется. Графики Газовый термометр Задача: 2. Найти во всех системах координат : а) изотермы; б) изобары; в) изохоры Ответы: а) 2; б)1; в) 3 а)1 б)2 в)3 а)2 б)3 в)1 Задача: 3. На рисунке представлен замкнутый цикл изменения состояния газовой системы. Вычертить эту диаграмму в координатах pV и VT. ОБОБЩЕНИЕ T = const P1V1 = P2V2 T1 T2 V = const P = const P1V1 = P2V2 V1 T1 = V2 T2 P1 T1 = P2 T2 Презентацию выполнила преподаватель физики ГБОУ СПО АКТТ Полетаева Г.В.