Презентация "Железо и его свойства"
advertisement

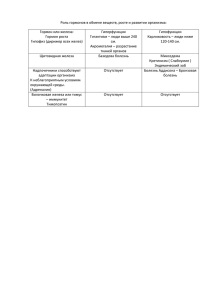
Железо: строение атома, физические и химические свойства. Генетические ряды железа (II) и железа (III). Павлова Галина Григорьевна учитель химии, МС(к)ОУ «С(к)ОШ № 24» г. Магнитогорск, Челябинская область. 2010 Положение элемента – железа в периодической системе Д.И. Менделеева. ►Порядковый номер ►Период ►Группа ►Подгруппа ►26 ►Четвертый ►II ►Побочная Строение атома железа Допишите электронную формулу 2 2 6 2 1s 2s 2р 3s 6 3р …. 1s2 2s2 2р6 3s2 3р6 3d6 4s2 Какие электроны для элементов главных подгрупп являются валентными? А какие электроны для элементов побочных подгрупп являются валентными? Запомни! Особенностью электронного строения элементов побочных подгрупп является заполнение электронами не последнего, а предпоследнего уровня. Запомните! Валентные электроны атомов элементов побочных подгрупп распределяются на последнем и предпоследнем уровнях. Для железа характерны две основные степени окисления: +2, +3. 0 +2 Fe –2e = Fe 0 +3 Fe –3e = Fe Физические свойства железа: Цвет Блеск Пластичность Серебристо-белый Блестящий Очень пластичный, легко куется, прокатывается, штампуется Магнитные свойства Намагничивается и размагничивается 15390С Температура плавления Твердость Твердый Железо – металл серого цвета Способность притягиваться к магниту – особое свойство железа и его сплавов. Fe +2 +3 +2, +3 S, Cu2+, p.HCI, p.H2 SO4 CI2, HNO3 O 2, H 2O Закончить уравнения химических реакций: Fe + CI2 = Fe + S = Fe + HCI = Fe + O2 = Fe + CuSO4 = Fe + H2O = Fe + O2 + H2O = Химические свойства железа Взаимодействие с простыми веществами -неметаллами 1) С кислородом. 0 0 +2, +3 -2 3Fe + 2O2 —>Fe3O4 +2 -2 +3 -2 (FeO • Fe2O3 ) Химические свойства железа Взаимодействие с простыми веществами - неметаллами. 2) С серой и хлором. Запишите уравнение реакции и составьте электронный баланс. 0 0 +2 -2 +3 -1 Fe + S —>FeS электронный баланс 2Fe0 + 3Cl20 —> 2FeCl3 электронный баланс Fe0 – 2e- —> Fe2+ S0 + 2e- —> S2- Fe0 – 3e- —> Fe3+ Cl20 +2e- —> 2Cl1- Химические свойства железа Взаимодействие со сложными веществами 1) С водой. +2, +3 3Fe0 + 4H2O —> Fe3O4 + 4H20 при t =7000 - 9000 Химические свойства железа 2) С кислотами. ОПЫТ: осуществите реакцию между порошком железа и соляной кислотой. В каком случае возможны реакции между металлом и кислотой? Составить уравнение реакции. Сделать вывод. Fe + 2HCl —>FeCl2 + H2 Металлы взаимодействуют с кислотами если: 1. Металл находится в ряду активности металлов до водорода. 2. Должна получиться растворимая соль. 3. Реакция характерна для растворов кислот. 4. Металл + кислота → соль + водород Химические свойства железа 3) С солями. ОПЫТ: осуществите реакцию между порошком железа и раствором хлорида меди (II). В каком случае возможны реакции между металлом и растворами солей? Составить уравнение реакции. Сделать вывод. Fe + CuCl2 —> FeCl2 + Cu Металлы взаимодействуют с растворами солей если: 1. Каждый металл вытесняет из растворов солей все другие металлы, расположенные правее его в ряду напряжений. 2. Обе соли (и реагирующая, и образующая в результате реакции) должны быть растворимыми. Соединения железа: Fe3O4 – магнитный железняк Fe2O3 – красный железняк (гематит) 2Fe2O3 FeS2 * 3H2O – бурый железняк – железный колчедан Генетические ряды железа (II) и железа (III). Задание: 1) 3) запишите формулы оксида железа (II) и оксида железа (III); 2) составьте соответствующие им формулы гидроксидов; отметьте характер этих соединений. Степень окисления металла в оксиде должна соответствовать степени окисления металла в соответствующем гидроксиде +2 +2 FeO —>Fe(OH)2 Данный оксид носит основный характер. Какие реакции подтверждают основный характер оксидов? +3 +3 Fe2O3 —> Fe(OH)3 Какие соединения называются амфотерными? Какие из реакций соответствуют схеме Fe+2 =>Fe+3 ? 1) 2) 3) 2FeCI2 + CI2 = 2FeCI3 FeCI3 + 3NaOH = Fe(OH)3 + 3NaCI 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3 Качественные реакции на ионы железа Fe2+ и Fe3+ На ионы Fe2+ +2 +3 +2 FeCl2 + K3[Fe(CN)6] —> KFe[Fe(CN)6]+2KCL красная кровяная соль синий осадок ----------------------------------------------------------------------------------------------------------- На ионы Fe3+ +3 +3 +2 FeCl3 + K4[Fe(CN)6] —> KFe[Fe(CN)6]+3KCL желтая кровяная соль +3 синий осадок +3 FeCl3 + KCNS —> Fe(CNS)3 + 3KCl роданид калия раствор красного цвета Лабораторный опыт Осуществите практически цепочки химических превращений. Составьте уравнения реакций. Вариант 1: Fe —> FeCl2 —> Fe(OH)2 —> FeO Вариант 2: Fe —> FeCl3 —> Fe(OH)3 —> Fe2O3 Горение железа в хлоре с образованием хлорида железа (III)