ЛС для инфекционно-воспалительных заболеваний
advertisement

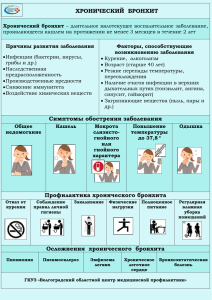
Министерство образования и науки РФ Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования Новгородский Государственный Университет имени Ярослава Мудрого (НовГУ) __________________________________________________ Кафедра внутренних болезней, неврологии и психиатрии Методическая разработка по клинической фармакологии для преподавателей и студентов IV курса специальность 060108.65 "Фармация" Тема: Клинико-фармакологические подходы к выбору групп и конкретных лекарственных средств для фармакотерапии инфекционновоспалительных заболеваний (пневмоний, бронхита, абсцесса, септических заболеваний, пиелонефрита). Составитель: к.м.н., доцент Яковлева О.А. _____________________ Принята на заседании кафедры зав. кафедрой проф. Вебер В.Р. _____________________ «_____»_______2011 г. Великий Новгород 2011 год 1. Цель занятия Для преподавателя: сформировать навыки и умения по теме «Клинико-фармакологические подходы к выбору групп и конкретных лекарственных средств для фармакотерапии инфекционно-воспалительных заболеваний (пневмоний, бронхита, абсцесса, септических заболеваний, пиелонефрита)» необходимые провизору в профессиональной деятельности. Для студента: ИЗУЧИТЬ клинические синдромы проявлений инфекционно-воспалительного поражения легких и бронхов, септических процессов, пиелонефрита; ОСВОИТЬ умения и навыки, необходимые провизору для участия в проведении (врачом) индивидуализированной фармакотерапии больным с инфекционно-воспалительными поражениями - содействия в рациональном выборе и применении антимикробных лекарственных средств (ЛС); ОЗНАКОМИТЬСЯ с методами контроля за эффективностью и безопасностью используемых в клинической практике антимикробных лекарственных препаратов (ЛП). 2. Основные вопросы темы 2.1. Клиническая характеристика синдрома пневмонии - инфекционного заболевания, характеризующегося экссудативным воспалительным процессом паренхимы и межуточной ткани легких, с накоплением экссудата в просвете альвеол: классификация пневмоний; этиология, факторы риска и патогенез пневмоний; основные клинические проявления; сравнительная характеристика течения крупозной и очаговой пневмонии; отличительные особенности отдельных пневмоний в зависимости от их этиологии; осложнения пневмоний; критерии тяжести пневмоний; рациональная фармакотерапия пневмоний (включая осложнение абсцессом). 2.2. Выбор ЛП при внебольничных и внутрибольничных пневмониях; показания к комбинированной терапии антибактериальными ЛП и длительности лечения пневмонии; рациональная фармакотерапия абсцесса легких. 2.3. Клиническая характеристика синдрома бронхита - заболевания, характеризующегося инфекционного-воспалительным диффузным поражением бронхиального дерева с дискринией и протекающее остро циклически, либо хронически с обострениями и ремиссиями: классификация бронхита; этиология и патогенез бронхита, клинические типы хр. бронхита; клиническая картина бронхита (без обструкции); выбор ЛП для лечения необструктивного бронхита: поствирусного бронхита, обострения хр. простого и гнойного бронхита. 2.4. Клиническая характеристика синдрома сепсиса - системного инфекционного заболевания с различной локализацией первичного очага или источника инфекции: этиология и структура возбудителей у разных групп больных; принципы антибиотикотерапии сепсиса; эмпирическая моно- и комбинированная терапия сепсиса. 2.5. Клиническая характеристика пиелонефрита - неспецифического инфекционно-воспалительного поражения почечной паренхимы: классификация пиелонефрита; этиология и патогенез пиелонефрита; клиническая картина острого пиелонефрита (обострения хр. пиелонефрита); рациональная фармакотерапия острого и хронического пиелонефрита; противорецидивное лечение пиелонефрита. 3. Вопросы контроля исходного уровня Фармакокинетика, фармакодинамика, взаимодействие и побочные действия: 3.1. "Старых" макролидов: Эритромицина, Олеандомицина и др. 3.2. "Новых" макролидов: Спирамицин, Рокситромицин, Кларитромицин, Азитромицин и др. 3.3. "Старых" и "Новых - респираторных" фторхинолонов: Норфлоксацина, Пефлоксацина, Эноксацина, Офолоксацина, Ципрофлоксацина; Левофлоксацина, Моксифлоксацина и др. 3.4. Традиционных и "Защищенных" аминопенопенициллинов: Амоксициллина и Ампициллина; Коамоксиклава, Сультамициллина (Ампициллина/сульбактама) и др. 3.5. Других "Защищенных" пенициллинов: Тикарциллин/Клавулановая кислота, Пиперациллин/Тазобактам и др. 3.6. Пероральных цефалоспоринов 2-3 поколений: Цефаклора, Цефуроксима, Цефтибутена, Цефподоксима и др. 3.7. Тетрациклинов: Доксициклина. 2 3.8. Парентеральных цефалоспоринов II-III-поколений: Цефуроксима, Цефотаксима, Цефтриаксона, Цефтазидима, Цефомандола, Цефокситина и др. 3.9. Аминогликозидов II-III-поколений: Гентамицина, Тобрамицина, Амикацина, Нетилмицина и др. 3.10. Цефалоспоринов IV-поколения: Цефепима, Цефпирома и др. 3.11. Карбапенемов (Имипенема, Меропенема) и Линкосамидов (Клиндамицина). 3.12. ЛС лечения абсцедирующей пневмонии (в большинстве случаев обусловленной ассоциацией анаэробов и золотистого стафилококка): Метронидазола, Оксациллина, парентеральными цефалоспоринами I-поколения (Цефазолина, Цефалотина), Гликопептидов (Ванкомицина, Тейкопланина), Хлорамфеникола, Рифампицина и др. 3.13. Антибаткриальных ЛП, используемых в терапии инфекционно-воспалительных поражений почечной паренхимы: Сульфаниламидов, Аминопенициллинов, Цефалоспоринов, Тетрациклинов, Хинолонов и Фторхинолонов, Оксихинолонов, Нитрофуранов, Аминогликозидов и др. 4. Блок дополнительной информации Антибактериальная терапия инфекций верхних дыхательных путей Основными бактериальными возбудителями острых инфекций верхних дыхательных путей (ВДП) являются пневмококк (Streptococcus pneumoniae) и гемофильная палочка (Haemophilus influenzae). Гораздо реже выделяют моракселлу (M. catarrhalis), b-гемолитический стрептококк группы А (БГСА, S.pyogenes). Неясно значение вирусов, которые при специальных исследованиях как единственный возбудитель выделяют в 6% случаев. В последнее время появились первые сообщения о выделении Chlamydia pneumoniae. Однако основное значение имеют S.pneumoniae и H.influenzae. Основными вирусными возбудителями являются риновирусы (25-40% всех вирусов), коронавирусы, вирусы гриппа и парагриппа. Реже встречаются респираторно-синцитиальный вирус, аденовирусы, энтеровирусы, реовирусы и пикорнавирусы. Специфической терапии против вирусных инфекций верхних отделов дыхательных путей не имеется. Исключение составляет грипп типа А, при котором эффективно раннее назначение ремантадина. В нескольких исследованиях было показано профилактическое действие интерферона (ИФН) против риновирусной инфекции. Лейкоцитарный g-ИФН применяли интраназально в течение 45 дней. Однако при инфекциях, вызванных другими вирусами (грипп, парагрипп, коронавирусы) или Mycoplasma pneumoniae, защитное действие ИФН не проявлялось. При развитии симптомов риновирусной инфекции применение ИФН не оказывало влияния на ее течение. Кроме того, при длительном применении ИФН отмечалось раздражение слизистой оболочки носа (образование сухих корок, кровотечение). В связи с ограниченным спектром активности, склонностью вирусных инфекций к самоизлечению, а также с учетом стоимости терапии применение ИФН не получило широкого распространения. Эффективность таких популярных препаратов, как оксолиновая мазь, арбидол, многочисленных иммуномодуляторов, не доказана в рандомизированных сравнительных испытаниях. В целом можно согласиться с утверждением видного американского инфекциониста J. Barlett, который недавно написал: "Нет противовирусных препаратов, эффективность которых при лечении пациентов с инфекциями верхних отделов дыхательных путей была бы установлена". Таким образом, основу лечения вирусных инфекций составляют симптоматическая терапия и vis medicamentrics naturae (излечивающая сила природы — лат.). В основе антибактериальной терапии ВДП лежит эмпирический выбор. Однако при этом надо помнить, что эмпирическая терапия должна базироваться на сведениях, полученных в проспективных исследованиях. Планируя эмпирическую антибиотикотерапию, врач должен задать себе четыре главных вопроса. Какой наиболее вероятный возбудитель мог вызвать это заболевание? 3 Эффективность каких антибиотиков доказана в рандомизированных клинических исследованиях? Какова наиболее вероятная чувствительность предполагаемого возбудителя к этим антибиотикам? Какие имеются локальные данные о его чувствительности? Наиболее трудным вопросом является последний, так как в большинстве поликлиник и стационаров нет достоверных данных о чувствительности истинных возбудителей (а не контаминирующей микрофлоры !) к современным антибиотикам. Поэтому мы приведем общие сведения о чувствительности наиболее вероятных возбудителей инфекций ВДП. Пневмококк. Во всем мире наиболее существенной проблемой последних лет является быстрый рост устойчивости к пенициллину в сочетании с устойчивостью к макролидным антибиотикам, тетрациклинам, ко-тримоксазолу, оральным цефалоспоринам и иногда даже к парентеральным цефалоспоринам III поколения (цефотаксим, цефтриаксон). Различают пневмококки с промежуточной чувствительностью и резистентные. При лечении инфекций, вызванных штаммами с промежуточной чувствительностью, эффективны высокие дозы бензилпенициллина, цефалоспорины III (цефотаксим, цефтриаксон) и IV (цефепим, цефпиром) поколения, а также клиндамицин. Из оральных пенициллинов лучшим является амоксициллин, из оральных цефалоспоринов - цефуроксим аксетил. При резистентности пневмококков к bлактамным антибиотикам применяют ванкомицин, рифампицин. Перспективными препаратами являются хинолоны III поколения (грепафлоксацин, тровафлоксацин и др.), хинупристин/дальфопристин, оксазалидиноны (линезолид). Гемофильная палочка. Для многих данный возбудитель представляется чем-то экзотическим, поскольку в большинстве микробиологических лабораторий его не выделяют. А в том случае, если это удается сделать, то результаты определения чувствительности очень часто вызывают большие сомнения. Так, из отечественных лабораторий поступают сообщения не просто о резистентности, а о высокой резистентности к цефалоспоринам III поколения. В мировой литературе такой феномен не описан. Причина ошибок заключается в высокой требовательности гемофильной палочки к агару и условиям инкубирования. Поэтому для получения достоверных данных и их воспроизводимости во всем мире принято пользоваться рекомендациями Национального комитета по клиническим лабораторным стандартам США (NCCLS). Как показано в нашей лаборатории, для определения чувствительности гемофильной палочки нельзя использовать отечественную среду АГВ. Дозы антибиотиков при амбулаторных инфекциях ВДП Антибиотик Доза для Разовая доза Кратность, детей,(мг/кг/ в для взрослых, раз/сут; сутки); мг; Ампициллин 40-50 500 4 Амоксициллин 40 500 3 Амоксициллин/клавуланат 40 625 3 Цефаклор 40 500 3 Цефуроксим 30 250-500 2 Цефтибутен 9 400 1 Цефтриаксон 50 1000 1 Азитромицин 10 500 1 Кларитромицин 15 250 2 Рокситромицин 5-8 150 2 Спирамицин 150 000 МЕ 3 000 000 МЕ 2 Курс, сут; 10 10 10 10 10 10 10 3 10 10 10 4 Мидекамицин Ципрофлоксацин Офлоксацин Ко-тримоксазол 30-50 Противопоказан Противопоказан 8 400 500 400 960 3 2 2 2 10 7-10 7-10 10 Ошибки антибактериальной терапии инфекций ВДП можно разделить на три группы. 1. Пренебрежение приемом антибиотиков внутрь. Антибиотики важны с двух точек зрения. Во-первых, они позволяют облегчить состояние пациента, ускорить выздоровление и предотвратить хронизацию инфекции. Во-вторых, их использование необходимо для предупреждения как ранних, так и поздних осложнений. Мы слишком быстро забыли о том, что стрептококковый тонзиллофарингит при неадекватной терапии ведет к развитию ревматизма, гломерулонефрита; острый синусит - к менингиту и т.д. Попытки заменить прием антибиотиков внутрь местными антибактериальными препаратами или препаратами с декларируемой производителями иммуностимулирующей активностью в настоящее время представляются необоснованными, так как нет достоверных клинических данных, показывающих эффективность этих препаратов. Например, рекомендация по применению препарата фузафунгин - "местное лечение воспалительных инфекционных заболеваний носоглотки и дыхательных путей: риниты, синуситы, фарингиты, тонзиллиты, ларингиты, трахеиты, бронхиты" - свидетельствует не о том, что наконец осуществилась мечта Пауля Эрлиха о "магической пуле", а о том, что мы позволяем себя обманывать, разрешая публикацию подобных рекомендаций. В 1997 г. были опубликованы материалы симпозиума, посвященного изучению препарата "Рибомунил", который продвигается на рынок как специфический иммуностимулятор. Руководитель симпозиума G. Bellanti (США) пришел к следующим вполне корректным выводам - "необходимо дальнейшее исследование этого препарата, как и многих других препаратов с потенциальной способностью стимуляции иммунитета для того, чтобы оценить их значение". 2. Неправильный выбор препарата, доз, путей введения. К сожалению, антибиотики нередко назначают, не задумываясь о наиболее вероятном возбудителе, его чувствительности к антибактериальным препаратам, не учитывая результаты, полученные в контролированных клинических исследованиях. Даже в амбулаторных картах можно встретить назначение типа "антибиотик внутрь". Из-за недостатка знаний многие врачи нередко отождествляют генерики ципрофлоксацина с оральными цефалоспоринами, излюбленными препаратами продолжают оставаться сульфаниламиды, в том числе "стрептоцид под язык" (!), гентамицин или линкомицин внутримышечно у амбулаторных больных. 3. Недостаточное внимание к бактериологическому исследованию. Несмотря на то что эмпирический выбор антибиотиков составляет основу их назначения, так как за исключением стрептококкового тонзиллофарингита нельзя быстро идентифицировать возбудитель, бактериологическое исследование должно обязательно проводиться. Помимо прямой пользы для данного пациента, например, при неэффективности стартовой терапии и необходимости смены антибиотиков, ее значение состоит в получении и накоплении эпидемиологических данных о структуре возбудителей и, что наиболее важно, их чувствительности к антибиотикам. Опора на локальные данные об антибиотикорезистентности позволяет сделать эмпирическую антибиотикотерапию максимально эффективной и поставить ее на научные основы. При лечении инфекций ВДП важно преодолеть нигилизм по отношению к применению антибиотиков, который нередко встречается среди врачей и связан с высокой частотой спонтанного выздоровления. Предпочтение следует отдавать препаратам с наиболее высокой клинической и бактериологической эффективностью, ибо инфекциями ВДП болеют многие 5 миллионы пациентов и небольшие различия в эффективности на практике оборачиваются тысячами случаев неэффективной терапии. Фармакотерапия хроническиого бронхита ХБ характеризуется хроническим диффузным неаллергическим воспалением бронхов и проявляется кашлем с отделением мокроты в течение продолжительного периода. По определению ВОЗ, диагноз ХБ может быть установлен в том случае, если продуктивный кашель отмечается в течение 3 мес на протяжении 2 лет и исключены такие заболевания, как туберкулез легких и бронхоэктазы. В генезе ХБ ведущая роль принадлежит курению и загрязнению внешней среды. Инфекционные агенты имеют значение в стадиях обострения. ХБ практически всегда протекает с признаками бронхиальной обструкции и приводит к прогрессирующему нарушению легочной вентиляции. У больных выслушиваются сухие хрипы различного тембра. При длительном течении заболевания отмечаются одышка, цианоз, клинические признаки эмфиземы легких и легочного сердца. Рентгенологическое исследование на ранних стадиях неинформативно, позднее выявляются признаки эмфиземы легких, диффузного пневмосклероза. Лабораторные данные демонстративны при обострениях, когда фиксируются лейкоцитоз и нейтрофилез, большое количество нейтрофилов и макрофагов в мокроте. При выраженной дыхательной недостаточности обнаруживаются гипоксемия и гиперкапния. При исследовании функции внешнего дыхания выявляются обструктивные нарушения вентиляции, которые постепенно прогрессируют. ХБ вне обострения не является поводом для назначения антибактериальной терапии. Рекомендации прошлых лет по периодической химиопрофилактике обострений в настоящее время не имеют сторонников. Больные ХБ в стадии ремиссии нуждаются в длительной терапии бронхорасширяющими препаратами (холинолитические, симпатомиметические средства, теофиллины), отхаркивающими и другими симптоматическими средствами. К причинам обострения ХБ относят курение, техногенные воздействия, контакт с аллергенами, нестабильность сопутствующей бронхиальной астмы. Важной причиной обострений являются инфекционные агенты, среди которых основными считаются вирусы, пневмококки и гемофильные палочки. Острые респираторные вирусные инфекции ответственны за 30% обострений ХБ. Среди вирусов наибольшее значение имеют вирусы гриппа, парагриппа, риновирусы и коронавирусы. При обострениях ХБ из мокроты больных чаще всего выделяют гемофильные палочки (70%) и пневмококки (30%). Обострения ХБ редко манифестируют высокой лихорадкой. Субфебрильная температура тела возможна, но часто обострения начинаются при нормальной температуре. Поэтому основными критериями обострения ХБ являются: увеличение количества отделяемой мокроты и усиление степени ее гнойности, прогрессирование одышки. Любой из трех перечисленных признаков может служить основанием для решения вопроса о начале антибактериальной химиотерапии. При аускультации определяются сухие хрипы различного тембра, иногда влажные хрипы. Ознобы и плевральная боль характерны для пневмонии. При исследовании периферической крови часто выявляют умеренный лейкоцитоз и нейтрофилез. Нередко клинически трудно дифференцировать обострение ХБ от пневмонии, в этих случаях приоритетным методом диагностики является рентгенологическое исследование легких. Рентгенологическое исследование обязательно при лихорадке и выявлении влажных хрипов. При выраженной дыхательной недостаточности и/или интоксикации больные нуждаются в госпитализации. Программа лечения обострений ХБ включает применение антибактериальных средств, оксигенотерапию, использование бронхорасширяющих и отхаркивающих препаратов, а при тяжелой обструктивной дыхательной недостаточности – кортикостероидов. Выбор антибиотика фактически сводится к назначению препаратов, наиболее активных в отношении одновременно двух наиболее вероятных микроорганизмов - пневмококка и гемофильной палочки. За рубежом 6 обычно применяют амоксициллин, доксициклин и ко-тримоксазол в течение 10 – 14 дней. В России с учетом тенденций антибиотикорезистентности более предпочтительными представляются амоксициллин/клавулановая кислота, ампициллин/сульбактам, азитромицин, рокситромицин, спирамицин, цефуроксим аксетил, цефтибутен, хотя препаратами выбора могут быть также амоксициллин и доксициклин. ХБ часто сочетается с инфекционно-зависимой бронхиальной астмой. Аллергологический анамнез у таких пациентов обычно отягощен. Поэтому, даже если нет указаний на аллергию к пенициллинам, целесообразно избегать назначения аминопенициллинов таким больным. Если у пациента были аллергические реакции на пенициллины, то не должны применяться все bлактамные антибиотики. В подобном случае, естественно, выбор терапии ограничивается макролидами, тетрациклинами и, возможно, фторхинолонами. В то же время для лечения обострений ХБ у больных бронхиальной астмой могут с успехом использоваться левомицетин и близкий к нему флуимуцил-антибиотик (тиамфеникол + N ацетилцистеин). У больных старше 65 лет ХБ нередко протекает на фоне различных сопутствующих заболеваний. При обострениях бронхита у этих пациентов нередко выделяются не только пневмококки и гемофильные палочки, но также энтеробактерии и стафилококки, причем в 3/4 культуральных исследований мокроты обычно обнаруживается сочетание грамположительной и грамотрицательной флоры. Естественно, что при потенциально столь широком спектре микроорганизмов трудно ожидать высокой эффективности применения макролидов. Оправданным может быть использование цефалоспоринов III поколения и аминопенициллинов в комбинации с ингибиторами b-лактамаз. У больных старших возрастных групп с сопутствующей бронхиальной астмой и/или аллергией к пенициллинам препаратами выбора являются фторхинолоны и левомицетин. Особый подход в выборе антибактериальной терапии требуется у больных с обострением ХБ, протекающего с бронхоэктазами. Кроме пневмококков, стафилококков, гемофильных палочек и энтеробактерий, у этих больных особую этиологическую значимость могут иметь синегнойная палочка и анаэробы. В подобной клинической ситуации логично начинать лечение фторхинолонами (офлоксацин, ципрофлоксацин). При отсутствии эффекта оправдано назначение цефалоспоринов последних поколений (цефтазидим, цефпиром) или сочетаний цефалоспоринов III поколения с аминогликозидами и/или метронидазолом. Впрочем, у больных с бронхоэктазами иногда удается избежать эскалации системной антибактериальной химиотерапии путем местного применения антибактериальных средств при эндобронхиальных санациях. Лечение развернутых обострений ХБ может представлять значительные трудности в связи с дыхательной недостаточностью, декомпенсацией легочного сердца, обострением сопутствующих заболеваний у больных пожилого возраста. Ранняя и эффективная антибактериальная химиотерапия обеспечивает лучший прогноз, сокращает сроки лечения и объем применяемой терапии, улучшает качество жизни больных. Фармакотерапия пиелонефрита Подходы к лечению больных острым и хроническим пиелонефритом различны. Острый пиелонефрит без признаков обструкции подлежит незамедлительному лечению антибактериальными препаратами, в случае обструкции лечение начинают с восстановления пассажа мочи с помощью катетера (стента) или нефростомии. Лечение хронического пиелонефрита условно подразделяется на два этапа — лечение в период обострения (практически не отличается от терапии острого пиелонефрита) и противорецидивное. Антибактериальные препараты, применяемые при пиелонефрите, должны обладать высокими бактерицидными свойствами, широким спектром действия, отсутствием нефротоксичности, выводиться с мочой в высоких концентрациях. Используют антибиотики, 7 сульфаниламиды, нитрофураны, производные налидиксовой и пипемидовой кислот, хинолоны, фторхинолоны, растительные антисептики. Основой антибактериальной терапии являются антибиотики, в первую очередь полусинтетические пенициллины (ампициллин, ампиокс, оксациллин), активно воздействующие на кишечную палочку — главную причину острых инфекций мочевыделительной системы (до 80%). Их назначают внутрь или (лучше) парентерально в обычной дозировке (2,0–4,0 г/сут.) в течение 7– 10 дней. Многие авторы отмечают развитие резистентности к ампициллину (в 30–60% случаев), что, по-видимому, обусловлено наиболее частым его применением. Для преодоления устойчивости бактерий к аминопенициллинам их сочетают с ингибиторами b-лактамаз клавулановой кислотой, сульбактамом и др. Комбинированные препараты - аугментин (амоксициллин + клавулановая кислота) для приема внутрь и уназин (ампициллин + сульбактам) для парентерального применения активны в отношении стафилококков и грамотрицательных бактерий, выделяющих b-лактамазы.Специально предназначены для лечения инфекций, вызванных Pseudomonas aeruginosa, карбенициллин, тикарциллин, пиперациллин, азлоциллин. Широко применяют и другие b-лактамные антибиотики — цефалоспорины, обладающие умеренной нефротоксичностью. Для приема внутрь из цефалоспоринов 1-го поколения используют цефалексин (активен в отношении как стафилококков, стрептококков, так и кишечной палочки, клебсиеллы) в дозе 1–2 г/сут. (по 0,25 г или 0,5 г 4 раза) в течение 7–14 дней. В амбулаторной практике для лечения неосложненных бактериальных инфекций наиболее распространены цефалоспорины 2-го поколения, спектр действия которых шире: цефаклор (цеклор) в дозе 0,75 г/сут. (по 0,25 г 3 раза), цефуроксим аксетил (зиннат) в дозе 0,5 г/сут. (по 0,25 г 2 раза ). Все препараты 1-го и 2-го поколения выводятся почками в неизмененном виде, что создает в паренхиме и в моче высокую их концентрацию. При осложненных инфекциях используют цефалоспорины 3-го поколения: оральные (цефетамет пивоксил, цефиксим и др.), парентеральные — цефотаксим (клафоран), цефтазидим (фортум, кефадим), для которых характерны более длительный период полувыведения и двойной путь экскреции — с мочой и желчью. При хроническом течении процесса, смешанной инфекции с присутствием атипичной флоры (b-лактамазные антибиотики, в том числе цефалоспорины, недостаточно эффективны. Препаратом, отличающимся сверхшироким спектром действия и устойчивостью к b-лактамазам, является имипенем/циластатин (тиенам), рассматриваемый как резервный антибиотик (из группы карбапенемов). Аминогликозиды (гентамицин, тобрамицин, бруломицин, амикацин) оказывают выраженное действие на грамотрицательные аэробные бактерии (Pseudomonas spp., Enterobacter spp., Escherichia coli, Proteus spp., Klebsiella spp.), они являются средством выбора при серьезных инфекциях, в частности внутрибольничных. В тяжелых случаях аминогликозиды комбинируют с антисинегнойными пенициллинами или цефалоспоринами. Аминогликозиды плохо всасываются в желудочно-кишечном тракте и выводятся почками, в связи с чем их применяют парентерально и при почечной недостаточности дозу снижают. Основным недостатком всех аминогликозидов являются выраженные ото- и нефротоксичность (в результате повреждения канальцев развивается неолигурическая почечная недостаточность). Частота поражения почек при лечении аминогликозидами достигает 17%, снижения слуха — 8%. При лечении необходимо контролировать уровень калия, мочевины, креатинина сыворотки крови. Факторами риска развития нефротоксичности к аминогликозидам являются: престарелый возраст больного, повторное применение препарата с интервалом менее 1 года, хроническая диуретическая терапия, сочетанное применение с цефалоспоринами. 8 В последние годы все шире применяются препараты из группы фторхинолонов: офлоксацин (таривид), пефлоксацин (абактал), норфлоксацин (нолицин), ципрофлоксацин (цифран, ципробай), активные в отношении большинства грамотрицательных микроорганизмов, включая Pseudomonas aeroginosa, и многих грамположительных кокков, в том числе Staphylococcus aureus. Они эффективны, хорошо переносимы, применяются 1–2 раза в день. Из-за непредсказуемости осложнений значительно реже назначают левомицетин, который ранее широко использовался при мочевой инфекции. Современные тетрациклины (доксициклин, миноциклин) из-за быстро развивающейся устойчивости микроорганизмов считаются при лечении пиелонефрита резервными средствами. Нитрофураны близки по действию к антибиотикам широкого спектра действия, они являются средством выбора у беременных. Активны в отношении грамположительной и грамотрицательной флоры (кишечной палочки, протея, стафилококков). Выделяются нитрофураны и их метаболиты почками, частично — с желчью и в просвет кишечника. Высокая концентрация препарата в моче сохраняется до 12 ч. Для предотвращения побочных эффектов рекомендуют обильное питье, антигистаминные препараты и витамины группы В. Наибольшее распространение получили фурадонин и фурагин в дозе 0,2–0,4 г/сут. (по 0,1–0,15 г 3 раза в день). При наличии почечной недостаточности опасны нитрофурановые полиневриты. Сульфаниламиды оказывают бактериостатическое действие на грамположительные и грамотрицательные бактерии. В настоящее время их роль существенно уменьшилась вследствие распространения устойчивых штаммов к ним, частых серьезных побочных эффектов и появления более активных антибиотиков. Продолжает широко использоваться ко-тримоксазол (бисептол, септрим и др.), в состав которого, помимо сульфаметоксазола, входит триметоприм. Препарат назначают в дозе 0,96 г/сут. (по 0,48 г 2 раза в день), рекомендуется запивать его ощелачивающим питьем. Основное показание — неосложненные мочевые инфекции, вызванные грамотрицательными бактериями, в частности кишечной палочкой. Препараты налидиксовой кислоты (невиграмон, неграм, налидикс) влияют главным образом на грамотрицательную флору (кишечная палочка, клебсиелла). Поскольку они оказывают умеренный терапевтический эффект, их чаще используют для профилактики обострений, назначая курсами по 10–12 дней в дозе 2,0–4,0 г/сут. (по 0,5 г 4 раза). Они малотоксичны. Нитроксолин (5-НОК) — производное оксихинолина, оказывает антибактериальное действие на грамположительные и грамотрицательные бактерии, эффективен в отношении некоторых грибов (рода Candida), выводится в неизмененном виде почками. Чаще назначают для профилактики обострений хронического пиелонефрита курсами по 2–3 недель в дозе 0,4 г/сут. (по 0,1 г 4 раза в день). Какова тактика лечения пиелонефрита? Обычно лечение инфекции мочеполового тракта начинают до получения результатов бактериологического исследования мочевой культуры и определения чувствительности к ней (эмпирическая антибактериальная терапия). Предполагается, что диагноз мочевой инфекции может быть основан на клинической картине и результатах анализов мочи (схема). В эмпирическом подходе определяющими являются локализация, характер (острый, хронический) и выраженность инфекционного процесса. При неосложненном впервые выявленном пиелонефрите терапию начинают с ампициллина (амоксициллина), цефалоспоринов 1–2-го поколения или ко-тримоксазола. Если эффект в течение 2–3 дней отсутствует (сохраняются лихорадка, интоксикация), добавляют гентамицин (до 180 мг/сут. внутримышечно в 3 приема), который расширяет спектр действия указанных антибиотиков, или назначают фторхинолоны, цефалоспорины 3-го поколения. При тяжелом течении инфекции антибактериальные средства следует сразу назначать внутривенно (до нормализации температуры и улучшения состояния пациента), предпочтительнее цефалоспорины 3-го поколения, карбопенициллины или уреидопенициллины 9 в сочетании с внутримышечным введением аминогликозидов, ингибиторы b-лактамаз, монобактамы (азтреонам), карбапенемы. При осложненной инфекции (урологические заболевания, аномалии развития мочеполовой системы), нередко ассоциирующейся с госпитальной флорой, катетеризацией мочевого пузыря и другими эндоскопическими процедурами, чаще выявляются клебсиеллы, протей, энтеробактер, энтерококки, синегнойная палочка, что диктует изначально использование комбинации b-лактамазных антибиотиков с ингибиторами b-лактамаз, цефалоспорины 2–3-го поколения, фторхинолоны. Эмпирическая аетибактериальная моно- и комбинированная терапия сепсиса На сегодняшний день наиболее приемлемыми средствами эмпирической антибактериальной монотерапии являются такие новейшие антибиотики, как карбапенемы (имипенем/циластатин и меропенем) и “защищенные” пенициллины расширенного спектра действия (пиперациллин/тазобактам и тикарциллин/клавулановая кислота). Если точно исключена анаэробная этиология, то возможно также применение в качестве монотерапии парентеральных цефалоспоринов IV поколения (цефепим). В комбинированной терапии наиболее часто (в мировой практике) используется комбинация парентеральных цефалоспоринов III-IV поколений (цефтриаксона, цефотаксима, цефтазидима) с аминогликозидами II-III поколений (амикацин имеет наиболее широкий спектр активности). При подозрении на участие анаэробов показаны комбинации антибиотиков с антианаэробной активностью - клиндамицина или метронидазола с “защищенным” пенициллином или парентеральным цефалоспорином (лучше анаэробным). 5. Примерные вопросы по теме для рейтингового контроля 1. Клиническая характеристика синдрома пневмонии, рациональная фармакотерапия пневмоний (включая осложнение абсцессом). 2. Выбор ЛП при внебольничных и внутрибольничных пневмониях; рациональная фармакотерапия абсцесса легких. 3. Клиническая характеристика синдрома бронхита; выбор ЛП для лечения необструктивного бронхита: поствирусного бронхита, обострения хр. простого и гнойного бронхита. 4. Клиническая характеристика синдрома; принципы антибиотикотерапии сепсиса; эмпирическая моно- и комбинированная терапия сепсиса. 5. Клиническая характеристика пиелонефрита; рациональная фармакотерапия острого и хронического пиелонефрита; противорецидивное лечение пиелонефрита. 6. Перечень практических навыков 6.1. На основания самостоятельной диагностической ориентации в природе и характере данного конкретного заболевания у исследуемого пациента с инфекционно-воспалительным поражением, правильной оценки клинических факторов, влияющих на рациональный индивидуализированный выбор ЛП, а также опираясь на собственные фармакологические знания и широкий спектр авторитетной фармакологической информации, студент-фармацевт формирует навыки выделения групп(ы) ЛП предпочтительного выбора и далее рационально обосновывает оптимальность 1-2 ЛП - эффективных, безопасных, приемлемых и стоимостно доступных. 6.2. Далее, в отношение рационально выбранных ЛП (антигипертензивных, антиангинальных или антиаритмических средств), формируются навыки рационального выбора режима дозирования и способа введения ЛП (с учетом возраста больного, сопутствующих заболеваний и осложнений, функционального состояния сердечно-сосудистой системы, равно как состояния желудочно-кишечного тракта, органов метаболизма и экскреции у данного больного, 10 возможности лекарственного взаимодействия, а также факторов, способствующих изменению чувствительности к выбранному ЛП). 6.3. На этой основе в дальнейшем отрабатываются навыки прогнозирования возможного развития побочных эффектов и, соответственно, - назначения соответствующих методов оценки и контроля эффективности и безопасности, включая меры по диагностике, коррекции и профилактике побочных реакций (назначения мониторного наблюдения). 6.4. На заключительной стадии формируется навык рационального комбинирования ЛС. 7. Самостоятельная работа студентов 7.1. На основании проведенного тщательного и всестороннего субъективного обследования больного (расспроса и изучения анамнестических данных), студент-фармацевт самостоятельно формулирует индивидуализированный диагноз у конкретных больных с инфекционновоспалительным поражением определенных органов и систем организма. 7.2. В каждом отдельном случае студент-фармацевт самостоятельно осуществляет рациональный выбор 1-2 оптимальных ЛП (на основе максимально точного диагноза и с обязательным выяснением этиопатогенетических и клинических детерминант данного конкретного заболевания). Далее, на основе всестороннего выяснения и знания фармакодинамических и фармакокинетических особенностей выбранных ЛП он самостоятельно определяется с выбором пути их введения ЛП, дозированием, продолжительностью курса лечения, кратностью введения и прочими особенностями рационального применения рационально выбранных ЛП. 7.3. После самостоятельного назначения курсовой терапии выбранным(и) ЛП, студент, на основе прогнозирования возможных побочных реакций, самостоятельно определяется с планом мониторирования назначенных ЛС - с выбором методов оценки и контроля эффективности и безопасности назначенных ЛП. 8. Литература 8.1 Основная 1. Вебер В.Р. Клиническая фармакология. СПб.: Человек. 2004. – 448 с., 2006 – 539 с., 2009 – 445 с., 2. Д.А.Харкевич. Фармакология. Учебник. М.: Медицина, 2004, 2005, 2008 3. Харкевич Д. А. Фармакология: Учебник для студентов мед. вузов / Д. А. Харкевич. - 10-е изд., испр., перераб. и доп. - М.: ГЭОТАР-Медиа, 2010. - 750 с. 4. Сычев Д.А. Клиническая фармакология. Общие вопросы клинической фармакологии. Практикум. Учебное пособие. – М.: ГЭОТАР-Медиа, 2011. – 223 с. 8.2 Дополнительная 1. Венгеровский А.И. Лекции по фармакологии: Для врачей и провизоров:Учеб.пособие для мед.вузов/ А.И. Венгеровский. ─ 3-е изд.,перераб.и доп. ─ М.:Физматлит, 2007. ─ 702 с. 2. Лекарственная болезнь: диагностика и лечение: Метод. рекомендации/ Сост.:В.Р.Вебер, Л.И.Шелехова, Т.Х.Расулова;Новгород.гос.ун-т им.Ярослава Мудрого. ─ Великий Новгород, 2009. ─ 43 с. 3. Зборовский А.Б. Неблагоприятные побочные эффекты лекарственных средств/ А.Б. Зборовский, И.Н. Тюренков, Ю.Б. Белоусов; Авт.: Л.Е.Бородкина и др. ─ М.:Медицинское информ.агентство,2008. ─ 651 11