Применение нобена (идебенон) в комплексном лечении частой
advertisement

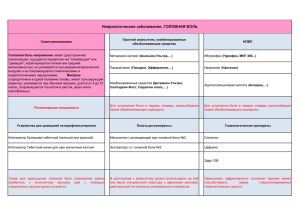
КРАТКИЕ СООБЩЕНИЯ Применение нобена (идебенон) в комплексном лечении частой эпизодической и хронической мигрени К.м.н., рук. отд. М.И. КОРЕШКИНА The use of noben (idebenone) in the complex treatment of episodic and chronic migraine M.I. KORESHKINA Центр головной боли Международной клиники MEDEM, Санкт-Петербург Ключевые слова: нобен (идебенон), мигрень, хроническая головная боль. Key words: noben (idebenone), chronic migraine. По данным статистики, мигренью страдает около 15% населения [7]. Врачи общей практики европейских стран отмечают, что 4% всех пациентов жалуются на головные боли. Вторичные головные боли встречаются реже — только у 2—3% и, как правило, являются результатом какого-либо заболевания [22]. В специализированных центрах головной боли отмечается рост числа пациентов с хроническими головными болями [13]. Были проанализированы финансовые потери от первичных головных болей — мигрени и головной боли напряжения в некоторых европейских странах. Так, в Великобритании за 1 год случается более 190 000 приступов мигрени, что приводит к отсутствию на работе или учебе более 100 000 человек или потере более 25 млн рабочих или учебных дней каждый год [23]. В 2007 г. в странах Европы было затрачено на лечение мигрени более 27 млрд евро. Прямые и косвенные расходы составляют больше, чем те же затраты на эпилепсию, паркинсонизм и инсульты. В России у 28 млн пациентов, страдающих мигренью, средняя частота приступов составляет 1 эпизод в месяц. За 12 мес количество приступов мигрени может составлять 336 млн [9]. По показателю лет дезадаптации DALY (dissability adjusted life years) мигрень занимает 19-е место среди наиболее распространенных заболеваний, у женщин — 9-е. В среднем, пациенты, страдающие мигренью, отсутствуют на работе 25 рабочих дней в год, а около 10 дней в году их состояние характеризуется снижением трудоспособности [18]. Таким образом, мигрень — это не только важная медицинская, но и социальная проблема. В последние годы сведения о мигрени, как о заболевании, существующем только в эпизодической форме, претерпели изменения. Термин «трансформированная мигрень» применялся для описания пациентов, имеющих эпизодическую мигрень, у которых в течение заболевания произошло увеличение частоты приступов головной боли от приближающихся к ежедневным до ежедневных. Международное Общество по изучению головной боли (International Headache Society — IHS) в 2004 г. опубликовало Международную классификацию головной боли, 2-го издания (МКГБ—II), в которой термин «трансформированная мигрень» был изменен на «хроническую мигрень» [16]. По предложенным критериям, для установления диагноза «хроническая мигрень» достаточно 8 приступов мигрени в месяц, купированных триптанами [20]. К факторам риска перехода эпизодической головной боли в хроническую относятся: женский пол, одиночество (разведенные, вдовы, вдовцы, одинокие), низкий уровень образования, ожирение, предшествующие черепномозговые травмы, эпизодическая мигрень, злоупотребление анальгетиками [14]. При хронификации головных болей происходит резкое снижение качества жизни пациента. По данным литературы [8, 10, 21] наиболее частыми коморбидными расстройствами при мигрени являются: депрессия, тревога, астенические состояния, артериальная гипертензия и артериальная гипотония, феномен Рейно, эпилепсия, панические атаки, гипервентиляция, избыточная масса тела, бронхиальная астма и дисфункция желудочно-кишечного тракта. По данным Центра головной боли Международной клиники MEDEM, одним из наиболее частых синдромов коморбидной хронической мигрени является астения. Наблюдается прямая связь между частотой и длительностью приступов головной боли и выраженностью астенического расстройства. Лечение частой и хронической мигрени включает несколько этапов. Наряду с важнейшей задачей — подбором лекарственного средства для купирования приступа из © М.И. Корешкина, 2010 e-mail: korishkina@medem.ru Zh Nevrol Psikhiatr Im SS Korsakova 2010;110:6:98 98 ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 6, 2010 ЛЕЧЕНИЕ МИГРЕНИ группы триптанов, необходима: профилактическая терапия, выявление триггеров приступа и их исключение из жизни пациента, дополнительные лекарственные (в том числе ноотропы) и нелекарственные (психотерапия, методики релаксационной лечебной физкультуры и т.д.) методы лечения. Среди зарегистрированных в Российской Федерации ноотропных препаратов в последние годы заслуженное внимание привлекает препарат идебенон (нобен). Идебенон активирует дыхательную функцию митохондрий и оказывает положительное влияние на процессы перекисного окисления липидов в ткани головного мозга, на фоне его применения в нервной ткани активируется образование АТФ и утилизация глюкозы [4, 15, 19]. Препарат обладает ноотропным и антиоксидантным эффектом, имеет антиастеническое, психостимулирующее и антидепрессивное действие [16]. Идебенон повышает скорость сенсомоторных реакций, оказывает выраженное специфическое действие на когнитивные процессы, улучшая показатели краткосрочной и оперативной памяти и внимания [2, 11]. Показаниями к назначению препарата являются: цереброваскулярные расстройства, астенические состояния, психоорганический синдром, эмоционально-лабильные расстройства. Целью исследования было изучение эффективности нобена при разных клинических проявлениях мигрени. Материал и методы Обследовали 42 пациента (все женщины) в возрасте от 25 до 45 лет, обратившихся в центр по лечению головной боли в связи с частыми головными болями и последующим за этим снижением качества жизни. У большинства (57%) пациенток поводом к обращению стал выраженный астенический синдром на фоне частых приступов головной боли. Важным представляется тот факт, что обратиться за помощью в специализированный центр по лечению головной боли пациенток заставила не сама головная боль, а сопутствующие ей коморбидные симптомы: ухудшение памяти, рассеянность внимания, повышенная утомляемость и снижение настроения. Влияние именно коморбидных мигрени процессов на снижение качества жизни пациентов отмечалось и другими исследователями [6]. Для установления диагноза были использованы следующие диагностические методики: критерии диагностики эпизодической и хронической мигрени (МКГБ — II); визуально-аналоговая шкала ВАШ (от 0 до 10); шкала функциональной активности при мигрени МИДАС; дневник головной боли (разработанный Европейской Федерацией головной боли — исследование “Eurohead”); магнитно-резонансная томография (МРТ) головного мозга и магнитно-резонансная ангиография для исключения вторичного характера головной боли на высокопольном аппарате 3,0 Тл; допплерографическое исследование сосудов головного мозга; электроэнцефалография (ЭЭГ); анкета сопутствующих симптомов и коморбидных расстройств. Для купирования приступов мигрени пациенту подбирался индивидуально триптан из списка препаратов, зарегистрированных в Российской Федерации — элетриптан, суматитриптан, золмитрипатан [1, 12]. В качестве профилактической терапии использовались препараты, ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 6, 2010 рекомендованные Российской ассоциацией по изучению головной боли [10] — антиконвульсанты и антидепрессанты. В качестве дополнительного лечения астенического синдрома применялся идебенон (нобен) в дозе 90 мг в сутки в утреннее и дневное время в течение 3 месяцев. Для оценки результатов лечения использовались различные способы эффективности профилактической терапии при мигрени [5, 10]. Результаты 26 пациенток имели частую форму эпизодической мигрени — от 6 до 8 приступов в месяц, а у 16 женщин была диагностирована хроническая мигрень (более 15 приступов в месяц). По данным шкалы МИДАС, средний балл потери трудоспособности составил более 20, то есть выявлялось выраженное снижение функциональной активности. «Портрет» типичной пациентки с хронической мигренью представлен в табл. 1. В дневнике головной боли ежедневно в течение месяца пациентки фиксировали частоту, длительность и интенсивность головной боли по шкале ВАШ, локализацию головной боли, сопутствующие симптомы — фотофобию, фонофобию, тошноту/рвоту. Также отмечалось количество и названия препаратов, применяемых для купирования приступа мигрени, их эффективность и выраженность снижения работоспособности. Ведение анкеты показало, что пациент не всегда отдает себе отчет в количестве приступов и применяемых препаратов. После подведения итогов 1-го месяца ведения дневника (до начала лечения) количество приступов и лекарственных средств оказалось гораздо больше, чем предполагал пациент. По данным МРТ, у 39 (94%) пациенток были выявлены дисциркуляторные очаги в белом веществе головного мозга (табл. 2). Последние исследования [17] показали, что мелкие очаги, выявляемые на МРТ у больных с мигренью, могут быть очагами демиелинизации, глиозом и, наоборот, зонами разрежения глии. Наличие очагов отражает глубину поражения мозгового вещества при тяжелых формах мигрени. Отмечена закономерность, что именно у пациенток с хронической головной болью и наличием множественных очагов в белом веществе более часто были зафиксированы жалобы на снижение памяти, ухудшение внимания, особенно при работе с числами, сложными формулировками, Таблица 1. «Портрет» пациентки с хронической мигренью Возраст, лет Образование среднее специальное высшее Рабочий день >8 ч в сутки Руководитель среднего и высшего звена Количество приступов головной боли в месяц Длительность приступов головной боли, ч Сон < 6 ч в сутки Работа за компьютером >4 ч в день (в среднем составила 6,5 ч за рабочий день) Наличие постоянных стрессовых ситуаций Отсутствие отпуска в течение 2 недель за последние 12 мес Нарушение режима сна — позднее засыпание 33,8 5% 95% 92% 80% 12,3 6,2 95% 65% 82% 60% 75% 99 КРАТКИЕ СООБЩЕНИЯ Таблица 2. Изменения по данным МРТ у пациенток с эпизодической и хронической мигренью в головном мозге Морфологические изменения Очаги в белом веществе Отсутствие очагов Расширенные периваскулярные пространства Гипоплазия позвоночной артерии Аномалия Арнольда — Киари I Арахноидальная киста Число пациентов абс. % 31 77 11 23 12 28 3 1 1 снижение работоспособности. Таким образом, именно этим больным было показано применение препарата из группы ноотропов. На ЭЭГ у 9 (21%) больных патологических изменений выявлено не было. У 21 (50%) больной отмечались признаки умеренной диффузной функциональной корковой дезорганизации со снижением индекса α-активности, умеренными пространственными корковыми нарушениями и дезадаптацией на функциональные нагрузки. У 12 (29%) пациенток были выявлены выраженные функциональные нарушения с подавлением основного ритма, диффузными ирритативными корковыми нарушениями с признаками очаговой заинтересованности, соответствовавшими выявленным при МРТ изменениям. Следует отметить, что выявляемые изменения биоэлектрической активности при ЭЭГ не носят специфического характера, а лишь отражают функциональное состояние работы головного мозга, что определяется наличием сопутствующих заболеваний (травмы, цереброваскулярные расстройства) и индивидуальными особенностями нервной деятельности. Однако у ряда пациентов с наиболее тяжелым типом мигрени, особенно в период приступа, можно отметить общие черты изменения корковой биоэлектрической активности в виде запредельного коркового торможения, функциональной корковой дезадаптации, а в 7 случаях даже фокальной заинтересованности с эпилептиформными элементами, что позволило обоснованно применить противоэпилептические препараты в качестве профилактической терапии. При контрольном исследовании, проведенном через 3 мес с начала комплексной терапии, в 90% случаев были отмечены улучшение или полная нормализация показателей функциональной активности головного мозга. Применение ЭЭГ как вспомогательного метода позволяет патогенетически подходить к рекомендуемой терапии и контролировать результат лечения. Результаты оценки эффективности проведенного лечения представлены в табл. 3. Субъективно отмечена хорошая переносимость комплексной терапии триптанами, препаратами профилактической терапии и нобена. Не было зафиксировано случаев отмены нобена из-за плохой переносимости. Несмотря на сложную схему лечения каждой пациентки (подбор триптана и профилактического средства проводился индивидуально), все они успешно завершили 3-месячный курс лечения. После его окончания больные продолжили или только купирование триптаном приступов мигрени (при числе приступов менее 4 в месяц), или прием триптана в сочетании с профилактическим средством. Дополнение специализированной терапии с применением нобена позволило не только улучшить память и внимание, но и добиться повышения качества жизни больных. Следует отметить, что достаточно быстрое достижение позитивного результата от ноотропной терапии — через 2—3 нед от начала лечения, заключавшемся в снижении утомляемости, повышении настроения и работоспособности пациентов, дало надежду на успех лечения и позволило провести запланированный курс полностью. Большой проблемой для проведения профилактического лечения у пациентов с хронической головной болью является медленное наступление улучшения интенсивности и частоты приступов головной боли. Комбинация специфического лечения мигрени с препаратом из группы ноотропов дала возможность получить более быстрый результат и позволила повысить эффективность лечения. Таким образом, использование идебенона (нобена) в комбинированной терапии у пациенток с частой и хронической мигренью позволяет быстрее получить терапевтический эффект и улучшить качество жизни пациентов. Удобство применения и хорошая переносимость препарата дают возможность его использования в комбинации с триптанами и профилактической терапией. Таблица 3. Результаты комплексной медикаментозной терапии пациентов с частой эпизодической и хронической мигренью Показатель Редукция частоты атак на 50% в соответствии с дневником головной боли Снижение выраженности атак Снижение ограничения социальной активности Улучшение памяти Уменьшение тревоги и депрессии Способ оценки Частота атак в мес До лечения 12,3 Через 3 мес лечения 3,8 Выраженность боли по шкале ВАШ (баллы) Балл по шкале MIDAS 8,4 >20 4,7 <10 Балл по краткой шкале оценки психического статуса (MMSE) Балл по госпитальной анкете тревоги и депрессии (HADS) 26,3 28,2 12,2 5,4 ЛИТЕРАТУРА 1. Амелин А.В. Современные аспекты диагностики, патогенеза и лечения мигрени. М: ООО НТЦ АМТ 2007; 88. 2. Бочкарев В.К., Файзуллоев А.З., Бородин В.И., Аведисова А.С. Психофизиологическая характеристика действия нобена. Психиат и психофармакол 2004; 06: 4. 100 3. Воронкова К.В., Мелешков М.Н. Применение нобена (идобенон) в терапии при деменции и с нарушениями памяти, не достигшими степени деменции. Журн неврол и психиат 2008; 4: 27—32. 4. Дамулин И.И. Применение идебенона (нобена) в неврологической практике. Журн неврол и психиат 2006; 106: 11: 66—71. ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 6, 2010 ЛЕЧЕНИЕ МИГРЕНИ 5. Наприенко М.В., Филатова Е.Г. Катадолон в лечении хронической головной боли напряжения. Лечение нервных болезней 2006; 1: 34—38. 6. Осипова В.В., Вознесенская Т.Г. Коморбидность мигрени: обзор литературы и подходы к изучению. Журн нeврол и психиат 2007; 107: 3: 64—73. 15. Geramel V., Darin N., Chretien D. Coenzyme Q10 and idebenone in the therapy of respiratory cchain diseases: rationale and comparative benefits. Mol Gent Metabol 2002; 77: 21—30. 16. Headache classification subcommittee of the International Headache Society. The International Classification of Headache Disorders 2nd Edition. Cephalalgia 2004; 24: Suppl 1: 100—160. 7. Осипова В.В., Табеева Г.Р. Первичные головные боли. Практическое руководство. М 2007; 56. 17. 8. Осипова В.В. Головная боль напряжения. Практическое руководство для врачей. М: ОГТИ. Рекламная прдукция 2008; 44. Igarashi H., Sakai F., Kan S. Magnetic resonance imaging of the brain in patients with migraine. Cephalalgia 1991; 11: 69—74. 18. 9. Рачин А.П. Фармакоэкономическое обоснование применения назального спрея имигран. Атмосфера. Нервные болезни 2009; 2. 10. Табеева Г.Р., Азимова Ю.Э. Профилактическое лечение мигрени. М 2009; 84. Leonardi M., Steiner T.J., Scher A.T., Lipton R.B. The Global Burden of migraine: measuring disability in headache disorders with WHO; Classification of Functioning Disability and health (ICF). J headache Pain 2005; 6: 429—440. 19. 11. Федин А.И., Румянцева С.А. Современные подходы к энергокорригирующей терапии гипоксических поражений мозга. Consilium medicum: журнал доказательной медицины для практикующих врачей 2007; 9: 8: 104—105. Mordente A., Martorana G.E., Minotti G. Antioxidantties of 2,3 — dimethoxy -5-methyl — 6 —(10-hydroxydecyl) — 1,4- benzoquinone (idebenone). Chem Res Toxicol 1998; 11: 54—63. 20. Olesen J., Bousser M.G., Diener H.C. Headache Classification Committee. New appendix criteria open for a broader concept of chronic migraine. Cephalalgia 2006; 26: 742—746. 21. Jensen R., Stovner L. Epidemiology and comorbidity of headache. Lancet Neurol 2008; 7: 4: 354—362. 22. Sher A., Lipton R.B., Stewart W. Risk factor for chronic daily headache. Current Pain and Headache Reports 2002; 6: 486—491. 23. Steiner T.J., Scher A.J., Stewart W.F. The prevalence and disability of adult migraine in England and their relationship to age, gender and ethnicity. Cephalalgia 2003; 23: 519—527. 12. Филатова Е.Г. READY — первое российское мультицентровое исследование эффективности РЕЛПАКСА (элетриптан) при лечении приступов мигрени. Лечение заболеваний нервной системы 2006; 2: 19: 38—43. 13. Яхно Н.Н., Парфенов В.А., Алексеев В.В. Головная боль. М: Ремедиум 2000; 150. 14. BASH. Guidelines for all healthcare professional for the diagnosis and management of migraine, tension-type, cluster and medication-overuse headache. British Association for the Study of Headache 2007 www.bash. org.uk ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 6, 2010 101