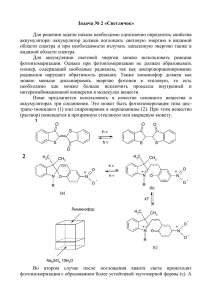
Наночастицы для доставки лекарственных и диагностических
advertisement

Московский государственный университет тонких химических технологий им. М.В. Ломоносова Кафедра БТ и БНТ Подходы к разработке новых терапевтических агентов на основе ковалентных и нековалентных модификаций используемых лекарственных средств для улучшения доставки препаратов к клеткам-мишеням Аспирант Руководитель Дьякова Л.Н. доц. Шастина Н.С. Идеальное лекарство: 1. Хорошая избирательность (селективность) – только на одну мишень 2. Направленность на орган-(ткань-, клетки-)-мишень 3. Контролируемое высвобождение (controlled release, sustained release) • равномерное по времени • контролируемое по месту • зависимое от «концентрации мишени» 4. Высокая эффективность (действует в малых дозах, слабые побочные эффекты) 5. Удобная для пациента форма (пероральная, трансдермальная, интранозальная и т.п.) 6. Высокая биодоступность (хорошее прохождение через тканевые барьеры); в том числе и экономический фактор Два направления для решения этих проблем 1. Конструирование специальных систем доставки лекарств – для изменения фармакокинетики (ADME-Tox) (нековалентное связывание) 2. Создание пролекарственных соединений (ковалентное связывание) для предотвращения недостатков фармакологически активных соединений ProDrug Design Изменение ADME-Tox Абсорбция Два барьера: • метаболический – рН, – ферменты, – Р-гликопротеин (P-gp, продукт гена MDR-1) • физический – муциновый слой – плотные контакты между клетками эпителия – клеточная мембрана Вещества, способные проникнуть через эпителий кишечника • Вещества со средним Кр – пассивная диффузия через мембрану • Липофильные в-ва (с желч. кислотами) • Питательные в-ва (а.к., моносахариды и т.п.) – посредством специф. переносчиков • В12, EGF – рецепторопосредованный трансцитоз • Мм до 600 Да Вещества, не способные проникнуть через эпителий кишечника • Деградирующие в желудке и/или в кишечнике • Полимеры: в т.ч. белки, НК, полисахариды • Плохо растворимые вещества Способы увеличения биодоступности и организации равномерного, контролируемого высвобождения • Защита от воздействия среды • Увеличение концентрации вблизи клеток эпителия • Усиление транспорта • Улучшение растворимости Защита от воздействия среды: – Микрокапсулирование – Гидрофобизация – Ингибирование ферментов Увеличение концентрации вблизи клеток эпителия кишечника – Использование мукоадгезивных носителей – Высвобождение в нужном отделе кишечника • Инкапсулирование • рН-зависимое высвобождение • Ферментзависимое высвобождение Усиление транспорта • Через мембрану эпителиальных клеток – Гидрофобные prodrugs – Использование ПАВ (желчных кислот – есть рецепторы на клетках эпителия) – Биоконъюгация с молекулами, имеющими переносчики (а.к., дипептиды, фолиевая кислота, желчные кислоты, В12 и др.) через мембрану эпителиальных клеток • Ориентация на поглощение М-клетками (включение в микро- и наночастицы) Улучшение растворимости солюбилизация • Комплексообразование с амфифильными полимерами (ПВП, ПЭГ) • Включение в состав микро- или наночастиц (липосомы, дендримерные соединения) • Получение наносуспензий (нанокристаллов) Биоконъюгация с веществами, имеющими переносчики • • • • В12 Желчные кислоты Бета-лактамные АБ Фолиевая кислота Еще одно преимущество: таким образом удается «обойти» Р-гликопротеин Биоконъюгация с желчными кислотами • Некоторые факты из «жизни» желчных кислот – – – – – – Секреция 600-800 мл/день Всего в человеке 1.5-4 г Циркуляция 17-40 г/день 6-15 циклов/день Потери 0.2-0.5 г/день (5%) Специфические рецепторы в печени и тонком кишечнике Желчные кислоты OH H3C H3C OH O OH H H O CH3 OH H HO HO NH CH3 CH3 CH3 O OH OH H O H3C OH NH CH3 CH3 O S O Кислоты рКа холевая 5 гликохолевая 3-4 таурохолевая 2.0 OH HO OH Желчные кислоты: SAR взаимодействия с рецепторами OH H3C O CH3 12 17 H CH3 H 3 HO OH H 7 OH H 1. Необходимы 2 или более гидроксильных групп 2. Необходим отрицательный заряд в районе С17 (два заряда – плохо) 3. Замещение в С3 не оказывает сильного влияния 4. Возможен отрицательный заряд около С3 5. Необходимо цис-сочленение колец А и В Применение конъюгатов с желчными кислотами: 1. Улучшение биодоступности при пероральном введении (улучшение всасывания в кишечнике) 2. Сайт-направленная доставка лекарственной субстанции в печень 3. Доставка лекарственной субстанции в желчный пузырь Примеры: улучшение биодоступности Препарат Гептапептид (ГП) Конъюгат ГП—спейсер—хол. кта Биодоступность 0.5% 7% Липосомы – наиболее продвинутый вид наночастиц, используемых в медицине Основные молекулы липосом – природные полярные липиды ORxn Rxn Фосфатидилхолин (ФХ) O Rxn O O P O O O Rxn Rxn X5 N(Me)3 Rxn O Фосфатидилэтаноламин (ФЭ) Фосфатидная кислота (ФК) NH3 H COOH NH3 Фосфатидилглицерин (ФГ) OH OH HO HO HO ORxn Rxn Rxn Rxn O Rxn Rxn O ORxn Rxn O Фосфатидилинозит (ФИ) O O P HORxnO OH HO O Rxn P O O Дифосфатидилглицерин (ДФГ) O Rxn Rxn O ORxn O Rxn Rxn OH OH O Rxn Rxn Фосфатидилсерин (ФС) Rxn O Rxn O O HO O HO OH OH Гликозилдиглицериды (ГД) Липосомы образуются самопроизвольно при гидратации полярных липидов H2O Гидрофобная поверхность; отсутствует только у замкнутых бислоев Липосома – модель биологических мембран Липиды в бислое могут перемещаться вдоль поверхности (латеральная диффузия); перескок между монослоями (флип-флоп) – более редкое событие; «покидание» бислоя возможно при контакте с другими клетками, липопротеидами или белками Форма молекулы Перевернутый конус Полиморфная фаза Форма образующихся агрегатов зависит от формы молекул липидов Мицеллярная Бислойная (L) Цилиндр Конус Сочетание нескольких типов молекул Гексагональная Кубическая (HII) (Q) Динамическая форма молекул некоторых амфифилов зависит от свойств окружающей среды ФлА2 Т - H+ Ca2+ + Фосфолипаза А2 отщепляет одну жирнокислотную цепь, что уменьшает объем гидрофобной области При нагревании увеличивается объем гидрофобной области При протонировании или в присутствии двухвалентных катионов уменьшается гидратация полярных головок, что приводит к уменьшению ее объема Т Термотропные фазовые переходы (полиморфные переходы) Получение липосом Липидная пленка (порошок) Гидратация Мультиламеллярные Лс Измельчение •Экструзия •УЗ Моноламеллярные Лс Загрузка полярных веществ Эффективность включения до 10%, зависит • от размера Лс, • концентрации Лс Соотношение активное вещество/носитель менее 0.01% Загрузка липофильных веществ Гидратация Эффективность включения около 100% Обычно включается до 10% мольн. от липидов мембраны Получение липосом «замещением растворителя» Спиртовой раствор липидов Вода 1) Смешение 2) Упаривание спирта Моноламеллярные Лс Активная загрузка Лс слабыми основаниями 1. Загружают соль слабого основания ((NH4)2SO4) 2. Добавляют активное вещество (доксорубицин, дофамин или другое слабое основание) 3. Происходит обмен активного вещества на аммиак Эффективность включения до 100% Дофамин: недостаток в мозгу приводит к болезни Паркинсона HO HO NH2 HO HO + NH3 Преимущества липосомных препаратов Эффект Накопление в сердце (доксорубицин) Липосомный препарат/р-р 1/2.3 LD50 (доксорубицин) 2.3 Накопление в опухоли (доксорубицин) 8.5 Концентрация в плазме (рифампицин дауномицин) Время выживания животных (доксорубицин) Равноэффективная доза (дауномицин, ДОФА) Увеличение растворимости (бетулиновая кислота) 3.3-185 2 1/10 1000 Основные причины использования липосомных препаратов Депонирование при местном введении Офтальмология Обработка раневых и ожоговых поверхностей Легочные инфекции Нацеливание в клетки РЭС Грибковые и бактериальные внутриклеточные инфекции Вакцины Нацеливание в области воспаления: долгоциркулирующие липосомы Противоопухолевые препараты Инфекции Основные сферы использования липосомных препаратов • Противоопухолевые • Лечение грибковых и бактериальных внутриклеточных инфекций • Вакцины Сферы использования липосомных препаратов Противоопухолевые Субстанция Название Доксорубицин D99 Заболевание Фирма Рак молочной железы The Liposome Co. Саркома Капоши, рак молочной железы, SEQUUS Doxil простаты, первичный Pharmaceuticals рак печени Саркома Капоши, рак NeXstar Дауномицин DaunoXome молочной железы и др. Pharmaceuticals солидные опухоли Доксорубицин (Stealth liposomes) Антрациклиновые антибиотики OH O OH OH O OH O O OH OH H O O OH O H3C O H3C O O O Доксорубицин, эпирубицин OH O OH CH3 CH3 NH2 NH2 OH O OH CH3 OH O OH O O OH O O OH O H3C O O Дауномицин, пирорубицин OH O OH H3C O O O CH3 CH3 OH O NH2 NH2 Сферы использования липосомных препаратов Грибковые и бактериальные внутриклеточные инфекции Субстанция Название Заболевание Фирма Системные грибковые NeXstar Амфотерицин В AmBiosome инфекции, Pharmaceuticals лейшманиозы Системные грибковые Амфотерицин В ABCL The Liposome Co инфекции Системные грибковые Амфотерицин В Amphocil SEQUUS инфекции Серьезные Амикацин MiKasome бактериальные NeXstar инфекции Амфотерицин B и амикацин OH OH O H3C OH O HO OH OH OH OH O O CH3 OH H3C O OH O HO NH2 H2N O HO HO HO O OH OH HO O H2N O H2N NH OH HO O H H2N CH3 Образует комплекс с цитостерином, что приводит к образованию пор в мембране грибов Сферы использования липосомных препаратов Вакцины Субстанция Название Заболевание Фирма Инактивиров. Epaxal-Berna Swiss Serum and вирионы Гепатит А vaccine Vaccine Inst. гепатита А Белки из Trivalent Swiss Serum and вирионов трех influenza Грипп Vaccine Inst штаммов vaccine E.coli 0157:H7 E.coli 0157:H7 E.coli 0157 Novavax (killed) vaccine (oral) инфекция Shigella S. flexnery 2A Shigella flexnery 2A flexnery 2A Novavax (killed) инфекция vaccine (oral) Модификации поверхности липосом НИОТ Загружаемый препарат ddC d4T Модификация липосом Цель модификации Увеличение заряда на поверхности Направленная доставка в макрофагоподобные клетки Введение на поверхность Направленная доставка в стеариламина для увеличения макрофаги и моноциты заряда AZT конъюгаты Ацетилирование поверхности (холестериновых молекул) Направленная доставка в клетки J7774.A и U937 AZT Увеличение положительного заряда стериламином Доставка в клетки печени d4T Конъюгирование поверхности с маннозой Доставка в клетки MT2 d4T Конъюгирование поверхности с галактозой Доставка в клетки печени Дендримеры – разветвленные полимеры • Синтезируются ступенчато, образуя дендримеры соответствующего поколения • Как правило, имеют сферическую форму • Имеют полости, куда могут включаться молекулы лекарственных веществ • Поверхностные группы могут использоваться для ковалентного присоединения модифицирующих молекул • Дендримеры с аминогруппами – удобные переносчики ДНК для генной терапии Структура дендримера на основе аминокислот (полиамидо -амин, PAMAM) Сравнительные размеры дендримеров, белков и некоторых надмолекулярных комплексов Дендримеры на основе пропилендиамина – эффективные агенты для трансфекции Молекулярные модели связывания ДНК с денримерами 1-5 генераций Вид сбоку Вид сверху Ковалентные модификации НИОТ . Prodrugs Динуклеозидтетрафосфаты Противоопухолевый конъюгат хитозана Эффективным является использование природного полимера хитозана для доставки лекарственных препаратов. Хитозан – линейный полисахарид, состоящий в основном из остатков аминоглюкозы. R=R1=AZT Увеличение биодоступности Использование пептидных транспортеров Ингибирование фермента Биоимитация, липидная стратегия Фармакологически активное соединение Липид Фармакологически активное соединение Фармакологически активное соединение Липид + Липид Фармакологически активное соединение Примеры липофильных матриц и нуклеозидных противовирусных средств, на основе которых были синтезированы пролекарственные соединения Структура липофильной части молекулы O R O R Drug-C(O)O R = ЖК R2O OR1 O O P X Drug O Лекарственные соединения (Drug); жирные кислоты (R) 1. Хлорамбуцил; ЖК: 2 С16 2. L-ДОФА; ЖК: 2 С16 3. Фенитоин; ЖК: 2 С14 4. AZT; ЖК: С16, С18:1 5. ddI; спейсер: Glu; ЖК: 2 C16 6. ddI MP; спейсер: hex; ЖК: 2 C16 7. Напроксен; ЖК: 2 С16 8. Аспирин и другие НПВС; ЖК: 2 (С2 – С16) 9. Saq или Ind; спейсер: Suc; ЖК : 2 C15 10. Iva-Phe-Nle-Sta-Ala-Sta; спейсер: Glu; ЖК : 2 C15 11. NFX, ЖК 2 С16 12. Ибупрофен, ЖК 2 С16; ЖК 2 С18 1. 1-β-D-Арабинофуранозилцитозин и цитидин; R1 = S-(C16, C18), R2 = C1, C2 ,C16, X = PO2O 2. AZT и ddI; R1 = NHCO-C17, O-C16, S-C16, R2 = C1, C2, X = O 3. Гемцитабин; X = О, R1 = S-C12, R2 = C10 4. Гемцитабин; X = спейсер: Suc; кардиолипин 5. 5-Фторуридин; X = О, R1 = C16, R2 = H, C16, C18:2, C2 0:4 Пронуклеотидный подход