ВАРИАНТ номера заданий 1
advertisement
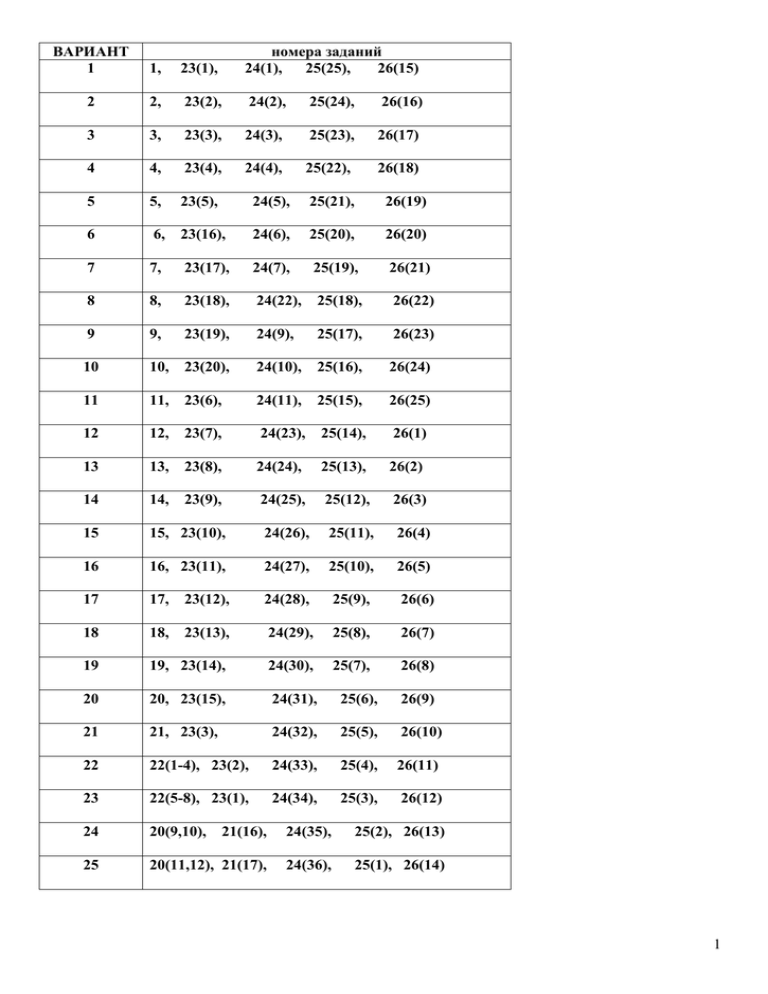
ВАРИАНТ 1 1, 23(1), номера заданий 24(1), 25(25), 26(15) 2 2, 23(2), 24(2), 25(24), 26(16) 3 3, 23(3), 24(3), 25(23), 26(17) 4 4, 23(4), 24(4), 25(22), 26(18) 5 5, 23(5), 24(5), 25(21), 26(19) 6 6, 23(16), 24(6), 25(20), 26(20) 7 7, 23(17), 24(7), 25(19), 26(21) 8 8, 23(18), 24(22), 25(18), 26(22) 9 9, 23(19), 24(9), 25(17), 26(23) 10 10, 23(20), 24(10), 25(16), 26(24) 11 11, 23(6), 24(11), 25(15), 26(25) 12 12, 23(7), 24(23), 25(14), 26(1) 13 13, 23(8), 24(24), 25(13), 26(2) 14 14, 23(9), 24(25), 25(12), 26(3) 15 15, 23(10), 24(26), 25(11), 26(4) 16 16, 23(11), 24(27), 25(10), 26(5) 17 17, 23(12), 24(28), 25(9), 26(6) 18 18, 23(13), 24(29), 25(8), 26(7) 19 19, 23(14), 24(30), 25(7), 26(8) 20 20, 23(15), 24(31), 25(6), 26(9) 21 21, 23(3), 24(32), 25(5), 26(10) 22 22(1-4), 23(2), 24(33), 25(4), 26(11) 23 22(5-8), 23(1), 24(34), 25(3), 26(12) 24 20(9,10), 21(16), 24(35), 25(2), 26(13) 25 20(11,12), 21(17), 24(36), 25(1), 26(14) 1 ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОЙ РАБОТЫ Тема: ОСНОВНЫЕ КЛАССЫ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 1. Закончить уравнения реакций, назвать исходные и конечные вещества BaO + H2O = CrO3 + H2O = Na2O + HNO3 = Zn(OH)2 + KOH = Al2(SO4)3 + KOH = 2. Какие из перечисленных оксидов будут реагировать с CO2,: K2O, NO2, Mn2O7, Cr2O3, N2O5? Напишите уравнения реакций. 3. Какие из указанных газов вступают в химическое взаимодействие с раствором щелочи: HCl, H2S, NO2, N2, Cl2, CH4, SO2, NH3? Написать уравнения соответствующих реакций. 4. Написать и назвать продукты полной и неполной нейтрализации по систематической номенклатуре для уравнения: Cu(OH)2 + H2SO4 → 5. С какими из перечисленных ниже веществ будет реагировать соляная кислота: B2O3, Zn(OH)2, CaO, AgNO3, SiO2, H3PO4? Составить уравнения соответствующих реакций. 6. Какие из указанных веществ реагируют с гидроксидом натрия: HNO3, CaO, CO2, CuSO4, Cd(OH)2, P2O5? Составить уравнения реакций. 7. Написать уравнения реакций образования Ca3(PO4)2, Mg(ClO4)2, Ba(NO3)2 в результате взаимодействия: а) основного и кислотного оксида; б) основания и кислотного оксида; в) основного оксида и кислоты; г) основания и кислоты. 8. С какими из перечисленных веществ взаимодействует соляная кислота: MgO, N2O3, AgNO3, SO3, Pb(NO3)2, CuSO4, FeS, FeO, Cu, Zn? Составить уравнения реакций. 9. Напишите уравнения реакций, при помощи которых перечисленные ниже соли могут быть переведены в средние: (CuOH)2SO4, Ca(HCO3)2, 2 [Al(OH)2]2SO4, [Cr(OH)2]2SO3, (BiOH)2SeO4. 10. Получите кислые, основную и среднюю соли, изменяя соотношения молей реагирующих веществ по реакции Cа(OH)2 + H3PO4 11. Получите кислую, основные и среднюю соли, изменяя соотношения молей реагирующих веществ по реакции Al(OH)3 + H2SO4 12. Какие из перечисленных веществ взаимодействуют с оксидом бария: CO2, NaOH, P2O5, HNO3, Na2O, H2O, SiO2? Напишите уравнения реакций. 13.Какие из перечисленных веществ реагируют с серной кислотой: CuO, MgCl2, Al2O3, Be(OH)2, CO2, Mn2O7? Напишите уравнения реакций. 14. Какие из оксидов (CO2, Na2O, TeO3, SiO2, Al2O3) способны к солеобразованию с основаниями? Составьте уравнения реакций взаимодействия их с гидроксидом кальция. 15. Какие из оксидов (N2O3, MgO, SiO2, P2O5, BeO) способны к солеобразованию с основаниями? Составьте уравнения реакций взаимодействия их с гидроксидом бария. 16. Составьте уравнения реакций неполной нейтрализации, в результате которых образуются соли: Ba(HSO3)2 и CrOH(NO3)2. 17. Составьте уравнения реакций, с помощью которых можно превратить следующие кислые и основные соли в средние: KHCO3, (ZnOH)2SO4, CrOHCl2, Na2HPO4. 18. Напишите уравнения реакций взаимодействия гидроксида железа (III) с хлороводородной кислотой, при которых образуются следующие соединения: дигидроксохлорид железа (III), гидроксохлорид железа (III), хлорид железа (III). 19. С какими из перечисленных веществ будет реагировать бромоводородная кислота: AgNO3, CO2, Mg, CuO, Ca(OH)2, P2O5? Напишите уравнения реакций. 20. Составьте уравнения реакций разложения гидроксида серебра (I), гидроксида железа (III), гидроксида меди (II), карбоната кальция, нитрата серебра. 21.Изменяя соотношения молей реагирующих веществ по реакции Ca(OH)2 + H3AsO3 получите кислые, основную и среднюю соли. 22. Составьте уравнения реакций получения всеми возможными способами следующих солей: 3 1) сульфат меди (II); 2) карбонат кальция; 3) силикат натрия; 4) хлорид кальция; 5) сульфид железа (II); 6) фосфат калия; 7) нитрат алюминия; 8) карбонат калия; 9) силикат натрия; 10) бромид калия; 11) сульфат цинка; 12) сульфид натрия; 13) хлорид алюминия. 23. Докажите амфотерные свойства: 1) Al2O3; 2) SnO; 3) Cr2O3; 4) BeO; 5) ZnO; 6) MnO2; 7) PbO2; 8) PbO; 9) SnO2; 10) Cr(OH)3; 11) Mn(OH)4; 12) Zn(OH)2; 13) As(OH)3; 14) Be(OH)2; 15) Sn(OH)4; 16) Sn(OH)2; 17) Pb(OH)2; 18) Pb(OH)4; 19) Sb(OH)3; 20) Al(OH)3. 24. Назовите следующие соединения, укажите к какому классу они относятся: 1) NO, Al2O3, H2SeO4, Mn(OH)2, FeOHNO3, Ca(H2PO4)2 2) Cs2O, N2O3, NH4OH, H2S, K3PO4, Pb(HSO3)2, Cr(OH)2Cl 3) SnO, Mn2O7, CH3COOH, Ag2CrO4, (Fe(OH)2)2SO4, NaHSiO3 4) SO3, FeO, H2SiO3, Cu(OH)2, NH4NO3, Cr(HSO4)3, (CuOH)2CO3 5) Ag2O, CrO3, Bi(OH)3, HF, MgHPO4, Hg(NO3)2, NiOHBr 6) P2O3, CuO, CH3COOH, Mn(OH)2, NH4F, Zn(HSO4)2, (SnOH)3PO4 7) Bi2O3, Mn2O7, H3PO4, Fe(OH)2, K2CrO4, Na H2PO4 , (Al(OH)2)SO4 8) Fe(HPbO3)2, Al2(SO4)3, (CaOH)2CrO4, K3[Fe(CN)6], NO2, As(OH)3 9. KAl(SO4)2, Na2BeO2, (CuOH)2S, BaHAsO4, H3PO3, SiO2 10. (ZnOH)2SO4, Sr(ClO4)2, Fe(HPbO3)2, NaAlO2, N2O5, Be(OH)2 11. K3CrO3, KAl(SO4)2, (MnOH)2SO4, Ca(H2SbO3)2, CO2, H3AsO4 12. BaOHNO3, Ca3(PO4)2, Cu(HS)2, KMnO4, [Cd(NH3)4](ClO4)2, H4SiO4 13. ZnHPO4, HgCl2, (CuOH)2CO3, H3AsO3, K[Ag(NO2)2], Al2O3 14. Al2(SO4)3, (ZnOH)3PO4, NaHSnO3, K2ZnO2, [Ag(NH3)2]NO3, MgO 15. Al(OH)3, Mg(HCrO4)2, CaOHNO3, Al2Se3, [Ag(NH3)2]Cl, H2BeO2 16. FeOHTeO4, SrHPO4, Mg3(SbO4)2, Co(OH)2, K2[Ni(CN)4], Na2O 17. CaSiO3, AlOHSO3, HClO3, ZnHSbO4, Na2[Cd(CN)4], SO3 18. CaHPO4, K2Se, FeOHCO3, HI, K[Al(OH)4], Cu(OH)2 19. K2PbO3, Ca(H2AsO4)2, (CuOH)2CO3, HNO2, Na3[AlF6], P2O7 20. MgOHI, K2CO3, AlOHSnO3, Zn(HSeO4)2, [Ni(NH3)4]Br2, SiO 21. Al2S3, (CdOH)2CO3, H2 Cr2O7, K2HPO4, K[AgI2], CO 22. H3AlO3, CuOHBr, CaTe, Zn(H2AsO4)2, Fe(OH)3, BeO 4 23. Ca(HCrO4)2, MgSiO3, CuOHNO2, (PbOH)2SO3, Cs2O, HPO3 24. Al(OH)2NO3, HBr, Cu(HSO3)2, Ba3(AsO4)2, Ba(OH)2, CaO 25. Ca(HSe)2, K3SbO3, H2SO3, AlOH(NO2)2, Cr(OH)3 , NO 26. K2Cr2O7, KH2PO4, (MnOH)2Se, KNaCO3, H2Te, Fe(OH)2 27. Ba3(PO4)2, Ca(HSO4)2, (CuOH)2CO3, HCrO2, Zn(OH)2, SrO 28. KMnO4, PbOHI, Ba(HS)2, HAlO2, CrO3, Sn(OH)4 29. Na2SnO3, CoOHCl, H2CrO4, NaHTeO4, As(OH)3, Cu2O 30. K2CrO4, NaHSnO3, HNO2, PbOHCl, Na2O, Al(OH)3 31. (ZnOH)2SO3, Fe(CrO2)2, CaHPO4, KNaCO3, NH4OH, H2Te 32. NaClO4, Cr(OH)3, Al(OH)22 SiO3, Ca(HCO3)2, HCN, NO2 33. Na2ZnO2, Ba(HCO3)2, AlOHCl2, KCr(SO4)2, Cr2O3, H3BO3 34. KHS, KAl(SO4)2, Hg(NO3)2, (CdOH)3AsO4, Fe(OH)3, Mn2O7 35. Cu(HSO3)2, Al(OH)2NO2, H3IO3, Al2(CO3)3, Cu(OH)2, Ag2O 36. FeOHTeO4, SrHPO4, Mg3(SbO4)2, Co(OH)2, Ni(OH)2, H3PO4 25. Запишите формулы соединений: 1) оксид золота (I), оксид,брома (III), гидроксид марганца (II), метакремневая кислота, нитрат гидроксомеди (II), ортофосфат кальция, 2) оксид бора, оксид алюминия, гидроксид меди (II), уксусная кислота, дигидрофосфат аммония, нитрат висмута, хлорид дигидроксохрома 3) оксид магния, оксид углерода (II), фтороводородная кислота (плавиковая), гидроксид кобальта (II), иодид кальция, гидросульфид бария, нитрат дигидроксожелеза 4) оксид ванадия (V), оксид кремния (IV), гидроксид олова (IV), азотистая кислота, сульфид меди (II), дигидрофосфат калия, сульфат дигидроксохрома 5) оксид марганца (VII), оксид азота (II), азотная кислота, гидроксид аммония, фосфат магния, гидрокарбонат бария, хлорид гидроксожелеза (III) 6) оксид калия, оксид углерода (IV), ортомышьяковая кислота, гидроксид цинка, карбонат лития, дигидроортофосфат меди (II), ортоарсенат гидроксоцинка; 7) оксид железа (II), оксид азота (IV), ортосурьмяная кислота, гидроксид кадмия (II), теллурид калия, дигидроортофосфат кальция, сульфат гидроксостронция; 5 8) оксид цезия, оксид фосфора (V), селеноводородная кислота, гидроксид магния, хромат алюминия, метасиликат гидроксокальция, дигидроортостаннат натрия; 9) оксид кальция, оксид кремния (II), двухромовая кислота, гидроксид олова (II), карбонат висмута (III), гидроортоарсенит магния, сульфид гидроксокальция; 10) оксид бария, оксид свинца (IV), марганцовистая кислота, гидроксид рубидия, сульфат калия – хрома (III), метасиликат гидроксокальция, гидротеллурид магния; 11) оксид лития, оксид серы (IV), метасвинцовая,кислота, гидроксид сурьмы (III), хлорид мышьяка (III), нитрит гидроксоалюминия, гидрометасиликат кальция; 12) оксид цинка, оксид азота (I), йодоводородная кислота, гидроксид свинца (II), бериллат калия, гидроортоарсенит калия, сульфат дигидроксожелеза (III); 13) оксид натрия, оксид азота (V), ортоборная кислота, гидроксид свинца (IV), гипохлорит натрия, ортостибат гидроксомагния, гидрохромат стронция; 14) оксид железа (III), оксид бериллия, селенистая кислота, гидроксид мышьяка, ортоплюмбат меди (II), гидросульфит железа (II), карбонат гидроксомагния; 15) оксид германия (IV), оксид фосфора (III), молибденовая кислота, гидроксид кобальта (III), сульфат калия - алюминия, ортосиликат гидроксокальция, гидротеллурит магния; 16) оксид циркония, оксид марганца (IV), хромовая кислота, гидроксид ванадия (III), перхлорат натрия, гидрокарбонат кальция, сульфит гидроксомагния; 17) оксид ванадия (III), оксид серы (VI), ортокремниевая кислота, гидроксид калия, хлорат цинка, хромат гидроксокальция, гидроортостибит калия; 18) оксид марганца (III), оксид кобальта (II), метамышьяковая кислота, гидроксид висмута (III), карбонат хрома (III), дигидроортофосфат алюминия, сульфид гидроксоалюминия; 19) оксид титана (IV), оксид галлия (III), теллуристая кислота, гидроксид таллия (I), метахромит железа (II), сульфат калия-хрома (III), ортоплюмбат гидроксобария; 20) оксид марганца (II), оксид мышьяка (III), йодноватая кислота, гидроксид галлия (III), сульфат висмута (III), метастаннат гидроксокальция, дигидроортоарсенат алюминия; 21) оксид хрома (II), оксид таллия (I), метависмутовая кислота, гидроксид 6 кадмия (II), ортофосфат бария, дигидроортоарсенат калия, нитрит дигидроксоалюминия; 22) оксид индия (III), оксид азота (IV), метафосфористая кислота, гидроксид аммония, сульфат олова (II), йодат гидроксожелеза (III), гидроортоарсенат бария. 23) оксид ртути (II), оксид азота (II), свинцовистая кислота, гидроксид индия (III), гипохлорит кальция, дигидроортостаннат бария, ортоарсенат гидроксостронция; 24) оксид платины (IV), оксид галлия (III), сернистая кислота, гидроксид кальция, ортоалюминат натрия, селенит дигидроксохрома (III), гидросульфид меди (II); 25) оксид кобальта (III), оксид серебра (I), гидроксид алюминия, метахромистая кислота, сульфат алюминия, метасиликат гидроксомеди (II), дигидроортостаннат калия; 26. Запишите уравнения реакций с помощью которых можно осуществить следующие превращения: 1) SSO2H2SO3КHSO3К2SO3 2) BaOBa(OH)2BaOHClBaCl2 3) P2O5H3PO4LiH2PO4Li2HPO4Li3PO4 4) K2OKOHKH2PO4K2HPO4K3PO4 5) AlAl2O3Al(NO3)3Al(OH)3Na3AlO3 6) SSO3H2SO4CsHSO4Cs2SO4 7) ZnZnOZnCl2Zn(OH)2ZnOHNO3Zn(NO3)2 8) BeBeOBe(NO3)2Be(OH)2K2[Be(OH)4] 9) KClО3 → О2 → Р2О5; б) KMnO4 → О2 → Fe3O4 10) Ca → CaO → Ca(OH)2 → Ca(NO3)2 ↓ Ca(OH)2 11) Na2O → NaOH → Cu(OH)2 → (CuOH)2SO4 → CuSO4 ↓ NaCl 12) Ba → BaO → Ba(OH)2 ↓ 7 Ba(OH)2 → BaO 13) Na → NaOH → NaHCO3 → Na2CO3 → Na2SO4 14) Cu → CuO → CuCl2 → Cu(OH)2 →Cu(OH)NO3 15. CuO → CuSO4 → Cu → CuO → Cu(NO3)2 16. Li → Li2O → LiOH → Li H2PO4 → Li3PO4 ↓ Li NO3 17. Р2О5 → H3PO4 → Са3(РО4)2 → H3PO4 → Са(Н2РО4)2 18. Al2(SO4)3 → Al(OH)3 → Al2O3 → AlCl3 → Al(OH)3 19. Sb → SbCl2 →SbOHCl → Sb(OH)2 →Sb(NO3)2 20. FeCl2 → Fe(OH)2 → (FeOH)2SO4 → FeSO4 → Fe → FeCl2 21. P → P2O5 →H3PO4 → Na3PO4 → Ca3(PO4)2. 22. FeCl2 → Fe → FeCl3 → Fe(OH)3 → FeOHSO4 → Fe2(SO4)3 K2[Zn(OH)4] 23. Zn ZnO ZnCl2 Zn(OH)2 ZnCl2 24. Fe FeCl2 FeS H2S NaHS Na2S Cr(NO3)3 Cr2O3 25. Cr CrCl3 Cr(OH)3 K3[Cr(OH)6] 8
