СИНДРОМ СМЕШАННОЙ КРИОГЛОБУЛИНЕМИИ Обзор литературы Баймурынова А. Ж., Курманова Г.М.
advertisement
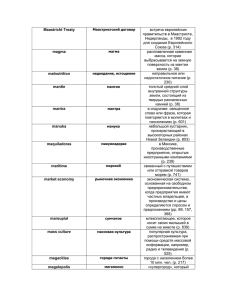
СИНДРОМ СМЕШАННОЙ КРИОГЛОБУЛИНЕМИИ Обзор литературы Баймурынова А. Ж., Курманова Г.М. Казахский Национальный медицинский университет им. С.Д. Асфендиярова Под криоглобулинемией понимают наличие в сыворотке иммуноглобулинов, выпадающих в осадок при низкой температуре и вновь растворяющихся при 37°С. Эти иммуноглобулины, которые принято называть кри-оглобулинами, образуют комплексы с другими иммуноглобулинами и белками. Криоглобулин в сочетании с пурпурой как проявление самостоятельного заболевания был впервые опи-сан Лернером и Уотсоном в 1947 г. [1]. В 1974 г. Бруэ и соавторы [2] предложили классификацию криоглобу-линемий по трем типам криоглобулинов (табл. 1) Таблица 1. Классификация криоглобулинов по Bruet и соавт. [2] Криоглобулины Тип I. Моноклональные криоглобулины (IgM, IgG, IgA, легкие цепи — белок Бенс-Джонса). Чаще всего встречаются при: миеломная болезнь, макроглобулинемия Вальденстрема, лимфопролиферативные заболева-ния, например хронический лимфолейкоз. Проявления: поражение кожи, ангиотрофоневрозы (в том числе ган-грена кончиков пальцев), поражение нервной системы. Редко вызывает поражение почек. Тип III. Поликлональные криоглобулины: образуют криопреципитат с поликлональны-ми IgG и неимму-ноглобулиновыми компонентами сыворотки (компонентами комплемента, липопротеидами и другими). Воз-можно, криопреципитат образуют не сами иммуноглобулины, а иммунные комплексы. Проявления: пальпи-руемая пурпура, синдром Рейно, поражение почек и нервной системы. Поликлональная криоглобулинемия: аутоиммунные заболевания: СКВ, РА, УП, б. Шегрена, ССД, Шен-лейн-Геноха, б.Бехчета, полимиозит, тиреоидит, реже при различных инфекционных заболеваниях, например гепатит В, гепатит С, инфекционный мононуклеоз, цитомегаловирусная инфекция, инфекционный эндокардит, проказа, сифилис, инфекции, вызванные стрептококками группы А. Наибольшее клиническое значение имеет смешанная криоглобулинемия (тип II). Смешанная криоглобулинемия Тип II. Смешанные криоглобулины: состоят из двух иммуноглобулинов, из 1-го моноклонального иммуноглобулина в роли антитела, (традиционно IgM (содержащий преимущественно один тип лѐгких цепей — к), реже IgA либо G), соединенного с поликлональным IgG. В последние годы установлено, что самым распро-страненным сочетанием при криоглобулинемии II типа является комплекс моноклональный IgM + поликло-нальный IgG, в котором IgM представляет собой анти – IgG (ревматоидный фактор). Взаимодействие этих ком-понентов при низкой температуре сопровождается выпадением их в осадок. Смешанная криоглобулинемия — особый тип системного васкулита мелких сосудов, характеризующийся отложением в стенке сосудов криоглобулинов и наиболее часто проявляющийся поражением кожи в виде пур-пуры и клубочков почек. Криоглобулины — сывороточные иммуноглобулины, обладающие свойством обратимой холодовой пре-ципитации. Смешанная криоглобулинемия II типа может развиваться при целом ряде инфекционных и аутоиммунных заболеваний, и в этом случае еѐ называют вторичной смешанной криоглобулинемией. До недавнего времени примерно у 30% пациентов не удавалось установить связь криоглобулинемии с другой патологией, что привело к появлению термина «эссенциальная криоглобулинемия». Эссенциальная криоглобулинемия была описана М. Meltzer в 1966 г. как синдром, включающий общую слабость, пурпуру, артралгии (триада Мельтцера) в сочета-нии с криоглобулинемией II типа. В настоящее время термин «эссенциальная криоглобулинемия» следует счи-тать условным, поскольку в генезе смешанной криоглобулинемии чѐтко установлена ключевая роль вирусных инфекций. Этиология В начале 90 годов было установлено, что «эссенциальная» смешанная криолобулинемия часто наблюда-ется при HCV-инфекции, что позволило предположить патогенетическую роль HCV при этом заболевании [3,4,5-7]. Оказалось, что HCV является не только гепатотропным, но и лимфотропным вирусом, способным ин-фицировать до 80% мононуклеаров периферической крови [3,18]. Была обнаружена связь лимфотропизма с пролиферацией В-клеток, продукцией криоглобулинов и с образованием аутоантител [8, 9,10]. В настоящее время является точно установленным, что в подавляющем большинстве случаев криоглобулинемия ассоциирована с HCV, а роль других вирусов (Эпштейна-Барр, гепатитов А и В) менее значима. У па-циентов, инфицированных HCV, частота выявления криоглобулинемии варьирует от 34% до 54%. При смешан-ной криоглобулинемии маркѐры инфекции HCV в крови обнаруживают в 63-76% случаев, а в криопреципита-тах — в 75-99% случаев. HCV-РНК была найдена методом ПЦР не только в сыворотке больных криоглобули-немией, но и в высоко концентрированной форме в криопреципитатах [9,11]. Даже при вторичной криоглобулинемии, ассоциированной с аутоиммунными заболеваниями, нельзя ис-ключить тот факт, что триггер-фактором может быть вирус HCV. Для данного вируса доказано участие в пато-генезе многих аутоиммунных заболеваний, а при ряде других – обсуждается его возможная этиологическая роль. Патогенез В основе патогенеза синдрома смешанной криоглобулинемии лежит синдром поликлональной активации. Core-протеин HCV, обладает характеристиками суперантигена, а как суперантиген он способен вызывать не-специфическую пролиферацию различных клонов В-лимфоцитов, в том числе продуцирующего поликлональ-ный (IgM) или моноклональный (IgMK) ревматоидный фактор. Суперантигены способны вызвать поликло-нальную пролиферацию ИКК в 100 раз большую, чем специфическая клональная пролиферации в ходе нор-мального иммунного ответа на тот или иной антиген [5, 7, 8]. Связывание РФ в крови или in situ с IgG (при инфекции HCV IgG проявляет свойства AT к HCV) приво-дит к образованию криопреципитатов II типа, отложение которых в стенке мелких сосудов, в том числе и в ка-пиллярах клубочков, сопровождается потреблением компонентов комплемента, индуцируя повреждение сосу-дистой стенки и развитие воспаления. Оказалось, что моноклональный IgM (ревматоидный фактор) смешанных криоглобулинов обладает способностью связываться с фибронектином мезангиального матрикса клубочков, чем и объясняют высокую нефритогенность криоглобулинов II типа. Поражение почек отмечают и при III типе криоглобулинемии, однако при II типе — в 3 раза чаще. В отличие от III типа, при котором почечные проявле-ния неспецифичны, при II типе с моноклональным IgM развивается ГН с особыми морфологическими призна-ками, позволяющими рассматривать его как отдельный вариант гломерулонефрита — криоглобулинемический. Как следствие поликлональной Вклеточной активации, отложение циркулирующих криопреципити-рующих комплексов ведет к развитию васкулита вследствие активации системы комплемента через IgG1 и IgG3 компоненты ИК с участием криоглобулинов [3,4,8]. Известно, что IgG1 и IgG3 являются основными подклас-сами IgG в криопреципитатах, наиболее эффективно инициирующими классический путь активации компле-мента [11], что и ведет к гипокомплементемии. До сих пор нет информации о том, насколько частота и тяжесть проявлений HCV-ассоциированных васкулитов отличается при различных генотипах HCV. В отношении гепатита, однако, показано, что генотип 1b вызывает более тяжелые гистологические изменения и отличается резистентностью к терапии интерфероном [3, 11, 12]. В литературе имеется единственная публикация, в которой сообщается о преобладании смешанной криоглобулинемии при подтипе 2а [8]. Патоморфология По данным недавнего обзора гистологических исследований чаще всего при синдроме смешанной криог-лобулинемии наблюдается экссудативный мембранопролиферативный гломерулонефрит (МПГН) I типа. Неко-торыми авторами он определяется как «криоглобулинемический васкулит», поскольку гломерулярные повреж-дения отличаются от тех, которые можно видеть при идиопатическом МПГН или при диффузном пролиферативном ГН, ассоциированном с СКВ. «Интралюминальные тромбы» из аморфного, эозинофильного, PASпозитивного вещества, содержащего IgG или IgM, как показывает иммуногистология, обнаруживаются более чем у трети всех больных. Было показано, что депозиты идентичны с циркулирующим криоглобулином (задер-живающимся локально или преципитированном), однако определение вирусного генома в биоптате представ-ляется очень сложным [13]. Картина умеренной сегментарной мезангиальной пролиферации, недостаточно ти-пичная для криоглобулинемического ГН, обнаруживается в 10% случаев [13], но она выявляется также и у больных со смешанной криоглобулинемией при доказанном HCV. С другой стороны, до сих пор не достигнуто согласия по вопросу о существовании и частоте HCVассоциированного некриоглобулинемического ГН [3,14]. Моноклональный IgM-ревматоидный фактор (IgМRF), возможно, играет существенную роль в возникновении гломерулярного заболевания. Это было недавно показано в эксперименте, на животных, у которых IgM-RF, изолированный от смешанных криоглобулинов, откладывался в клубочках. Этот процесс может быть опосредо-ван связыванием с фибронектином, как было показано для IgM-RF, но не для других моноклональных и поли-клональных IgM. Напротив, IgG антитела могут перекрестно реагировать с гломерулярными антигенами [3,14,9,15]. Клинические проявления Самым частым проявлением криоглобулинемии является поражение кожи. Поражение кожи наблюдается практически у всех больных, страдающих криоглобулинемией, и часто является поводом для обращения к вра-чу. Иммунокомплексные васкулиты с поражением мелких и средних сосудов могут возникать у 20-30% боль-ных с HCV-ассоциированной криоглобулинемией [16]. Кожные проявления HCV-инфекции неспецифичны и разнообразны [16,3,20]. Они не ограничиваются классической пурпурой или уртикарным васкулитом, локали-зующимся обычно на коже конечностей, когда низкая температура вызывает активацию комплемента [4,17,21]. Дальнейшими клиническими последствиями HCV-инфекции являются периферическая нейропатия, су-хой синдром (Шегрена), аутоиммунный тиреоидит, аутоиммунная тромбоцитопеническая пурпура и аутоиммунный гепатит II типа с LKM 1-антителами [8,9,14]. Поражение почек чаще развивается при смешанной криоглобулинемии, варьируя по степени тяжести от изолированного мочевого синдрома (протеинурия с микрогематурией) до острого нефритического синдрома. Описаны случаи возникновения нефротического синдрома с постепенным переходом в хроническую почечную недостаточность. Прогноз заболевания в большей степени определяет наличие поражения почек. В первые 7 лет после начала заболевания умирает около 70% больных с поражением почек и 31% больных с интактными почками. Клинически вовлечение почек при любой форме иммунокомплексного васкулита имеет огромное зна-чение [13]. Клинические симптомы или изменение биохимических показателей, свидетельствующие о нарушении функции печени, имеются только у 50-84 % больных, страдающих смешанной криоглобулинемией, то есть у большого пула больных при наличии HCVинфекции, гепатит протекает с нормальным уровнем трансаминаз. Артралгия и артрит появляется уже на ранних стадиях заболевания. Артралгия – мигрирующая и затра-гивает крупные и средние суставы. Артрит как правило недеструктивный и обусловлен отложениями циркули-рующих иммунных комплексов. Артрит у больного может быть не только в следствии синдрома смешанной криоглобулинеии, но протекать и в рамках суставного синдрома, сопутствующего ХВГ В или С. При смешанной криоглобулинемии нередко поражаются легкие, однако это обычно не диагностируется. Поражение легких носит двусторонний характер и проявляться пульмонитом и фиброзирующим альвеолитом. Часто больного ведут как больного пневмонией, но при этом антибактериальная терапия оказывается неэффек-тивной. Измерение параметров функции внешнего дыхания часто полезно для выявления поражения дистальных отделов воздухопроводящих путей. В лабораторных показаниях наблюдаются анемия, гипергаммаглобулинемия, ревматоидный фактор об-наруживается у 92% больных, у 70% - повышение СОЭ, снижение С3, С4, СН50; гематурия, пиурия, протеину-рия, азотемия, повышение активности трансаминаз (50%). Диагностика Клинические критерии диагностики криоглобулинемии (Monti и соавт. 1995): Наличие более 2-ух признаков из триады Мельтцера (геморрагическая пурпура, слабость, арт-ралгия); Системность поражения: кожные проявления, поражение почек, печени и наличие перифериче-ской нейропатии (позволяет оценить степень прогрессирования васкулита); Обнаружение криоглобулинов - уровень криокрита (отношение криопреципитата к объему плаз-мы) более 1%, что выявляется в течение более 6 месяцев; Положительный ревматоидный фактор в сыворотке крови; Низкий уровень С4-компонента комплемента в сыворотке крови (наименее 8 мг/мл); Исследование крови на маркеры вируса гепатита В и С, ПЦР на HCV РНК, при отрицательном результате – исследование на другие инфекции, способные вызвать синдром; Исключение вторичной криоглобулинемии (на фоне аутоиммунных заболеваний). В общем анализе крови почти у всех больных с продолжительно текущим криоглобулинемическим васкулитом отмечается нормоцитарная нормохромная анемия. Часто при использовании автоматических устройств для подсчѐта форменных элементов крови встречается псевдолейкоцитоз и псевдотромбоцитоз. Это свя-зано с тем, что криоглобулины образуют большие преципитаты, ложно регистрируемые как лейкоциты и тром-боциты. При микроскопии мазка крови время от времени в нейтрофилах обнаруживают множественные вклю-чения, состоящие из криоглобулинов. При поражении почек в моче находится белок, эритроциты, цилиндры, при развитии почечной недоста-точности в крови увеличивается уровень креатинина. При определении наличия и содержания криоглобулинов нужно строго соблюдать условия забора крови (более 10 мл венозной крови в подогретую до 37 °С пробирку) и постановки (сыворотка обязана находится при 4 °С в течение 7 дней) теста, по другому его диагностическая ценность существенно понижается. Отсутствие криоглобулинов при обычной медицинской картине просит проведения их повторного определения (более 3 раз), в этом случае, если криоглобулины не определяются нужно исключить криофибриногенемию. Рентгенологическое исследование и КТ грудной клетки используют при подозрении на лѐгочное крово-течение. УЗИ нередко употребляется для оценки структурных конфигураций печени при криоглобулинемиче-ском васкулите, ассоциированном с вирусом гепатита C. Биопсия кожи и почки являются наиболее достовер-ным методом подтверждения диагноза. Лечение НСV-ассоциированных смешанных криоглобулинемии и васкулитов До того, как роль HCV в развитии криоглобулинемических васкулитов была установлена, методом выбо-ра в лечении являлась иммуносупрессия, то есть применение кортикостероидов, цитостатиков и/или плазмафе-реза. В настоящее время, когда при смешанной криоглобулинемии в 80-90% случаев выявляется HCV, появи-лась возможность применять этиотропную противовирусную терапию [9,10]. При этом имеется в виду противовирусное лечение IFN-a (по 5-6 млн. МЕ. три раза в неделю), по меньшей мере в течение 6 месяцев. Такое лечение вызывает клиническую ремиссию у многих больных. Однако после его прекращения нередко развива-ются обострения [3,18,19], даже несмотря на имевшую место сероконверсию. Таким образом, возникает необ-ходимость в длительном лечении – до 12-24-36 мес. Более эффективна терапия пегилированными интерферо-нами в обычных дозах для лечения гепатита С в сочетании с рибавирином. Но лечение интерферонами может быть рискованным, поскольку может привести к прогрессирования системной патологии. Поэтому при быс-тропрогрессирующем ГН иммуносупрессия остается по-прежнему методом выбора. Плазмаферез – нужный элемент при лечении криоглобулинемического васкулита высокой и средней ак-тивности. Более распространенная схема предупреждает замещение до 3 л плазмы трижды в неделю в течение 2-3 недель. В качестве замещающего раствора употребляется 5% раствор нагретого альбумина и/или нативная и свежезамороженная плазма. Уменьшение криокрита на фоне плазмофереза не постоянно коррелирует с уменьшением клинических проявлений, поэтому нужно учесть изменение клинических симптомов. Быстрее всего на фоне плазмафереза проходят кожные поражения, полинейропатия традиционно устойчива к такой те-рапии. Подход к терапии криоглобулинемического васкулита зависит от активности заболевания и наличия у больного угрожающих жизни либо существенно ухудшающих еѐ качество осложнений. К огорчению, обще-принятой системы оценки тяжести заболевания у больных криоглобулинемическим васкулитом не создано. Угрожающее жизни течение. В эту группу входят больные с быстропрогрессирующим гломерулонеф-ритом; васкулитом ЦНС, мезетериальных сосудов; большими язвами, резистентными к терапии; некрозами кончиков пальцев. Рекомендуемый режим терапии: 1. Циклофосфамид внутрь 2 мг/кг×сут. 2. Метилпреднизолон внутривенно 500-1000 мг/сут в течение 3 дней с переходом на приѐм внутрь. 3. Плазмаферез – 3 л плазмы трижды в неделю на протяжение 2–3 недель. Тяжѐлое течение. В эту группу входят больные с нефротическим синдромом, тяжѐлой полинейропатией и поражениями кожи неязвенного характера. Рекомендуемый режим терапии: 1. Циклофосфамид внутривенно 0,5–1,0 г/м3 каждые 3 недели. 2. Метилпреднизолон внутривенно 500–1000 мг/сут в течение 3 дней с переходом на приѐм внутрь. Течение умеренной степени тяжести. В эту группу входят больные с мочевым синдромом, пальпируе-мой пурпурой, субклинической либо легкой степени выраженности полинейропатия, артралгии, миалгии. Ре-комендуемый режим терапии: 1. Интерферон альфа2 по 3 млн МЕ 3 раза в неделю. 2. Метилпреднизолон по 5–7,5 мг в дни, когда нет приѐма интерферона альфа-2. Поддерживающая противовирусная терапия. После достижения ремиссии всем больным нужно проводить комбинированную противовирусную тера-пию пегилированым интерфероном альфа-2 и рибавирином. При отсутствии почечной недостаточности пред-почтение отдаѐтся ПЭГ-интерферону альфа2a либо ПЭГ-интерферону альфа-2b. При СКФ менее 50мл/мин рибавирин назначать не следует. Длительность противовирусной терапии, обычно, составляет от 19 до 24 меся-цев. Нужно учитывать то, что интерферон альфа-2 может вызывать обострение как невропатии, так и гломеру-лонефрита, поэтому при наличии соответствующих симптомов его следует назначать с особенной осторожно-стью. Резистентное течение. В последнее время в терапии устойчивых к стандратному лечению случаев криоглобулинемического васкулита начали употреблять моноклональные антитела к CD20-рецепторам (продукт получил название «ритуксимаб»). Ритуксимаб представляет собой химерные моноклональные антитела, со-стоящие из вариабельной области иммуноглобулина мыши с антигенной спецификой к CD20рецептору В-лимфоцитов и константной области людского иммуноглобулина. Механизм иммуносупрессивного действия продукта связан с его способностью связываться с CD20-антигеном Влимфоцитов, экспрессируемым ими на различных стадиях дифференцировки. В итоге происходит разрушение B-клеток, участвующих в индукции ау-тоиммунного ответа. Но для окончательного определения эффективности и сохранности ритуксимаба нужны дальнейшие исследования. Хирургическое лечение. Хирургическое вмешательство нужно при развитии осложнений васкулита (пе-риферической гангрены, тяжѐлых язвенных поражений и др.). Прогноз. При отсутствии исцеления прогноз неблагоприятный. При проведении комбинированной тера-пии 10 летняя выживаемость с момента возникновения первых симптомов составляет 70%. Список литературы: 1. Lerner A.B., Watson C.J. Studies of cryoglobulins. I. Unusual purpura associated with the presence of a high concentration of cryoglobulin (cold precipitable serum globulin). Am J Med Sci 1947; 214: 410-415. 2.Brouet J.-C., Clauvel J.-P., Danon F. el al. Biologic and clinical significance of cryoglobulins: a report of 86 cases. Am J Med 1974; 57: 775-788. 3.Gumber S.C., Chopra S. Hepatitis C. a multifaceted disease. Review of extrahepatic manifestations. Ann Intern Med 1995; 123:615-620. 4.Wong V.S., Egner W., Elsey T. et al. Incidence, character and clinical relevance of mixed cryoglobulinemia in patients with chronic hepatitis C infection, din Exp Immunol 1996; 104: 25-31. 5.Pasqual M., Perrin L., Giostra E. et al. Hepatitis C virus in patients with cryoglogulinemia type II. J Infect Dis 1990; 162: 569-570. 6.Ferri C., Greco F., Longobardo G. el al. Antibodies to hepatitis C virus in patients with mixed cryoglobulinemia. Arthritis Rheum 1991: 34: 1606-1610. 7.Agnello V., Chung R.T., Kaplan L.M. A role for hepatitis V virus infection in type II cryoglobulinemia. N Engi J Med 1992; 327:1490-1495. 8.Zignego A.L., Ferri C., Giannini C. et al. Hepatitis C virus genotype analysis in patients with type II mixed cryoglobulinemia. Ann Intern Med 1996; 124: 31-34. 9.Pasero G.P., Bombardieri S., Ferri C. From internal medicine to rheumatology and back: the example of mixed cryoglobulinemia. din Exp Rheumatol 1995; 13: 1-5. 10. Pawlotsky J.-M., Roudot-Thoraval F., Simmonds P. et al. Extrahepatic immunologic manifestations in chronic hepatitis C virus serotypes. Ann Intern Med 1995; 122: 169-173. 11. Martin P. Hepatitis C genotypes: The key to pathogenicity? Ann Intern Med 1995; 122: 227-228. 12. Sinico R.A., Ribero M.L., Fornasieri A. et al. Hepatitis C virus genotype in patients with essential mixed cryoglobulinaemia. Q J Med 1995; 88: 805-810. 13. Fornasieri A., D'Amico G. Type II mixed cryoglobulinaemia, hepatitis C virus infection, and glomerulonephritis. Nephrol Dial Transplant 1996; 11 [Suppl. 4]: 25-30. 14. D'Amico G. Is type II mixed cryoglobulinaemia an essential part of hepatitis C virus (HCV) - associated glomerulonephritis? Nephrol Dial Transplant 1995; 10: 1279-1282. 15. Dolcher M.P., Marchini B., Sabbatini A. et al. Autoantibodies from mixed cryoglobulinemia patients bind glome-rular antigens. din Exp Immunol 1994; 96: 317-322. 16. Pawlotsky J.-M., Dhumeaux D., Bagot M. Hepatitis C virus in dermatology. Arch Dermatol 1995; 131: 11851193. 17. Katayama I., Kimura K., Nishioka K. Cold induced complement activation in hepatitis C virus associated vasculopathy. J Rheumatol 1995; 22: 1806-1807. 18. Durand J.M., Cretel E., Kapllanski G. el al. Long-term results of therapy with interferon alpha for cryoglobulinemia associated with hepatitis C virus infection, din Rheumatol 1994; 13: 123-125. 19. Gilli P., Stabellini N., Storari A. et al. Effect of human leukocyte alpha interferon on cryoglobulinaemic membranoproliferative glomerulonephritis associated with hepatitis C virus infection. Nephrol Dial Transplant 1996; 11: 526-528. 20. Dupin N., Chosidow O., Lunel F. et al. Essential mixed cryoglobulinemia. A comparative study of dermatologic manifestations in patients infected or noninfected with hepatitis C virus. Arch Dermatol 1995; 131: 1124-1127. 21. Vitali C., Ferri C., Nasti P. et al. Hypercomplementaemia as a marker of the evolution from benign to malignant B cell proliferation in patients with type II mixed croglobulinemia. Br J Rheuinaiol 1994; 33: 791-792. Аралас криоглобулинемия синдромы Баймурынова А. Ж., Құрманова Г.М. Аралас криоглобулинемия – қан тамырлар қабырғасында криоглобулиндердің жиналуымен сипатталып, терінің пурпура түрінде кӛрінетін зақымдалуымен, гломерулонефрит дамуымен жүретін бүйрек шумақтарының зақымдалуымен және буындардың артрит түрінде зақымдалуымен кӛрінетін майда қан тамырлар жүйелі васкулитінің ерекше түрі. Тҥйінді сӛздер: аралас криоглобулинемия, HCV, HBVинфекция, ревматоидты фактор, гломерулонефрит. Mixed cryoglobulinemia Bajmurynova A.Z., Kurmanova G.M. Mixed cryoglobulinemia - special type system vasculitis the fine vessels, described as cryoglobulin adjournment in a vessels and most often shown defeat of a leather in the form of purples, an arthritis and defeat of kidneys with development of glomerulonephritis. Keywords: mixed cryoglobulinemia, HCV, a HBV-infection, rheumatoid factor, glomerulonephritis.