Задача 29. Ферментативный гидролиз N
advertisement
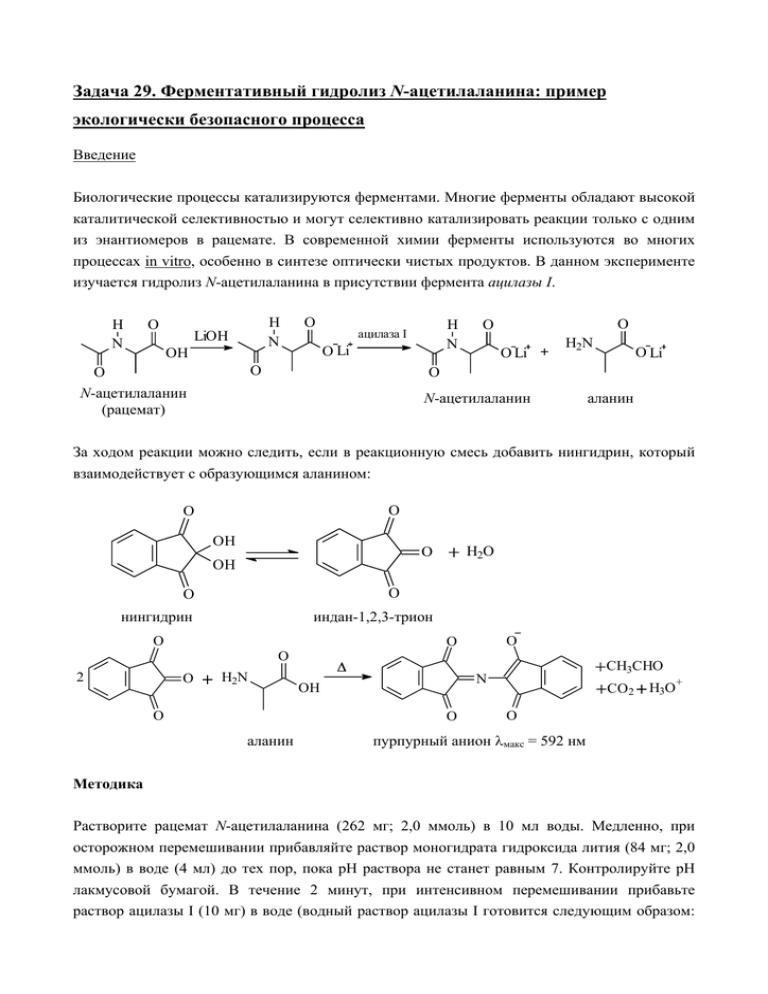
Задача 29. Ферментативный гидролиз N-ацетилаланина: пример экологически безопасного процесса Введение Биологические процессы катализируются ферментами. Многие ферменты обладают высокой каталитической селективностью и могут селективно катализировать реакции только с одним из энантиомеров в рацемате. В современной химии ферменты используются во многих процессах in vitro, особенно в синтезе оптически чистых продуктов. В данном эксперименте изучается гидролиз N-ацетилаланина в присутствии фермента ацилазы I. H N O H N LiOH OH O O Li O O N-ацетилаланин (рацемат) H N ацилаза I O O O Li H2N O Li O N-ацетилаланин аланин За ходом реакции можно следить, если в реакционную смесь добавить нингидрин, который взаимодействует с образующимся аланином: O O OH O O нингидрин индан-1,2,3-трион O O H2N ∆ аланин CH3CHO Ν OH Ο O Ο Ο O 2 H2O O OH CO 2 H3O+ Ο пурпурный анион λмакс = 592 нм Методика Растворите рацемат N-ацетилаланина (262 мг; 2,0 ммоль) в 10 мл воды. Медленно, при осторожном перемешивании прибавляйте раствор моногидрата гидроксида лития (84 мг; 2,0 ммоль) в воде (4 мл) до тех пор, пока pH раствора не станет равным 7. Контролируйте pH лакмусовой бумагой. В течение 2 минут, при интенсивном перемешивании прибавьте раствор ацилазы I (10 мг) в воде (водный раствор ацилазы I готовится следующим образом: навеска фермента добавляется к 5 мл воды, затем раствор отфильтровывается на стеклянном фильтре, покрытом диатомитом). После этого доведите объем раствора водой до 20,0 мл (точно). Поместите реакционную смесь в водяную баню (37оС) на 60 минут. Затем перенесите ровно 0,25 мл (для этого используйте шприц или мерную пипетку) реакционной смеси в пробирку и добавьте туда нингидрин (Sigma N 1632) (1,25 мл). Эту смесь нагревайте в кипящей воде в течение 20 минут, при этом появится интенсивная пурпурная окраска. После охлаждения аккуратно добавьте содержимое пробирки к буферному раствору, состоящему из 4 М литий-ацетатного водного буфера (рН = 5,2) и диметилсульфоксида в соотношении 1:3, находящемуся в мерной колбе на 250 мл. Доведите объем раствора до 250 мл. Измерьте оптическую плотность на спектрофотометре при λ = 592 нм. В качестве стандарта используйте раствор нингидрина в том же литий-ацетатном буфере в диметилсульфоксиде. εпурпурного комплекса = 13350 л⋅моль-1⋅см-1. Запишите следующие данные: 1. Начальную концентрацию рацемического N-ацетилаланина. 2. Значение оптической плотности при λ = 592 нм. 3. Используя закон Бугера-Ламберта-Бера, рассчитайте количество аланина (в ммоль), образовавшегося в результате ферментативной реакции. 4. Рассчитайте степень превращения. Вопросы: 29-1 Будет ли образующийся аланин оптически активен: да или нет? 29-2 Будет ли непрореагировавший N-ацетилаланин: (1) оптически неактивен, (2) обогащен одним из энантиомеров, (3) оптически чист, если степень превращения меньше 50%? 29-3 Будет ли непрореагировавший N-ацетилаланин: (1) оптически неактивен, (2) обогащен одним из энантиомеров, (3) оптически чист, если степень превращения составит ровно 50%? 29-4 Достижима ли степень превращения больше 50%, да или нет? Особое замечание: Если позволяет время, остановите реакцию и определите концентрацию аланина через 10, 25, 40 и 60 минут после начала реакции. Постройте график зависимости концентрации аланина от времени и оцените оптимальное время проведения реакции. Список необходимых реактивов: N-ацетилаланин, рацемат ацилаза I гидроксид лития раствор нингидрина (Sigma N 1632) 265 мг 10 мг 85 мг 2 мл Коды безопасности: RSRSR 23-34 S 45-26-27-36/37/39 R 11-20/21/22, 34 S 16-26-27-36/37/39 диметилсульфоксид литий-ацетатный буфер ок. 70 мл рН 5,2 R 36/37/38 R 20/21/22-63 S 26-36-23 S 22-36