ИНСТРУКЦИЯ «АмплиСенс Плант-контроль-FL»
advertisement

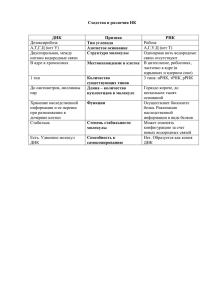
ИНСТРУКЦИЯ по применению набора реагентов для контроля качества препаратов ДНК, полученных при проведении исследований на наличие генетическимодифицированных организмов (ГМО) растительного происхождения в продуктах питания, сырье и кормах для животных, путем выявления ДНК экзогенного внутреннего контроля методом полимеразной цепной реакции (ПЦР) с гибридизационно-флуоресцентной детекцией «АмплиСенс® Плант-контроль-FL» АмплиСенс ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Российская Федерация, 111123, город Москва, улица Новогиреевская, дом 3а Только для исследовательских и иных немедицинских целей ОГЛАВЛЕНИЕ СПИСОК СОКРАЩЕНИЙ ............................................................................................... 3 НАЗНАЧЕНИЕ ................................................................................................................ 3 ПРИНЦИП МЕТОДА ...................................................................................................... 3 ФОРМАТЫ И ФОРМЫ ВЫПУСКА НАБОРА РЕАГЕНТОВ ........................................... 5 АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ ....................................................................... 5 МЕРЫ ПРЕДОСТОРОЖНОСТИ ................................................................................... 5 ДОПОЛНИТЕЛЬНЫЕ МАТЕРИАЛЫ И ОБОРУДОВАНИЕ ........................................... 7 ВЗЯТИЕ, ТРАНСПОРТИРОВАНИЕ И ХРАНЕНИЕ ИССЛЕДУЕМОГО МАТЕРИАЛА 7 ФОРМАТ FRT ................................................................................................................. 8 СОСТАВ.......................................................................................................................... 8 ПРОВЕДЕНИЕ ПЦР-ИССЛЕДОВАНИЯ ........................................................................ 8 ЭКСТРАКЦИЯ ДНК ИЗ ИССЛЕДУЕМЫХ ОБРАЗЦОВ ................................................. 8 ПРОВЕДЕНИЕ АМПЛИФИКАЦИИ С ДЕТЕКЦИЕЙ В РЕЖИМЕ «РЕАЛЬНОГО ВРЕМЕНИ» ..................................................................................................................... 9 А. Подготовка пробирок для амплификации................................................................ 9 Б. Проведение амплификации с детекцией в режиме «реального времени» ........... 9 АНАЛИЗ И ИНТЕРПРЕТАЦИЯ РЕЗУЛЬТАТОВ ......................................................... 10 СРОК ГОДНОСТИ. УСЛОВИЯ ТРАНСПОРТИРОВАНИЯ И ХРАНЕНИЯ ................. 13 ПРИЛОЖЕНИЕ 1. Расчетная таблица приготовления реакционных смесей для проведения амплификации ......................................................................................... 14 СИМВОЛЫ, ИСПОЛЬЗУЕМЫЕ В ПЕЧАТНОЙ ПРОДУКЦИИ .................................... 15 Формат FRT Форма 1: REF R-G11(RG,iQ,Dt,Ank) / VER 04.02.15 / стр. 2 из 16 СПИСОК СОКРАЩЕНИЙ В настоящей инструкции применяются следующие сокращения и обозначения: ГМ ВКО ОКО ПКО ПЦР К+ К– ОК - генетически модифицированный - внутренний контрольный образец - отрицательный контрольный образец - положительный контрольный образец - полимеразная цепная реакция - положительный контроль ПЦР - отрицательный контроль ПЦР - отрицательный контроль экстракции - Федеральное бюджетное учреждение науки «Центральный ФБУН ЦНИИ научно-исследовательский институт эпидемиологии» Эпидемиологии Федеральной службы по надзору в сфере защиты прав Роспотребнадзора потребителей и благополучия человека FRT - флуоресцентная детекция в режиме «реального времени» НАЗНАЧЕНИЕ Набор реагентов «АмплиСенс® Плант-контроль-FL» предназначен для контроля качества препаратов ДНК, полученных при проведении исследований на наличие генетически-модифицированных организмов (ГМО) растительного происхождения в продуктах питания, сырье и кормах для животных, с помощью выявления ДНК экзогенного внутреннего контроля (рекомбинантного препарата ВКО STI-87) методом ПЦР с гибридизационно-флуоресцентной детекцией продуктов в режиме «реального времени». ПРИНЦИП МЕТОДА Контроль качества препаратов ДНК, полученных при проведении исследований на наличие генетически-модифицированных организмов (ГМО) растительного происхождения, включает в себя три этапа: экстракцию ДНК из образцов, содержащих растительные ткани, с добавлением в процессе экстракции препарата экзогенного внутреннего контрольного образца (ВКО STI-87), амплификацию фрагмента ДНК препарата ВКО STI-87 и гибридизационно-флуоресцентную детекцию, которая производится непосредственно в ходе ПЦР. Тестирование позволяет оценить качество проведения процесса экстракции ДНК и выявить причину неудовлетворительных результатов амплификации эндогенных внутренних контролей (ЭК) на этапе скрининга ГМО. Возможны две схемы проведения контроля качества препаратов ДНК: – параллельно этапу скрининга ГМО, – после этапа скрининга ГМО. Формат FRT Форма 1: REF R-G11(RG,iQ,Dt,Ank) / VER 04.02.15 / стр. 3 из 16 При проведении контроля качества параллельно скринингу ГМО экзогенный внутренний контрольный образец (ВКО STI-87) добавляется в образцы на этапе первичной экстракции ДНК, после чего в двух параллельных ПЦР-тестированиях на разных приборах проводятся скрининг ГМО и контроль качества препаратов ДНК. Данный вариант использования набора реагентов «АмплиСенс® Плант-контроль-FL» рекомендуется для образцов, в которых заведомо предполагается наличие большого количества ингибиторов ПЦР, а также для образцов продуктов с низким содержанием растительных компонентов в рецептуре (лецитин, БАДы, соусы, жировая продукция и др.). Контроль качества препаратов ДНК после этапа скрининга ГМО проводится при получении на этапе скрининга неудовлетворительных результатов амплификации эндогенных контролей (ЭК). Для таких образцов необходимо провести повторную экстракцию ДНК с добавлением ВКО STI-87 (на этапе первичного скрининга ВКО STI87 не добавляется), после чего провести ПЦР-тестирование для контроля качества препаратов ДНК. Положительный результат амплификации (см. п. «Анализ и интерпретация результатов») ДНК ВКО STI-87 свидетельствует о хорошем качестве экстракции ДНК, приемлемом для анализа ГМО в образце методом ПЦР, то есть об эффективной очистке препарата ДНК от примесей. Результаты скрининга ГМО в таких образцах валидны, при условии получения корректных результатов по всем контрольным реакциям этапа скрининга. Если для образца на этапе скрининга получен отрицательный результат амплификации эндогенного внутреннего контроля (ЭК), и при этом результат амплификации ДНК ВКО STI-87 положительный, то следует считать, что образец изначально содержит недостаточное количество ДНК растительного происхождения для определения его методом ПЦР (например, вследствие деградации или удаления ДНК на этапе производства продукта питания). Анализ наличия ГМО в таких образцах методом ПЦР не возможен. Отрицательный результат амплификации ДНК ВКО STI-87 (см. п. «Анализ и интерпретация результатов») может быть обусловлен недостаточно качественным проведением операций при экстракции ДНК, а также недостаточной очисткой препарата ДНК, полученного после этапа экстракции, от примесных веществингибиторов (полисахариды, липиды, протеины, фенолы, соли). Влияние ингибиторов может быть устранено путем разбавления. В случае неэффективности данного способа и для проверки качества проведения процесса экстракции следует Формат FRT Форма 1: REF R-G11(RG,iQ,Dt,Ank) / VER 04.02.15 / стр. 4 из 16 провести повторную экстракцию ДНК из данного образца с добавлением ВКО STI-87. ФОРМАТЫ И ФОРМЫ ВЫПУСКА НАБОРА РЕАГЕНТОВ Набор реагентов выпускается в 1 формате. Формат FRT Набор реагентов выпускается в 2 формах комплектации: Форма 1 включает комплект реагентов «ПЦР-комплект» вариант FRT-50 F. Форма 2 включает наборы реагентов оптом, расфасованные по отдельным реагентам, с маркировкой реагентов на их оптовой фасовке. Форма комплектации 1 предназначена для проведения амплификации ДНК c гибридизационно-флуоресцентной детекцией в режиме «реального времени». Для проведения полного ПЦР-исследования необходимо использовать комплекты реагентов для экстракции ДНК из продуктов питания, рекомендованные ФБУН ЦНИИ Эпидемиологии Роспотребнадзора. Форма комплектации 2 предназначена для производственных целей для последующей маркировки на языке заказчика и комплектации по наборам. ВНИМАНИЕ! Использование формы комплектации 2 производится только в соответствии с регламентом, утвержденным ФБУН ЦНИИ Эпидемиологии Роспотребнадзора. АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ Аналитическая чувствительность Вид исследуемого материала Комплект для экстракции ДНК Комплект для амплификации и детекции Аналитическая чувствительность, копий ДНК/мл Продукты питания, растительное сырье, корма для животных «ДНК-сорб-С» «ПЦР-комплект» вариант FRT-50 F 1х103 Аналитическая специфичность Отсутствует положительная реакция в тестах с ДНК растений, млекопитающих, птиц, рыб. МЕРЫ ПРЕДОСТОРОЖНОСТИ Работа должна проводиться в лаборатории, выполняющей молекулярнобиологические (ПЦР) исследования продуктов, содержащих растительные компоненты или растительное сырье, с соблюдением санитарно-эпидемических правил СП 1.3.2322-08 «Безопасность работы с микроорганизмами III–IV групп Формат FRT Форма 1: REF R-G11(RG,iQ,Dt,Ank) / VER 04.02.15 / стр. 5 из 16 патогенности (опасности) и возбудителями паразитарных болезней», СанПиН 2.1.7.2790-10 «Санитарно-эпидемиологические требования к обращению с медицинскими отходами» и методических указаний МУ 1.3.2569-09 «Организация работы лабораторий, использующих методы амплификации нуклеиновых кислот при работе с материалом, содержащим микроорганизмы I–IV групп патогенности». При работе всегда следует выполнять следующие требования: - Организовывать работу и хранение исследуемых образцов в соответствии с СП 1.3.2322-08 «Безопасность работы с микроорганизмами III–IV групп патогенности (опасности) и возбудителями паразитарных болезней». - Убирать и дезинфицировать разлитые образцы или реактивы, используя дезинфицирующие средства в соответствии СП 1.3.2322-08 «Безопасность работы с микроорганизмами III–IV групп патогенности (опасности) и возбудителями паразитарных болезней». - Лабораторный процесс должен быть однонаправленным. Анализ проводится в отдельных помещениях (зонах). Работу следует начинать в Зоне Выделения, продолжать в Зоне Амплификации и Детекции. Не возвращать образцы, оборудование и реактивы в зону, в которой была проведена предыдущая стадия процесса. - Удалять неиспользованные реактивы в соответствии с СанПиН 2.1.7.2790-10 «Санитарно-эпидемиологические требования к обращению с медицинскими отходами». ВНИМАНИЕ! При удалении отходов после амплификации (пробирок, содержащих продукты ПЦР) недопустимо открывание пробирок и разбрызгивание содержимого, поскольку это может привести к контаминации продуктами ПЦР лабораторной зоны, оборудования и реагентов. - Применять набор строго по назначению, согласно данной инструкции. - Допускать к работе с набором только специально обученный персонал. - Не использовать набор по истечении срока годности. - Использовать одноразовые перчатки, лабораторные халаты, защищать глаза во время работы с образцами и реактивами. Тщательно вымыть руки по окончании работы. - Избегать контакта с кожей, глазами и слизистой оболочкой. При контакте немедленно промыть пораженное место водой и обратиться за медицинской помощью. Формат FRT Форма 1: REF R-G11(RG,iQ,Dt,Ank) / VER 04.02.15 / стр. 6 из 16 ДОПОЛНИТЕЛЬНЫЕ МАТЕРИАЛЫ И ОБОРУДОВАНИЕ 1. Комплект реагентов для выделения ДНК из клинического материала, продуктов питания и кормов для животных – «ДНК-сорб-С» (ТУ 9398-075-01897593-2008). 2. Дополнительные материалы и оборудование для экстракции ДНК – согласно инструкции к комплекту реагентов для выделения ДНК. 3. Бокс абактериальной воздушной среды (ПЦР-бокс). 4. Центрифуга/вортекс. 5. Автоматические дозаторы переменного объема (от 5 до 50 мл, от 20 до 200). 6. Одноразовые наконечники с фильтром до 100 мкл и 200 мкл в штативах. 7. Штативы для пробирок объемом 0,2 мл. 8. Холодильник от 2 до 8 °С с морозильной камерой от минус 24 до минус 16 °. 9. Отдельный халат, шапочки, обувь и одноразовые перчатки по МУ 1.3.2569-09. 10.Емкость для сброса наконечников. 11.Программируемый амплификатор с системой детекции флуоресцентного сигнала в режиме «реального времени» (например, Rotor-Gene 3000/6000 (Corbett Research, Австралия), Rotor-Gene Q (Qiagen, Германия); iCycler iQ, iCycler iQ5 (Bio-Rad, США); «ДТ-96» («ДНК-Технология», Россия), «АНК-16»/ «АНК-32» (ЗАО «Синтол», Россия) или аналогичные). 12.Одноразовые полипропиленовые пробирки для ПЦР объемом 0,2 мл a) тонкостенные нестрипованные пробирки для ПЦР объемом 0,2 мл с выпуклой крышкой (например, Axygen, США), стрипованные пробирки с выпуклой крышкой или 96-луночный планшет для ПЦР, снабженный термостабильными оптически прозрачными пленками (например, Bio-Rad, США) – при использовании прибора планшетного типа; б) тонкостенные нестрипованные пробирки для ПЦР объемом 0,2 мл с плоской крышкой (например, Axygen, США) – при использовании прибора роторного типа. ВЗЯТИЕ, ТРАНСПОРТИРОВАНИЕ И ХРАНЕНИЕ ИССЛЕДУЕМОГО МАТЕРИАЛА Рекомендации по взятию, транспортированию и хранению исследуемого материала, а также подготовке исследуемого материала к экстракции представлены в инструкциях к наборам реагентов для скрининга (напр., «АмплиСенс ГМ кукуруза-FL», «АмплиСенс ГМ соя-FL», «АмплиСенс ГМ Плант-1-FL» производства ФБУН ЦНИИ Эпидемиологии Роспотребнадзора. Формат FRT Форма 1: REF R-G11(RG,iQ,Dt,Ank) / VER 04.02.15 / стр. 7 из 16 ФОРМАТ FRT ФОРМАТ FRT СОСТАВ Комплект реагентов «ПЦР-комплект» вариант FRT-50 F – комплект реагентов для амплификации ДНК ВКО с STI-87 гибридизационно-флуоресцентной детекцией в режиме «реального времени» – включает: Реактив Описание Прозрачная бесцветная ПЦР-смесь-1-FRT Плант-контроль жидкость Прозрачная бесцветная ПЦР-буфер-Flu жидкость Прозрачная бесцветная Полимераза (TaqF) жидкость Прозрачная бесцветная ПКО STI-88 жидкость Прозрачная бесцветная ТЕ-буфер жидкость Объем, мл Кол-во 0,11 6 пробирок 0,35 1 пробирка 0,035 1 пробирка 0,1 1 пробирка 0,5 1 пробирка Комплект реагентов рассчитан на проведение 55 реакций амплификации, включая контроли. К комплекту реагентов прилагаются контрольные образцы этапа экстракции: Реактив Описание Прозрачная бесцветная жидкость Прозрачная бесцветная жидкость ВКО STI-87 ОКО Объем, мл Кол-во 1,0 1 пробирка 1,6 1 пробирка ПРОВЕДЕНИЕ ПЦР-ИССЛЕДОВАНИЯ ПЦР-исследование состоит из следующих этапов: - Экстракция ДНК из исследуемых образцов. - Проведение амплификации с гибридизационно-флуоресцентной детекцией в режиме «реального времени». - Анализ и интерпретация результатов. ЭКСТРАКЦИЯ ДНК ИЗ ИССЛЕДУЕМЫХ ОБРАЗЦОВ Для экстракции ДНК используется набор реагентов «ДНК-сорб-С» в соответствии с инструкцией к данному набору. Каждый исследуемый образец рекомендуется тестировать в двух повторах. ВНИМАНИЕ! Перед внесением сорбента универсального в каждую пробирку (в том числе и в пробирку с ОКО) отдельным наконечником добавить по 10 мкл ВКО STI-87, тщательно перемешать на вортексе, сбросить капли с крышек пробирок (центрифугировать 5 с при 5 тыс об/мин на микроцентрифуге). Формат FRT Форма 1: REF R-G11(RG,iQ,Dt,Ank) / VER 04.02.15 / стр. 8 из 16 ФОРМАТ FRT ПРОВЕДЕНИЕ АМПЛИФИКАЦИИ С ДЕТЕКЦИЕЙ В РЕЖИМЕ «РЕАЛЬНОГО ВРЕМЕНИ» А. Подготовка пробирок для амплификации Выбор пробирок для амплификации зависит от используемого амплификатора с системой детекции в режиме «реального времени». Для внесения в пробирки реагентов, проб ДНК и контрольных образцов используются одноразовые наконечники с фильтрами. Общий объем реакционной смеси – 25 мкл, включая объем пробы ДНК – 10 мкл. 1. Разморозить необходимое количество пробирок с ПЦР-смесью-1-FRT Плантконтроль. Перемешать на вортексе и сбросить капли с помощью кратковременного центрифугирования. 2. Отобрать необходимое количество пробирок на 0,2 мл. 3. Для проведения N реакций смешать в отдельной пробирке 10*(N+1) мкл ПЦРсмеси-1-FRT Плант-контроль, 5*(N+1) мкл ПЦР-буфера-Flu и 0,5*(N+1) мкл полимеразы (TaqF). Сделать расчет на необходимое число реакций, включающее тестирование исследуемых и контрольных образцов, можно согласно расчетной таблице, приведенной в приложении 1. 4. Перемешать подготовленную смесь на вортексе, осадить капли кратковременным центрифугированием и внести по 15 мкл в пробирки на 0,2 мл. 5. Используя наконечник с фильтром, в подготовленные пробирки добавить по 10 мкл ДНК исследуемых образцов. (Необходимо избегать попадания сорбента универсального в реакционную смесь). 6. Поставить контрольные реакции: а) отрицательный контроль ПЦР (К–) – внести в пробирку 10 мкл ТЕ-буфера. б) положительный контроль ПЦР (К+) – внести в пробирку 10 мкл ПКО STI-88. Б. Проведение амплификации с детекцией в режиме «реального времени» 1. Запрограммировать прибор (амплификатор с системой детекции в режиме «реального времени») для выполнения соответствующей программы амплификации и детекции флуоресцентного сигнала (см. табл. 1 и 2). Формат FRT Форма 1: REF R-G11(RG,iQ,Dt,Ank) / VER 04.02.15 / стр. 9 из 16 ФОРМАТ FRT Таблица 1 Программа амплификации для приборов Rotor-Gene, «ДТ-96», «АНК-16» и «АНК-32». Этап Температура, °С Продолжительность Этапа Измерение флуоресценции Количество циклов Hold/Удерж. темп-ры 95 15 мин (900 c) – 1 Cycling/Цикли рование 95 59 10 с 60 с – JOE/Yellow/R6G 40 Таблица 2 Программа амплификации для приборов iCycler iQ и iQ5. Этап Температура, °С Продолжительность Этапа Измерение флуоресценции Количество циклов Hold/Удерж. темп-ры 95 15 мин – 1 Cycling/Цикли рование 95 59 15 с 60 с – JOE 42 2. Установить пробирки в ячейки реакционного модуля прибора. 3. Запустить выполнение программы амплификации с детекцией флуоресцентного сигнала. 4. По окончании выполнения программы приступить к анализу и интерпретации результатов. АНАЛИЗ И ИНТЕРПРЕТАЦИЯ РЕЗУЛЬТАТОВ Анализ результатов проводят с помощью программного обеспечения используемого прибора для проведения ПЦР c детекцией в режиме «реального времени». Анализируют кривые накопления флуоресцентного сигнала по каналу для флуорофора R6G, по которому регистрируется сигнал, свидетельствующий о накоплении продукта амплификации ДНК ВКО STI-87. Результаты интерпретируются на основании наличия (или отсутствия) пересечения кривой флуоресценции с установленной на соответствующем уровне пороговой линией, что определяет наличие (или отсутствие) для данной пробы ДНК значения порогового цикла Ct в соответствующей графе в таблице результатов. Принцип интерпретации результатов следующий: ДНК ВКО STI-87 обнаружена, если для данной пробы в таблице результатов по каналу для флуорофора R6G определено значение порогового цикла Ct, не Формат FRT Форма 1: REF R-G11(RG,iQ,Dt,Ank) / VER 04.02.15 / стр. 10 из 16 ФОРМАТ FRT превышающее указанное граничное значение (см. табл. 3). В этом случае результат амплификации является положительным, а качество экстракции ДНК приемлемым для анализа ГМО в образце методом ПЦР. Если сигнал амплификации ДНК ВКО STI-87 отсутствует или его значение не соответствует заданным критериям (см. табл. 3), результат амплификации является отрицательным. Если причиной отрицательного результата предположительно является недостаточная очистка препарата ДНК от ингибиторов на этапе экстракции, рекомендуется снизить их концентрацию путём разбавления экстрагированного препарата ДНК в 5 раз, используя в качестве разбавителя ТЕ-буфер. Для разбавления отобрать 10 мкл выделенного препарата ДНК в чистую пробирку и добавить 40 мкл ТЕ-буфера, полученный раствор используется далее для повторного проведения ПЦР с помощью набора реагентов «АмплиСенс ® Плантконтроль-FL». Если данная процедура не оказала заметного влияния на устранение ингибирования, а также, если на этапе экстракции были допущены ошибки, следует повторить экстракцию с добавлением ВКО STI-87 с последующим тестированием с помощью набора реагентов «АмплиСенс® Плантконтроль-FL». Препарат ДНК, полученный путем разведения или повторной экстракции, для которого получен положительный результат при тестировании с помощью набора реагентов «АмплиСенс® Плант-контроль-FL», может быть использован для последующего проведения всех этапов анализа ГМО. ВНИМАНИЕ! Граничные значения Ct указаны во вкладыше, прилагаемом к набору реагентов. См. также методические рекомендации по применению набора реагентов «АмплиСенс® Плант-контроль-FL». Результат ПЦР-исследования считается достоверным, если получены правильные результаты для положительного и отрицательного контролей амплификации и отрицательного контроля экстракции ДНК, в соответствии с таблицей оценки результатов контрольных реакций (табл. 3). Формат FRT Форма 1: REF R-G11(RG,iQ,Dt,Ank) / VER 04.02.15 / стр. 11 из 16 ФОРМАТ FRT Таблица 3 Результаты тестирования контрольных и исследуемых образцов Контролируемый этап ПЦРисследования Значение порогового цикла, Сt по каналу для флуорофора R6G Исследуемый образец Экстракция ДНК меньше граничного ОК Экстракция ДНК меньше граничного K+ ПЦР меньше граничного К– ПЦР отсутствует Тип образца ВНИМАНИЕ! 1. Появление любого значения Ct в таблице результатов для отрицательного контроля ПЦР (ТЕ-буфер) свидетельствует о наличии контаминации реактивов. В этом случае результаты анализа положительных образцов считаются недействительными. Требуется повторить анализ всех положительных по используемому каналу детекции проб, а также предпринять меры по выявлению и ликвидации источника контаминации. 2. Если значение Ct для положительного контроля ПЦР (K+) отсутствует или превышает граничное значение (см. табл. 3), требуется повторное исследование всех отрицательных проб, начиная с этапа амплификации. Формат FRT Форма 1: REF R-G11(RG,iQ,Dt,Ank) / VER 04.02.15 / стр. 12 из 16 СРОК ГОДНОСТИ. УСЛОВИЯ ТРАНСПОРТИРОВАНИЯ И ХРАНЕНИЯ Срок годности. 9 мес. Набор реагентов с истекшим сроком годности применению не подлежит. Срок годности вскрытых реагентов соответствует сроку годности, указанному на этикетках для невскрытых реагентов, если в инструкции не указано иное. Транспортирование. Набор реагентов транспортировать при температуре от 2 до 8 С не более 5 сут. При получении разукомплектовать в соответствии с указанными температурами хранения. Хранение. Набор реагентов хранить при температуре от 2 до 8 °С кроме ПЦРсмеси-1-FRT Плант-контроль и полимеразы (TaqF). ПЦР-смесь-1-FRT Плантконтроль и полимеразу (TaqF) хранить при температуре от минус 24 до минус 16 С. ПЦР-смесь-1-FRT Плант-контроль хранить в защищенном от света месте. Рекламации на качество набора реагентов «АмплиСенс® Плант-контроль-FL» направлять в отдел рекламаций, организации обучения и контроля качества по адресу 115035, г. Москва, ул. Садовническая, д. 20/13, стр. 2 (тел. (495) 664-28-84, факс (495) 664-28-89, e-mail: cs@ilslab.ru)1. 1 Отзывы и предложения о продукции «АмплиСенс» вы можете оставить, заполнив анкету потребителя на сайте: www.amplisens.ru. Формат FRT Форма 1: REF R-G11(RG,iQ,Dt,Ank) / VER 04.02.15 / стр. 13 из 16 ТАБЛИЦА ПРИГОТОВЛЕНИЯ РЕАКЦИОННЫХ СМЕСЕЙ ПРИЛОЖЕНИЕ 1. Расчетная таблица приготовления реакционных смесей для проведения амплификации Объем реактивов на указанное количество исследуемых точек с учетом контролей и запаса2 Объем реагента на одну реакцию (мкл) Число исследуемых образцов 2 4 6 8 10 12 14 16 18 20 22 24 26 28 10,00 ПЦР-смесь-1-FRT Плант-контроль, мкл 60 80 100 120 140 160 180 200 220 240 260 280 300 320 5,00 0,50 ПЦР-буфер-Flu, мкл Полимераза (TaqF), мкл 30 40 50 60 70 80 90 100 110 120 130 140 150 160 3,0 4,0 5,0 6,0 7,0 8,0 9,0 10,0 11,0 12,0 13,0 14,0 15,0 16,0 2 Число исследуемых образцов, включая контроль этапа экстракции ДНК (N), контроли этапа ПЦР, с запасом на один образец (N+3+1). Формат FRT Форма 1: REF R-G11(RG,iQ,Dt,Ank) / VER 04.02.15 / стр. 14 из 16 СИМВОЛЫ, ИСПОЛЬЗУЕМЫЕ В ПЕЧАТНОЙ ПРОДУКЦИИ Номер в каталоге Осторожно! Обратитесь к сопроводительной документации Код партии Максимальное число тестов Только для исследовательских и иных немедицинских целей Использовать до Дата изменения Обратитесь к руководству по эксплуатации Ограничение температуры Не допускать попадания солнечного света Производитель Дата изготовления Формат FRT Форма 1: REF R-G11(RG,iQ,Dt,Ank) / VER 04.02.15 / стр. 15 из 16 Лист вносимых изменений Редакция 08.09.12 IvI Место внесения изменений Титульная страница Символы, используемые в печатной продукции Титульный лист 29.01.15 ChA 04.02.15 PM Срок годности. Условия транспортирования и хранения Символы, используемые в печатной продукции Титульный лист Символы, используемые в печатной продукции Суть вносимых изменений Замена символа «Изделие для in vitro диагностики» на символ «Только для исследовательских целей» Для символа добавлена надпись «Только для научно-исследовательских целей» Изменен адресат для направления рекламаций Для символа изменена фраза с «Только для исследовательских целей» на «Только для научноисследовательских целей» Для символа изменена надпись «Только для научно-исследовательских целей» на «Только для исследовательских и иных немедицинских целей» Формат FRT Форма 1: REF R-G11(RG,iQ,Dt,Ank) / VER 04.02.15 / стр. 16 из 16