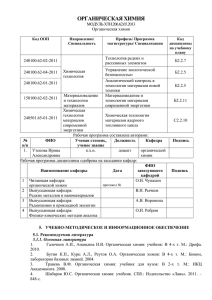
2.4 График и содержание занятий
advertisement

Западно-Казахстанский государственный университет им. М. Утемисова «Утверждаю» Директор педагогического института ____________Ботагариев Т.А. «_15_»_____09_____ 2008_г. Педагогический институт Кафедра химии УЧЕБНО-МЕТОДИЧЕСКИЙ КОМПЛЕКС ДИСЦИПЛИНЫ Теоретические основы органической химии по кредитной технологии обучения для студентов специальности 050112 – «Химия» Курс – 3 Семестр – 5 Количество кредитов - 4 Лекции – 30 часов Лабораторные занятия – 30 часов СРСП – 60 часов СРС – 60 часов Экзамен – в 5-м семестре Всего – 180 часов Уральск 2008 г 1. Учебно-методический комплекс дисциплины (УМКД) составлен Череватовой Ниной Константиновной, доцентом, кандидатом химических наук, профессором ЗКГУ на основании ГОСО РК 3.08.262-2006 специальности 050112 «Химия», МОН РК, Астана, 2006, утвержден и введен в действие Приказом Министра образования и науки РК от 23.12.2005г. № 779. На основании типовой учебной программы по «Теоретическим основам органической химии», утверждена Республиканским учебно-методическим Советом высшего и послевузовского образования МОН РК от 22.05.2006г. Рассмотрен на заседании кафедры Химии и ботаники Протокол № 1 от «15» 09. 2008 г. Зав. кафедрой ______________ Кайсагалиева Г.С. (подпись) Утвержден на заседании учебно-методического совета педагогического института Протокол № 1 от «15» 09. 2008 г. Председатель УМС педагогического института __________ Жангалиев Е.К. (подпись) (Ф.И.О.) 2. ПРОГРАММА КУРСА – (SILLABUS) 2. 1 Данные о преподавателе Череватова Нина Константиновна – профессор ЗКГУ, кандидат химических наук, доцент. Офис: кафедра химии Адрес: г. Уральск, пр. Достык, 121, к. 17 Телефон: 50-35-49 Е-mail: 2. 2 Данные о дисциплине Дисциплина «Теоретические основы органической химии» Семестр состоит из 15 учебных недель и 2 недель сессии. В неделю предполагается 4 кредит-часа. Каждый кредит-час состоит из четырех контактных часов (две лекции и два лабораторных занятия) и восьми часов самостоятельной работы обучаемых (СРО): под руководством преподавателя (СРСП)-4 и без него (СРС)-4. Распределение кредита на неделю: 01. 09.08 – 15.12.08 Занятия Занятия Время проведения СРО Контактный час 1 50 мин. СРСП, СРС (лекция) Контактный час 2 50 мин. СРСП, СРС (лекция) Контактный час 3 100 мин СПСП, СРС (лабораторное занятие) Контактный час 4 100 мин. СРСП, СРС (лабораторное занятие) Время Проведения 50 + 50 мин. 50 + 50 мин. 50 + 50 мин 50 + 50 мин. Количество кредитов – 4 Место проведения: корпус № 5 (пр. Достык 121, ауд. № 13, 14, 25, химическая лаборатория ЗКГУ, ауд. № 4) Выписка из учебного плана: Кур Семест Кредит Лекци с р ы и 3 5 4 30 Лабораторны е занятия 30 СРС П СР С Всег о Форма контроля 60 60 180 Тестирование, домашнее задание, реферат, коллоквиум, контрольная работа, собеседовани е Экзамен 2.3 Введение В современном обучении химии органическая химия занимает одно из ведущих мест, что связано с широким применением продукции органического синтеза и возрастающими потребностями в новых органических материалах технического, бытового и медицинского назначения, а также определяющей ролью органических реакций в жизнедеятельности организмов животного и растительного происхождения. Цель курса: изучение свойств основных классов органических соединений алифатического ряда в связи с их электронным строением. Задачи курса: 1. Научить характеризовать свойства веществ алифатического ряда с позиции электронного строения химической связи; 2. Уметь оперировать электронными эффектами органических соединений в объяснении химического поведения веществ; 3. Предвосхищать ожидаемые свойства вещества, исходя из их электронного строения; 4. Научиться связывать теорию с практикой (в частности, в синтезе органических веществ); Пререквизиты: для изучения курса необходимы базовые неорганической химии, аналитической химии, физической химии, физике. знания по Постреквизиты: знания, полученные при изучении указанного курса, будут необходимы при изучении химии функциональных производных органических молекул, биологической химии, коллоидной химии, методики преподавания химии. Методология обучения: обучение проводится в виде лекций, лабораторных и самостоятельных занятий под руководством преподавателя, на которых отражается содержание основного учебного материала и закрепляются практические навыки и полученные представления. Контроль знаний студентов осуществляется в виде проверки выполнения домашних заданий посредством защиты рефератов, выполнения контрольных работ, тестового задания, устного опроса, индивидуальных заданий и их защиты, коллоквиумов, собеседований, экзамена. 2.4 График и содержание занятий Неделя 1 Кредит час 4 Лекция № 1. Тема: Введение. Теория химического строения А.М.Бутлерова Содержание лекции: Предмет органической химии. Изучение соединений углерода. Связь органической химии с другими науками, ее значение для промышленности, культуры, роль в повышении благосостоянии народа. Значение органической химии в формировании материалистических мировоззрений. Теория химического строения А.М.Бутлерова. Основные положения теории. Взаимное влияние атомов в молекуле. Значение теории. Литература: 1 Перекалин В.В., Зонис С.А. Органическая химия. – М., 1982 2 Терней А. Современная органическая химия. -М., 2004 3 Петров А.А., Бальян Х.В., Трощенко А.Т. Органическая химия. – М., 1974 4 Нейланд О.Я. Органическая химия. – М., 2000 5 Несмеянов А.Н., Несмеянов Н.А. Начало Органической химии. - М., 1974. – т. 1,2. 6 Моррисон Р., Бойд Р. Органическая химия. – М., 2001 7 Череватова Н.К. Органическая химия. ч.I. Уральск, 2003 8 Череватова Н.К. Органическая химия. ч. II Уральск, 2004 9 Череватова Н.К. Органическая химия. ч. I-III Уральск, 2005 10 Череватова Н.К. Органическая химия. ч. I-IV, Уральск, 2007 11 Череватова Н.К., Жигалин П.В. Практикум по органической химии. Уральск, 2004 12 Васильева Н.В., Буховец С.В., Журавлева Л.Е., Грошева М.П. Задачи и упражнения по органической химии. – М., 1982 13 Смолина Т.А., Васильева Н.В., Куплетская Н.Б. Практические работы по органической химии. – М., 1986 14 Суворов Н.Н. Задачи и упражнения по органической химии. – М., 1988. Лекция №2 Тема: Электронная теория химической связи Содержание лекции: Влияние на развитие органической химии квантовохимических представлений и физико-химических методов исследования. Ионная и ковалентная связь. Семиполярная связь – комбинация ковалентной и ионной связи. Понятие о водородной связи. Квантовомеханическое описание ковалентной связи. Октетные формулы Льюиса. Понятие об эффективном и формальном зарядах атомов в молекулах. Понятие об изоэлектронных структурах. Литература: 1 Перекалин В.В., Зонис С.А. Органическая химия. – М., 1982 2 Терней А. Современная органическая химия. -М., 2004 3 Петров А.А., Бальян Х.В., Трощенко А.Т. Органическая химия. – М., 1974 4 Нейланд О.Я. Органическая химия. – М., 2000 5 Несмеянов А.Н., Несмеянов Н.А. Начало Органической химии. - М., 1974. – т. 1,2. 6 Моррисон Р., Бойд Р. Органическая химия. – М., 2001 7 Череватова Н.К. Органическая химия. ч.I. Уральск, 2003 8 Череватова Н.К. Органическая химия. ч. II Уральск, 2004 9 Череватова Н.К. Органическая химия. ч. I-III Уральск, 2005 10 Череватова Н.К. Органическая химия. ч. I-IV, Уральск, 2007 11 Череватова Н.К., Жигалин П.В. Практикум по органической химии. Уральск, 2004 12 Васильева Н.В., Буховец С.В., Журавлева Л.Е., Грошева М.П. Задачи и упражнения по органической химии. – М., 1982 13 Смолина Т.А., Васильева Н.В., Куплетская Н.Б. Практические работы по органической химии. – М., 1986 14 Суворов Н.Н. Задачи и упражнения по органической химии. – М., 1988. Лабораторная работа № 1,2 Тема: Техника безопасности при работе с органическими веществами. Качественный анализ органических веществ Содержание лабораторного занятия. Техника безопасности при работе с органическими веществами. Качественный анализ органических веществ: определение углерода, водорода, серы, азота и галогенов. Выполнение упражнений и задач. Литература: 1 Череватова Н.К., Жигалин П.В. Практикум по органической химии. Уральск, 2004 Лабораторная работа № 1. 2 Васильева Н.В., Буховец С.В., Журавлева Л.Е., Грошева М.П. Задачи и упражнения по органической химии. – М., 1974 3 Смолина Т.А., Васильева Н.В., Куплетская Н.Б. Практические работы по органической химии. – М., 1986 4 Суворов Н.Н. Задачи и упражнения по органической химии. – М., 1988. Содержание СРСП (1-4): Производство химических средств защиты растений, химических волокон, пластических масс, синтетических каучуков, синтетических моющих средств, лекарственных препаратов, лаков, красителей и других продуктов. Методы изучения органических веществ. Способы выделения индивидуальных веществ. Качественный и количественный анализ органических соединений. Установление строения физикохимическими методами. Литература: 1 Перекалин В.В., Зонис С.А. Органическая химия. – М., 1982 2 Терней А. Современная органическая химия. -М., 2004 3 Петров А.А., Бальян Х.В., Трощенко А.Т. Органическая химия. – М., 1974 4 Нейланд О.Я. Органическая химия. – М., 2000 5 Несмеянов А.Н., Несмеянов Н.А. Начало Органической химии. - М., 1974. – т. 1,2. 6 Моррисон Р., Бойд Р. Органическая химия. – М., 2001 7 Череватова Н.К. Органическая химия. ч.I. Уральск, 2003 8 Череватова Н.К. Органическая химия. ч. II Уральск, 2004 9 Череватова Н.К. Органическая химия. ч. I-III Уральск, 2005 10 Череватова Н.К. Органическая химия. ч. I-IV, Уральск, 2007 11 Череватова Н.К., Жигалин П.В. Практикум по органической химии. Уральск, 2004 12 Васильева Н.В., Буховец С.В., Журавлева Л.Е., Грошева М.П. Задачи и упражнения по органической химии. – М., 1982 13 Смолина Т.А., Васильева Н.В., Куплетская Н.Б. Практические работы по органической химии. – М., 1986 14 Суворов Н.Н. Задачи и упражнения по органической химии. – М., 1988. Содержание СРС (1-4): Характеристика ковалентной связи: энергия, длина, кратность, полярность, поляризуемость, направление в пространстве. Понятие о валентности, ковалентности, координационном числе. Выполнение задач и упражнений. Литература: 1 Перекалин В.В., Зонис С.А. Органическая химия. – М., 1982 2 Терней А. Современная органическая химия. -М., 2004 3 Петров А.А., Бальян Х.В., Трощенко А.Т. Органическая химия. – М., 1974 4 Нейланд О.Я. Органическая химия. – М., 2000 5 Несмеянов А.Н., Несмеянов Н.А. Начало Органической химии. - М., 1974. – т. 1,2. 6 Моррисон Р., Бойд Р. Органическая химия. – М., 2001 7 Череватова Н.К. Органическая химия. ч.I. Уральск, 2003 8 Череватова Н.К. Органическая химия. ч. II Уральск, 2004 9 Череватова Н.К. Органическая химия. ч. I-III Уральск, 2005 10 Череватова Н.К. Органическая химия. ч. I-IV, Уральск, 2007 11 Череватова Н.К., Жигалин П.В. Практикум по органической химии. Уральск, 2004 12 Васильева Н.В., Буховец С.В., Журавлева Л.Е., Грошева М.П. Задачи и упражнения по органической химии. – М., 1982 13 Смолина Т.А., Васильева Н.В., Куплетская Н.Б. Практические работы по органической химии. – М., 1986 14 Суворов Н.Н. Задачи и упражнения по органической химии. – М., 1988. Неделя 2 Кредит час 4 Лекция №3,4 Тема: Теория направленных валентностей. Изомерия Содержание лекции: Связь между электронной структурой элементов, зарядом их ионов и числом ковалентных связей в молекулах или ионах. Примеры изоэлектронных структур: метан, борогидридный и аммонийный ионы, метильный катион, ион гидроксония, аммиак и др. Теория гибридизации. Три валентных состояния атома углерода, правила для определения гибридизации атомов в молекуле. Тетраэдрическая (sp3)-гибридизация атомов углерода. Распределение электронной плотности в 3 sp - гибридной орбитали. Тетраэдрическая гибридизация атомов кислорода и азота. Электронное строение и валентные углы в молекулах этана, пропана, воды и аммиака. Электронное строение, схема σ – связей в молекулах метана, этана, этилового спирта, метиламина. Полярность связей и полярность молекул. Тригональная (sp2) – гибридизация. Модель молекул с двойной связью, схема σ- и π-связей, валентные углы в молекулах этилена, пропилена, бутадиена. Тригональная гибридизация атомов кислорода и азота. Схема σ- и π-связей в молекулах уксусной кислоты, нитрометана, мочевины и других соединений. Диагональная (sp) – гибридизация. Модель соединений с тройной связью, схема σ- и π-связей в молекулах ацетилена, аллена, оксида углерода (IV). Энергия, длина и поляризуемость простой, двойной и тройной связи в этане, этилене и ацетилене. Зависимость значений электроотрицательности (ЭО) и длины ковалентного радиуса от валентного состояния атома углерода. Энергия, длина и поляризуемость связей С-Н в алканах, алкенах и алкинах. Структурная изомерия (изомерия строения): изомерия строения углеродного скелета, положения функциональной группы, таутомерии и др. Стереоизомерия: конфигурационная и конформационная. Конфигурационная изомерия: оптическая и геометрическая. Оптическая изомерия. Понятие о хиральности асимметрическом центре. Энантиомеры (антиподы), рацематы и диастереомеры. Проекционные формулы Фишера. Абсолютная и относительная конфигурации. Геометрическая изомерия (цис-, транс- или Z – E ) на примере бутена-2. Физические свойства оптических и геометрических изомеров. Конформационная изомерия. Причина заторможенного вращения вокруг σ- связи. Потенциальная кривая – функция диэдрального угла. Понятие о напряжении Питцера. Литература: См. неделя №1. Лабораторная работа № 3,4 Тема: Очистка органических соединений. Определение их важнейших констант Содержание: Перегонка, кристаллизация, перекристаллизация органических веществ. Определение температур плавления и кипения. Выполнение задач и упражнений. Литература: 1 Васильева Н.Н. Органический синтез. М., 1978. 2 Череватова Н.К., Жигалин П.В. Практикум по органической химии. Уральск, 2004 3 Васильева Н.В., Буховец С.В., Журавлева Л.Е., Грошева М.П. Задачи и упражнения по органической химии. – М., 1982 4 Смолина Т.А., Васильева Н.В., Куплетская Н.Б. Практические работы по органической химии. – М., 1986 5 Суворов Н.Н. Задачи и упражнения по органической химии. – М., 1988. Содержание СРСП (1-4): Примеры изоэлектронных структур: метан, борогидридный и аммонийный ионы, метильный катион, ион гидроксония, аммиак и др. Теория гибридизации. Три валентных состояния атома углерода, правила для определения гибридизации атомов в молекуле. Тетраэдрическая гибридизация атомов кислорода и азота. Электронное строение и валентные углы в молекулах этана, пропана, воды и аммиака. Электронное строение, схема σ – связей в молекулах метана, этана, этилового спирта, метиламина. . Модель молекул с двойной связью, схема σ- и π-связей, валентные углы в молекулах этилена, пропилена, бутадиена. Тригональная гибридизация атомов кислорода и азота. Схема σ- и π-связей в молекулах уксусной кислоты, нитрометана, мочевины и других соединений. Модель соединений с тройной связью, схема σ- и π-связей в молекулах ацетилена, аллена, оксида углерода (IV). Энергия, длина и поляризуемость простой, двойной и тройной связи в этане, этилене и ацетилене. Зависимость значений электроотрицательности (ЭО) и длины ковалентного радиуса от валентного состояния атома углерода. Энергия, длина и поляризуемость связей С-Н в алканах, алкенах и алкинах. Структурная изомерия (изомерия строения): изомерия строения углеродного скелета, положения функциональной группы, таутомерии и др. Стереоизомерия: конфигурационная и конформационная. Конфигурационная изомерия: оптическая и геометрическая. Оптическая изомерия. Понятие о хиральности асимметрическом центре. Энантиомеры (антиподы), рацематы и диастереомеры. Проекционные формулы Фишера. Абсолютная и относительная конфигурации. Геометрическая изомерия (цис-, транс- или Z – E ) на примере бутена-2. Физические свойства оптических и геометрических изомеров. Конформационная изомерия. Причина заторможенного вращения вокруг σ- связи. Потенциальная кривая – функция диэдрального угла. Понятие о напряжении Питцера. Литература: См. неделя № 1. Содержание СРС (1-4): Выполнение задач и упражнений по валентным состояниям атомов и изомерии. Литература: См. неделя № 1. Неделя 3 Кредит час 4 Лекция №5,6 Тема: Теория электронных смещений. Классификация органических реакций и соединений Содержание лекции: Индуктивный эффект. Зависимость полярности σ-связи от электроотрицательности элементов. Таблица электроотрицательности по Полингу. Зависимость знака Iэффекта (+I или – I) от ЭО заместителей. Затухание I-эффекта по цепи σ-связей. Влияние индуктивного эффекта на физические и химические свойства. Мезомерный эффект (эффект резонанса или эффект сопряжения). Перераспределение электронной плотности в системе π-связей, стабилизация системы. Неполярные (М) и полярные (+М, –М) мезомерные эффекты. Типы сопряжения: π – π, р – π, σ – π, σ – σ. Предельные (резонансные) структуры, мезоформулы. Вид единой π-молекулярной орбитали (МО), число центров и π – электронов. Энергия резонанса, влияние на устойчивость системы. Влияние мезомерного эффекта на физико-химические свойства. Классификация органических реакций по направлению: присоединение (А), отщепление (Е), замещение (S), перегруппировка. По характеру реагирующих частиц: гомолитические (SR,AR) и гетеролитические (нуклеофильные - SN AN и электрофильные - SE AE). Понятие о субстрате и реагенте, радикальных, нуклеофильных и электрофильных частицах. Понятие о моно-, би- и полимолекулярных реакциях. Литература: См. неделя № 1. Лабораторная работа № 5,6 Тема: Электронные эффекты органических соединений (семинар) Содержание: Индуктивный эффект. Зависимость полярности σ-связи от электроотрицательности элементов. Таблица электроотрицательности по Полингу. Зависимость знака I-эффекта (+I или – I) от ЭО заместителей. Затухание I-эффекта по цепи σ-связей. Влияние индуктивного эффекта на физические и химические свойства. Мезомерный эффект (эффект резонанса или эффект сопряжения). Перераспределение электронной плотности в системе π-связей, стабилизация системы. Неполярные (М) и полярные (+М, –М) мезомерные эффекты. Типы сопряжения: π – π, р – π, σ – π, σ – σ. Классификация органических реакций по направлению: присоединение (А), отщепление (Е), замещение (S), перегруппировка. По характеру реагирующих частиц: гомолитические (SR,AR) и гетеролитические (нуклеофильные - SN AN и электрофильные - SE AE). Понятие о субстрате и реагенте, радикальных, нуклеофильных и электрофильных частицах. Понятие о моно-, би- и полимолекулярных реакциях. Литература: См. неделя № 1. Содержание СРСП (1-4): Таблица электроотрицательности по Полингу. Зависимость знака Iэффекта (+I или – I) от ЭО заместителей. Затухание I-эффекта по цепи σ-связей. Влияние индуктивного эффекта на физические и химические свойства. Мезомерный эффект (эффект резонанса или эффект сопряжения). Перераспределение электронной плотности в системе π-связей, стабилизация системы. Неполярные (М) и полярные (+М, –М) мезомерные эффекты. Типы сопряжения: π – π, р – π, σ – π, σ – σ. Классификация органических реакций по направлению: присоединение (А), отщепление (Е), замещение (S), перегруппировка. По характеру реагирующих частиц: гомолитические (SR,AR) и гетеролитические (нуклеофильные - SN AN и электрофильные - SE AE). Понятие о субстрате и реагенте, радикальных, нуклеофильных и электрофильных частицах. Понятие о моно-, би- и полимолекулярных реакциях. Классификация органических соединений. Ациклические (алифатические), карбоциклические (алициклические и ароматические), гетероциклические. Понятие о функциональных группах. Литература: См. неделя № 1 Содержание СРС (1-4): Выполнение задач и упражнений по электронным эффектам органических соединений, по классификации реакций и соединений. Литература: См. неделя № 1. Неделя 4 Кредит час 4 Лекция №7,8 Тема: Алканы (предельные углеводороды) Содержание лекции: Гомологический ряд метана. Структурная изомерия (изомерия углеродного скелета), оптическая и конформационная изомерия. Вывод структурных формул. Первичные, вторичные и третичные атомы углерода. Номенклатура алканов: историческая, рациональная, международная или систематическая (IUPAC – ИЮПАК). Углеводородные радикалы. Нахождение алканов в природе, их промышленное значение. Лабораторные и промышленные методы выделения и синтеза алканов. Физические и химические свойства алканов. Типы превращений. Радикальные реакции в условиях фотолиза и термолиза. Механизмы реакций радикального замещения (SR). Реакции галогенирования, сульфохлорирования, нитрования (жидкофазное и парофазное), окисления, горения. Дегидрирование алканов. Крекинг. Пиролиз. Понятие о термическом и каталитическом крекинге. Изомеризация н-алканов в изоалканы. Литература: См. неделя № 1. Лабораторная работа № 7,8 Тема: Алканы Содержание: Получение алканов, изучение их химических свойств. Углеводороды жирного ряда (алканы). Изомерия, номенклатура, углеводородные радикалы, получение алканов с сохранением, с уменьшением и увеличением углеродного скелета. Механизмы реакции химических свойств. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №2. Содержание СРСП (1-4):). Гомологический ряд метана. Структурная изомерия (изомерия углеродного скелета), оптическая и конформационная изомерия. Вывод структурных формул. Первичные, вторичные и третичные атомы углерода. Номенклатура алканов: историческая, рациональная, международная или систематическая (IUPAC – ИЮПАК). Углеводородные радикалы. Нахождение алканов в природе, их промышленное значение. Лабораторные и промышленные методы выделения и синтеза алканов. Физические и химические свойства алканов. Типы превращений. Радикальные реакции в условиях фотолиза и термолиза. Механизмы реакций радикального замещения (SR). Реакции галогенирования, сульфохлорирования, нитрования (жидкофазное и парофазное), окисления, горения. Дегидрирование алканов. Крекинг. Пиролиз. Понятие о термическом и каталитическом крекинге. Изомеризация н-алканов в изоалканы. Литература: См. неделя № 1. Содержание СРС (1-4): Выполнение задач и упражнений по теме: «Алканы». Литература: Васильева Н.В.Задачи и упражнения по органической химии. – М., 1982. № 35, 49, 51, 52, 63, 88, 94, 98, 101, 103, 110, 113, 121, 122, 128, 130, 146, 167, 170, 184, 221, 245, 253. Неделя 5 Кредит час 4 Лекция 9,10 Тема: Алкены (этиленовые углеводороды, олефины) Содержание лекции: Гомологический ряд этиленовых углеводородов. Структурная изомерия: углеродного скелета и положения функциональной группы. Пространственная изомерия (цис- и транс-). Номенклатура: историческая, рациональная и систематическая. Способы получения алкенов: крекинг нефтепродуктов, реакции отщепления, гидрирования ацетиленоваых углеводородов. Электронное строение молекул алкенов (этилен, пропилен), схемы σ- и π-связей. Энергетические и геометрические параметры двойной углерод-углеродной связи Химические свойства алкенов. Алкены как основания Льюиса. Реакции электрофильного присоединения к молекулам алкенов, двустадийный механизм реакции (π- и σ-комплексы). Динамический и статический факторы. Правило Марковникова. Исключения из правила Марковникова, эффект Караша (А R). Оксосинтез. Полимеризация (катионная, анионная, радикальная), механизм полимеризации. Катализаторы Циглера-Натта. Теломеризация. Получение высокооктанового топлива. Реакции замещения, хлорирование алкенов при высокой температуре (получение винилхлорида и аллилхлорида). Поливинилхлорид. Окисление алкенов без разрыва С – С –связи (реакция Вагнера и др.). Окисление пропилена с разрывом С – С-связи, озонидное расщепление, установление строения алкенов. Литература: См. неделя № 1 Лабораторная работа № 9,10 Тема: Алкены Содержание: Получение этилена и изучение его химических свойств. Изучение свойств жидких олефинов. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №3. Содержание СРСП (1-4): Гомологический ряд этиленовых углеводородов. Структурная изомерия: углеродного скелета и положения функциональной группы. Пространственная изомерия (цис- и транс-). Номенклатура: историческая, рациональная и систематическая. Способы получения алкенов: крекинг нефтепродуктов, реакции отщепления, гидрирования ацетиленоваых углеводородов. Электронное строение молекул алкенов (этилен, пропилен), схемы σ- и π-связей. Энергетические и геометрические параметры двойной углерод-углеродной связи Химические свойства алкенов. Алкены как основания Льюиса. Реакции электрофильного присоединения к молекулам алкенов, двустадийный механизм реакции (π- и σ-комплексы). Динамический и статический факторы. Правило Марковникова. Исключения из правила Марковникова, эффект Караша (А R). Оксосинтез. Полимеризация (катионная, анионная, радикальная), механизм полимеризации. Катализаторы Циглера-Натта. Теломеризация. Получение высокооктанового топлива. Реакции замещения, хлорирование алкенов при высокой температуре (получение винилхлорида и аллилхлорида). Поливинилхлорид. Окисление алкенов без разрыва С – С –связи (реакция Вагнера и др.). Окисление пропилена с разрывом С – С-связи, озонидное расщепление, установление строения алкенов. Литература: См. неделя № 1 Содержание СРС (1-4): Выполнение задач и упражнений по теме: «Алкены». Оформление результатов эксперимента. Литература: 1 Васильева Н.В.Задачи и упражнения по органической химии. – М., 1982. № 49 (1-5), 51, 52, 53, 63, 72, 86, 88, 94; 2. Решение задач. Контрольная работа на тему «Изомерия и номенклатура предельных углеводородов». 3. Васильева Н.В.Задачи и упражнения по органической химии. – М., 1982. № 98, 101, 103, 110, 113, 114, 116, 118, 122, 128, 130, 146, 170, 189, 221, 225, 245, 253; Неделя 6 Кредит час 4 Лекция №11, 12 Тема: Алкины (ацетиленовые углеводороды) Содержание лекции: Гомологический ряд ацетилена, изомерия, номенклатура. Электронное строение ацетилена, схемы σ- и π-связей, энергетические и геометрические параметры тройной углеродуглеродной связи. Сравнение энергии ионизации (Еи) этилена и ацетилена. Физические свойства ацетиленовых углеводородов. Способы получения алкинов. Получение ацетилена из карбида кальция и крекингом метана. Химические свойства алкинов. Получение ацетиленидов металлов, реактива Иоцича (магнийорганических соединений). Сравнение кислотных свойств спиртов, ацетилена, этилена и этана. Реакции присоединения к алкинам, механизм реакции АЕ (электрофильное присоединение). Реакция Кучерова. Правило Эльтекова – Эрленмейера, понятие о таутомерии (прототропии). Правило Марковникова. Нуклеофильное присоединение спиртов. Олигомеризация (ди-, три-, тетра-) и полимеризации алкинов, полимеры ацетилена. Применение ацетилена. Литература: См. неделя № 1 Лабораторная работа № 11,12 Тема: Алкины (ацетиленовые углеводороды) Содержание: Получение ацетилена, изучение химических свойств ацетилена. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №4. Содержание СРСП (1-4): Гомологический ряд ацетилена, изомерия, номенклатура. Электронное строение ацетилена, схемы σ- и π-связей, энергетические и геометрические параметры тройной углерод-углеродной связи. Реакция Кучерова. Правило Эльтекова – Эрленмейера, понятие о таутомерии (прототропии). Правило Марковникова. Нуклеофильное присоединение спиртов. Олигомеризация (ди-, три-, тетра-) и полимеризации алкинов, полимеры ацетилена. Применение ацетилена. Литература: См. неделя № 1 Содержание СРС (1-4): оформление результатов эксперимента. Выводы эксперимента. Выполнение задач и упражнений по теме: «Алкины». Литература: 1 Васильева Н.В.Задачи и упражнения по органической химии. – М., 1982. № 98, 101, 103, 110, 113, 114, 116, 118, 122, 128, 130, 146, 170, 189, 221, 225, 245, 253; Неделя 7 Кредит час 4 Лекция №13, 14 Тема: Алкадиены. Галогеноалканы Содержание лекции: Диеновые углеводороды. Классификация и номенклатура. Изомерия. Электронное строение 1,3-бутадиена, схемы σ- и π-связей. Неполярный мезомерный эффект (π- πсопряжение). Предельные структуры, мезоформулы, энергия мезомерии (делокализации). Методы синтеза диенов с сопряженными π-связями. Химические свойства 1,3-бутадиеновых углеводородов, реакции 1,4- присоединения (механизмы АЕ и АR). Натуральный каучук, строение, реакция Гарриеса. Пространственное строение натурального каучука и гуттаперчи. Синтетические каучуки: СКБ, СКД,СКИ,СКН. Галогенопроизводные алканов. Гомологические ряды галогеноалканов (алкилгалогенидов), историческая и систематическая номенклатуры. Изомерия углеродной цепи, положения функциональной группы, оптическая и конформационная. Первичные, вторичные и третичные алкилгалогениды. Электронное строение алкилгалогенидов, индуктивный эффект. Дипольные моменты, энергия, полярность и поляризуемость связей С – Х. Химические свойства. Реакции нуклеофильного замещения (SN). Примеры реакций: взаимодействие с водными растворами щелочей, спиртами, аминами, солями цианистоводородной кислоты и др. Механизм реакций SN1 SN2. Сравнение реакционной способности алкилгалогенидов в реакциях SN. Конкурирующие реакции дегидрогалогенирования Е1 и Е2. Правило Зайцева. Влияние различных факторов на направление реакции (замещение и отщепление). Взаимодействие алкилгалогенидов с металлами, реактивом Гриньяра. Восстановление галогеноалканов. Литература: См. неделя № 1 Лабораторная работа № 13, 14 Тема: Диены. Галогеноалканы Содержание: Получение галогеноалканов и изучение их свойств. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №5 Содержание СРСП (1-4): Натуральный каучук, строение, реакция Гарриеса. Пространственное строение натурального каучука и гуттаперчи. Синтетические каучуки: СКБ, СКД,СКИ,СКН. Гомологические ряды галогеноалканов (алкилгалогенидов), историческая и систематическая номенклатуры. Изомерия углеродной цепи, положения функциональной группы, оптическая и конформационная. Физические свойства алкилгалогенидов. Сравнение физических характеристик алканов и алкилгалогенидов. Спектральные характеристики. Способы получения галогеноалканов из спиртов, этиленовых и ацетиленовых углеводородов. Получение полигалогензамещенных алканов. Наиболее важные представители: продукты хлорирования метана, фторпроизводные, фреоны. Литература: См. неделя № 1 Содержание СРС (1-4): Оформление результатов эксперимента. Выполнение задач и упражнений. Литература: Васильева Н.В.Задачи и упражнения по органической химии. – М., 1982. № 296, 299, 300, 308, 315, 321, 324, 337, 340; Неделя 8 Кредит час 4 Лекция №15, 16 Тема: Алканолы (одноатомные спирты) Содержание лекции: Гомологические ряды спиртов. Изомерия углеродной цепи, положения функциональной группы, оптическая и конформационная. Номенклатура: историческая, рациональная (карбинольная) и систематическая. Первичные, вторичные и третичные спирты. Электронное строение этилового спирта. Схема σ-связей, их полярность. Химические свойства спиртов. Теория кислот и оснований Бренстеда - Лоури. Сопоставление силы кислот Н – Наl, Н – О, Н – N, Н – С. Кислотно-основные свойства спиртов. Нуклеофильное замещение группы ОН. Сложные эфиры минеральных кислот (серной, азотной, фосфорной), кислые и средние эфиры. Алкилирование спиртов в кислой и щелочной среде. Реакция дегидратации спиртов (внутримолекулярная, межмолекулярная). Правило Зайцева. Окисление первичных, вторичных и третичных спиртов. Правило Эльтекова. Литература: См. неделя № 1 Лабораторная работа № 15,16 Тема: Алканолы Содержание: Изучение свойств спиртов. Простые эфиры, сложные эфиры минеральных кислот. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №6 Содержание СРСП (1-4): Физические свойства спиртов. Причина повышения температуры кипения спиртов в сравнении с галогеноалканами. Растворимость в воде. Межмолекулярные водородные связи в спиртах. Спектральные характеристики спиртов. Идентификация спиртов. Важнейшие представители, распространение в природе, практическое применение. Простые и сложные эфиры. Электронное строение. Сравнение реакционной способности спиртов и эфиров. Литература: См. неделя № 1 Содержание СРС (1-4): оформление результатов эксперимента. Выводы эксперимента. Производство и применение спиртов. Реферат на тему: «Метанол, этанол, физиологическая активность». Решение задач и упражнений. Литература: Васильева Н.В.Задачи и упражнения по органической химии. – М., 1982. № 342, 344, 348, 353, 364, 413, 419, 398, 423, 448; Неделя 9 Кредит час 4 Лекция №17, 18 Тема: Многоатомные спирты. Простые эфиры Содержание лекции: Двух- и трехатомные спирты. Гликоли, изомерия, номенклатура. Получение гликолей. Глицерин. Способы получения глицерина. Физические и химические свойства диолов и триолов, кислотно-основные свойства. Окисление глицерина, глицерат меди. Нинакон-пинаколиновая перегруппировка. Полигликоли. Простые эфиры. Номенклатура, изомерия. Способы получения простых эфиров. Основные свойства, взаимодействие с галогеноводородными кислотами, серной кислотой. Литература: См. неделя № 1 Лабораторная работа № 17, 18 Тема: Многоатомные спирты. Простые эфиры Содержание: Изучение свойств многоатомных спиртов, простых эфиров. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №7 Содержание СРСП (1-4): Абсолютный эфир. Циклические эфиры (диоксан). Тиоспирты. Тиоэфиры и другие соединения серы. Тиолы или меркаптаны. Получение из галогеноалканов. Превращение в дисульфиды и обратный переход. Тиоэфиры. Сравнение кислотных свойств спиртов, эфиров и тиоэфиров. Литература: См. неделя № 1 Содержание СРС (1-4): Оформление результатов эксперимента. Природные многоатомные спирты. Решение задач и упражнений. Написать реферат по тиоспиртам и эфирам. Литература: Васильева Н.В.Задачи и упражнения по органической химии. – М., 1982. № 342, 344, 348, 353, 364, 413, 419, 398, 423, 448; Неделя 10 Кредит час 4 Лекция №19, 20 Тема: Амины и нитросоединения алифатического ряда Содержание лекции: Амины. Изомерия, номенклатура. Первичные, вторичные и третичные амины, их электронное строение. Четвертичные соли аммония. Стереохимия азота, оптическая изомерия четвертичных аммониевых солей. Получение аминов. Химические свойства аминов. Сопоставление кислотно-основных свойств аминов и спиртов. Реакции алкилирования, ацилирования, действие азотистой кислоты. Термический распад четвертичныз аммониевых солей. Литература: См. неделя № 1 Лабораторная работа № 19,20 Тема: Амины и нитросоединения алифатического ряда Содержание: Получение аминов и изучение их свойств. Изучение свойств нитросоединений. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №11. Содержание СРСП (1): Ди-, три-, тетра-, полиамины. Распространение в природе, практическое значение. Аминоспирты. Этаноламин. Холин. Синтез. Ацетилхолин. Фосфатиды. Биологическое значение. Литература: См. неделя № 1 Содержание СРС (1-4): Оформление результатов эксперимента. Выполнение задач и упражнений. Литература: Васильева Н.В.Задачи и упражнения по органической химии. – М., 1982. № 777, 778, 785, 790, 793, 801, 807, 811, 814, 832, 859. Неделя 11 Кредит час 4 Лекция №21, 22 Тема: Альдегиды и кетоны Содержание лекции: Функциональная карбонильная группа. Гомологические ряды альдегидов и кетонов. Изомерия и номенклатура. Спектральные характеристики альдегидов и кетонов. Электронное строение карбонильной группы (I-, М-эффекты), ее влияние на углеводородный радикал. Полярность и поляризуемость карбонильной группы. Связь строения и свойств карбонильной группы. Способы получения альдегидов и кетонов. Физические и химические свойства альдегидов и кетонов. Нуклеофильное присоединение к карбонильной группе, механизм АN, примеры реакций. Взаимодействие кетонов с гидроксиламином, бекмановская перегруппировка. Реакции с участием αводородного атома. Енолизация альдегидов и кетонов в щелочной и кислой среде. Механизм альдольной конденсации, кротоновая конденсация. Окислительно-восстановительные реакции. Окисление альдегидов и кетонов, правило Попова. Качественные реакции альдегидов: реакция «серебряного зеркала», взаимодействие с гидроксидом меди (П) и фуксинсернистой кислотой. Полимеризация альдегидов: триоксан, паральдегид, параформ, полиформальдегид. Литература: См. неделя № 1 Лабораторная работа № 21,22 Тема: Альдегиды и кетоны Содержание: Получение карбонильных соединений и изучение их свойств. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №8. Содержание СРСП (1-4): Енолизация альдегидов и кетонов в щелочной и кислой среде. Механизм альдольной конденсации, кротоновая конденсация. Окислительно-восстановительные реакции. Окисление альдегидов и кетонов, правило Попова. Качественные реакции альдегидов: реакция «серебряного зеркала», взаимодействие с гидроксидом меди (П) и фуксинсернистой кислотой. Полимеризация альдегидов: триоксан, паральдегид, параформ, полиформальдегид. Важнейшие представители: формальдегид, уксусный альдегид, ацетон. Кетен. Применение. Литература: См. неделя № 1 Содержание СРС (1-4): Оформление результатов эксперимента. Выполнение задач и упражнений. Литература: Васильева Н.В.Задачи и упражнения по органической химии. – М., 1982. № 469, 484, 498, 503, 512, 518, 525; Неделя 12 Кредит час 4 Лекция №23, 24 Тема: Монокарбоновые кислоты. Производные карбоновых кислот Содержание лекции: Гомологический ряд, изомерия, номенклатура (историческая, рациональная, систематическая). Методы синтеза карбоновых кислот. Электронное строение карбоксильной группы: – I-эффект, +М-эффект (р-π-сопряжение), предельные структуры, мезоформула. Взаимное влияние гидроксильной и карбонильной групп. Электронное строение карбоксилат-аниона, предельные структуры, мезоформула. Химические свойства. Кислотные свойства. Сравнение кислотных свойств минеральных кислот, органических кислот, воды, спиртов, аминов. Влияние строения радикалов и заместителей в углеводородной цепи на кислотные свойства карбоновых кислот. Соли. Основные свойства карбоновых кислот. Влияние карбоксильной группы на подвижность α-водородного атома. Нуклеофильное замещение НО-группы в карбоксильной группе. Сравнение свойств карбонильной группы у альдегидов, кетонов и карбоновых кислот. Функциональные производные карбоновых кислот. Нуклеофильное замещение в ацильной группе. Общий механизм нуклеофильного замещения. Хлорангидриды, ангидриды карбоновых кислот; строение, свойства, применение. Сложные эфиры карбоновых кислот, доказательство механизма их синтеза с использованием меченых атомов. Сложные эфиры в природе, их значение в промышленности. Амиды карбоновых кислот. Электронное строение амидов. Сравнение кислотных и основных свойств амидов и аминов. Химические свойства. Мочевина. Сравнение реакционной способности в реакциях нуклеофильного замещения производных карбоновых кислот с учетом индуктивного и мезомерного эффектов в функциональных группах. Литература: См. неделя № 1 Лабораторная работа № 23, 24 Тема: Монокарбоновые кислоты, производные карбоновых кислот Содержание: Получение карбоновых кислот и их производных и изучение их свойств. Получение и свойства предельных высших кислот. Мыла, изучение их свойств. Сложные эфиры. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №9,10 (опыты № 35, 36). Содержание СРСП (1-4): Физические свойства карбоновых кислот. Структура и температура кипения, межмолекулярные водородные связи (димеры). Спектральные характеристики карбоновых кислот. Отдельные представители: муравьиная, уксусная кислоты; получение, свойства, применение. Пальмитиновая, стеариновая, высшие жирные синтетические кислоты. Амиды карбоновых кислот. Электронное строение амидов. Сравнение кислотных и основных свойств амидов и аминов. Химические свойства. Мочевина. Литература: См. неделя № 1 Содержание СРС (1-4): Оформление результатов эксперимента. Выполнение задач и упражнений. Литература: Васильева Н.В.Задачи и упражнения по органической химии. – М., 1982. № 529, 548, 567, 577, 584, 608, 612, 635, 673, 706, 710; Неделя 13 Кредит час 4 Лекция №25, 26 Тема: Элементоорганические соединения. Соединения с двумя или несколькими функциями. Дикарбоновые кислоты Содержание лекции: Элементоорганические соединения. Классификация, номенклатура. Общая характеристика, получение, свойства металлоорганических соединений элементов I, II, III, IV групп. Зависимость химических свойств от степени ионности связи углерод-металл. Использование металлоорганических соединений в органическом синтезе. Непредельные кислоты жирного ряда. Номенклатура, изомерия. Акриловая, метакриловая, кротоновая, изокротоновая, винилуксусная кислоты. Геометрическая (цис-, транс-) изомерия. Реакции присоединения. Полимеризация эфиров акриловой и метакриловой кислот (органическое стекло). Непредельные высшие карбоновые кислоты (олеиновая, элаидиновая, линолевая и линоленовая). Дикарбоновые кислоты. Предельные дикарбоновые кислоты: щавелевая, малоновая, янтарная, глутаровая и адипиновая кислоты. Строение, номенклатура, способы получения. Химические свойства. Сравнение кислотных свойств с монокарбоновыми кислотами. Дегидратация. Декарбоксилирование. Малоновый синтез. Полиэфирные синтетические волокна. Применение. Непредельные дикарбоновые кислоты. Малеиновая и фумаровая кислоты. Отношение к нагреванию. Промышленное использование. Литература: См. неделя № 1 Лабораторная работа №25, 26 Тема: Производные карбоновых кислот. Непредельные и дикарбоновые кислоты Содержание: Жиры, масла. Свойства олеиновой кислоты. Получение и свойства щавелевой кислоты. Малоновая кислота. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №10, опыты № 37, 38, 39, 40. Содержание СРСП (1-4): Элементоорганические соединения. Классификация, номенклатура. Общая характеристика, получение, свойства металлоорганических соединений элементов I, II, III, IV групп. Зависимость химических свойств от степени ионности связи углерод-металл. Использование металлоорганических соединений в органическом синтезе. Непредельные алкилгалогениды. Винилхлорид. Аллилхлорид. Электронное строение, схемы σ- и π-связей, электронные эффекты, предельные структуры, мезоформула. Реакции нуклеофильного замещения, сравнение реакционной способности винилхлорида и аллилхлорида. Жиры. Строение триглицеридов. Гидролиз жиров, гидрогенизация. Мыла, получение из жиров. Синтетические моющие средства, детергенты. Понятие о фосфатидах. Литература: См. неделя № 1 Содержание СРС (1-4): Оформление результатов эксперимента. Выполнение задач и упражнений. Литература: 1 Васильева Н.В.Задачи и упражнения по органической химии. – М., 1982. № 529, 548, 567, 577, 584, 608, 612, 635, 673, 706, 710. 2 Суворов Н.Н. Задачи и упражнения по органической химии. – М., 1988. № 644, 652, 653, 654, 658, 660, 661, 662, 663, 664, 665. Неделя 14 Кредит час 4 Лекция №27, 28 Тема: Оксикарбоновые кислоты и оптическая изомерия Содержание лекции: Изомерия и номенклатура оксикарбоновых кислот. Гликолевая, молочная кислоты. Способы получения. Взаимное влияние гидроксильной и карбоксильной групп, электронные эффекты. Химические свойства. Отношение к нагреванию α-, β-, γ-, δ-оксикислот. Оптическая изомерия оксикислот. Асимметрический атом углерода. Знак вращения и конфигурация. Устройство поляриметра. Оптические изомеры, антиподы, рацематы, диастереомеры. Проекционные формулы Фишера, D- и L-ряды. Винная, мезовинная кислоты, хлоряблочная кислота. Способы разделения рацематов. Распространение в природе. Важнейшие представители. Литература: См. неделя № 1 Лабораторная работа № 27, 28 Тема: Оксикарбоновые кислоты Содержание: Изучение свойств иксикарбоновых кислот Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №12. Содержание СРСП (1-4): Оптическая изомерия оксикислот. Асимметрический атом углерода. Знак вращения и конфигурация. Устройство поляриметра. Оптические изомеры, антиподы, рацематы, диастереомеры. Проекционные формулы Фишера, D- и L-ряды. Винная, мезовинная кислоты, хлоряблочная кислота. Способы разделения рацематов. Распространение в природе. Важнейшие представители. Литература: См. неделя № 1 Содержание СРС (1-4): Оформление результатов эксперимента. Выполнение задач и упражнений. Литература: 1 Васильева Н.В.Задачи и упражнения по органической химии. – М., 1982. № 713, 714, 718, 721, 726, 736, 739, 742, 746, 750. 2 Суворов Н.Н. Задачи и упражнения по органической химии. – М., 1988. № 670, 676, 682, 684, 692, 693, 694, 697, 700, 704. Неделя 15 Кредит час 4 Лекция №29, 30 Тема: Альдегидо- и кетокислоты. Аминокислдоты Содержание лекции: Простейшие альдегидо- и кетокислоты: глиоксиловая и пировиноградная кислоты. Биологическое значение. Ацетоуксусная кислота. Влияние карбонильной группы на кислотные свойства. Получение ацетоуксусного эфира. Таутомерия. Ацетоуксусный эфир – смесь таутомеров. Синтезы на основе ацетоуксусного эфира. Аминокислоты. Изомерия, номенклатура. Оптическая изомерия α-аминокислот. Гидролиз белка. Микробиологический синтез. Биологическое значение α-аминокислот. Химические свойства аминокислот. Амфотерность, образование биполярных ионов. Соли. Комплексные соединения с ионами меди (П). Реакции по карбоксильной гркппе. Реакции по аминогруппе. Отношение к нагреванию α-, β-, γ-, δ-аминокислот. Лактам-лактимная таутомерия. Понятие о полипептидах. Белки. Полиамидные полимеры: капрон, энант. Литература: См. неделя № 1 Лабораторная работа № 29, 30 Тема: Альдегидо- и кетокислоты .Аминокислоты Содержание: Получение кетокислот. Изучение свойств аминокислот, мочевины. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №13. Содержание СРСП (1-4): Простейшие альдегидо- и кетокислоты: глиоксиловая и пировиноградная кислоты. Биологическое значение. Ацетоуксусная кислота. Влияние карбонильной группы на кислотные свойства. Получение ацетоуксусного эфира. Таутомерия. Ацетоуксусный эфир – смесь таутомеров. Синтезы на основе ацетоуксусного эфира. Аминокислоты. Изомерия, номенклатура. Оптическая изомерия α-аминокислот. Гидролиз белка. Микробиологический синтез. Биологическое значение α-аминокислот. Химические свойства аминокислот. Амфотерность, образование биполярных ионов. Соли. Комплексные соединения с ионами меди (П). Реакции по карбоксильной гркппе. Реакции по аминогруппе. Отношение к нагреванию α-, β-, γ-, δ-аминокислот. Лактам-лактимная таутомерия. Понятие о полипептидах. Белки. Полиамидные полимеры: капрон, энант. Литература: См. неделя № 1 Содержание СРС (1-4): Оформление результатов эксперимента. Выполнение задач и упражнений. Литература: 1 Васильева Н.В.Задачи и упражнения по органической химии. – М., 1982. № 777, 778, 785, 790, 793, 801, 807, 811, 814, 832, 859. 2 Васильева Н.В.Задачи и упражнения по органической химии. – М., 1982. № 753, 766, 767, 773, 774, 874, 888, 890, 893, 895. 3 Суворов Н.Н. Задачи и упражнения по органической химии. – М., 1988. № 708, 710, 712, 716, 726, 730, 735, 740, 742, 744. 2. 5Список литературы Основная литература 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. 18. 19. Типовая программа по специальности 050112 «Химия». Органическая химия.- Алматы, 2005 Перекалин В.В., Зонис С.А. Органическая химия.- М., 1982 Терней А. Современная органическая химия. - М., 1979 Петров А.А., Бальян Х.В., Трощенко А.Т. Органическая химия. - М., 1974 Нейланд О.Я. Органическая химия. - М., 1990 Несмеянов А.Н., Несмеянов Н.А. Начало органической химии. - М., 1974 – Т. 1,2 Моррисон Р., Бойд Р. Органическая химия. - М., 1974 Васильева Н.В., Буховец С.В., Журавлева Л.Б., Трошева М.П. Задачи и упражнения по органической химии. - М., 1982 Смолина Т.А., Васильева Н.В., Куплетская Н.Б. Практические работы по органической химии. - М., 1986 Некрасов В.В. Руководство к малому практикуму по органической химии. - М., 1975, 1988 Суворов Н.Н. Задачи и упражнения по органической химии. - М., 1986 Иванов. Практикум по органической химии. - М., 2000 Череватова Н.К. Органическая химия. - ч.1, Уральск, 2001 Васильева Н.В. и др. Практические работы по органической химии. - М., 1978 Череватова Н.К. Органическая химия. - ч. 2, Уральск, 2003 Череватова Н.К., Жигалин П.В. Практикум по органической химии. Уральск, 2004 Череватова Н.К. Органическая химия. - ч. 1-3, Уральск, 2005 Череватова Н.К. Органическая химия. - ч. 1-4, Уральск, 2007. Череватова Н.К. Органическая химия. Электронный учебник. – Уральск, 2007. – 300с. Дополнительная 20. 21. 22. 23. 24. 25. 26. 27. 28. 29. 30. 31. 32. 33. Днепровский А.С., Темников Т.И. Теоретические основы органической химии. - Л., 1979 Робертс Дж., Касерио М. Органическая химия. - М., 1978. т.1,2 Потапов В.М. Стереохимия. - М., 1976 Гроссе. Химия для любознательных. - М., 1985 Гордон А., Форд Р. Спутник химика. - М., 1976 Гаптман З., Грефе Ю., Реманс Х. Органическая химия. - М., 1979 Вацуро К.В., Мищенко Г.Л. Именные реакции в органической химии. - М., 1977 Грандберг И.И. Органическая химия. - М., 1976 Жиряков В.Г. Органическая химия. -М., 1978 Козицына Л.А., Куплетская Н.Б. Применение УФ -, ИК - , ЯМР – и масс – спектрометрии в органической химии. - М., 1979 Беккер Г. Введение в электронную теорию органических реакций. - М., 1977 Некрасов В.В. Практикум по органической химии. - М., 1975 Тедлер Дж., Нехватал А., Джубб А. Промышленная органическая химия. – М., 1977 Березин Б.Д., Березин Д.Б. Курс современной органической химии. – Высшая школа, 2001. 2.6 Информация по оценке знаний Схема оценки знаний по дисциплине «Теоретические основы органической химии» № 1 2 Критерии оценки Посещаемость активность лекциях Выполнение эксперимента и на на Оценка вида (max) % за % работ всего у 0,1 1,5 1 2 3 4 5 6 7 8 9 1 0 1 1 1 2 1 3 1 4 1 5 + + + + + + + + + + + + + + + 0,2 + + + + + + + + + + + + + + + 3,0 Неделя 3 4 5 6 7 8 9 10 11 12 лабораторных занятиях Посещаемость СРСП Выполнение заданий СРСП Выполнение заданий СРС Индивидуальное задание (доклад) Индивидуальное задание (реферат) Контрольная работа Активность на лабораторных занятиях Р1+Р2 Экзамен Итого 0,05 1,5 7,5 + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + 0,5 0,5 7,5 + + + + + + + + + + + + + + + 2,5 5,0 2,5 5,0 7,0 14,0 1 15 + + + + + + + + + + + + + + + + + + + + + 60 40 100 В течение семестра проводятся два рубежных контроля на 8 неделе и на 15 неделе. Максимальный показатель успеваемости студента по рубежным контролям составляет 60%. В конце каждого семестра проводится промежуточная аттестация по учебной дисциплине в виде экзамена. Максимальный показатель успеваемости по промежуточной аттестации (ПА), то есть экзамену, составляет 40%. Итоговая экзаменационная оценка по дисциплине определяется как сумма максимальных показателей успеваемости по рубежным контролям (max. 60%) и промежуточной аттестации, то есть экзамену (max. 40%) составляет 100%. Итоговый экзамен будет проходить в форме тестирования по 25-30 вопросам, охватывающим основное содержание теоретического и практического материала курса. Знания, умения и навыки студентов оцениваются следующим образом Оценка по буквенной системе в баллах в %-ном содержании по традиционной системе А 4,0 95 – 100 Отлично А3,67 90 – 94 В+ 3,33 85 – 89 Хорошо В 3,0 80 – 84 В2,67 75 – 79 С+ 2,33 70 – 74 С 2,0 65 – 69 Удовлетворительно С1,67 60 – 64 Д+ 1,33 55 – 59 Д 1,0 50 – 54 F 0 0 - 49 Неудовлетворительно 2.7 Политика и процедуры Политика курса должна обеспечивать высокую эффективность учебного процесса и обязательна для всех студентов. Каждый преподаватель предъявляет к студентам систему требований, правил поведения студентов на занятиях, взаимоотношений с преподавателем и другими студентами. Требования к студентам: Получение хорошего балла по курсу невозможно без постоянной работы. Это предполагает, что оценка по курсу формируется в течение всего семестра. Вы заинтересованы принимать активное участие в работе во время занятий. Максимальная оценка за все виды работ ставится, если был дан правильный, четкий ответ на поставленные вопросы работа выполнена аккуратно в полном объеме. 1. Посещение Посещение должно быть обязательным. Пропуски занятий отрабатываются в полном объеме занятия, отраженном в учебно-методическом комплексе (УМКД). Пропуски занятий без уважительной причины, в объеме, превышающем треть курса, ведут к исключению с курса. Если большое количество часов занятий пропускается по уважительной причине, то студенту необходимо в полном объеме отработать пропущенные занятия. 2. Поведение в аудитории Студент обязан не опаздывать на занятия, не разговаривать во время занятий, не читать газеты, отключать сотовый телефон, активно участвовать в учебном процессе. 3. Домашнее задание Выполнение домашнего задания обязательно для студентов, и отчетность по домашнему заданию принимается в оговоренное преподавателем время. У студентов, опоздавших во время отчитаться, домашнее задание приниматься не будет. На основе ваших отчетностей будет выведена оценка, которая повлияет на итоговую оценку. 4. Индивидуальные задания Индивидуальные семестровые задания являются обязательными. Они выполняются в виде рефератов и защищаются студентами, в виде собеседования, коллоквиума. Каждое из этих заданий оценивается отдельно и влияет на итоговую оценку. 5. Контрольная работа Выполняется на занятии, сдается в конце занятия, после которого не принимается и не оценивается. 6. Тестирование и собеседование Контроль знаний студентов, главным образом, будет осуществляться посредством решения тестовых заданий 2 раза в семестр. Собеседования должны сдаваться по договоренности с преподавателем. Собеседования по соответствующим темам сдают студенты, пропустившие занятия по какой-то уважительной причине. 2.8 Вопросы для проведения контроля знаний студентов по темам занятий и экзамена 2.8.1 Вопросы для проведения контроля по материалам 1-8 недели: 1) Ковалентная химическая связь, описываемая методом валентных связей и методом молекулярных орбиталей. Основное и валентное состояние атома углерода. 2) Важнейшие критерий ковалентной связи: энергия, длина, полярность, поляризуемость, направленность в пространстве. 3) Донороно-акцепторная связь, семиполярная связь, водородная связь. 4) Понятие об изоэлектронных структурах (углерод, азот, кислород). 5) Теория гибридизации. Тетраэдрическая гибридизация. σ –связь (6 видов). Конформационная изомерия. 6) Тригональная гибридизация. Образование π-связи. Геометрическая изомерия. 7) Диагональная гибридизация на примере ацетилена, аллена, углекислого газа. 8) Индукционный эффект (положительный и отрицательный). Связь с химическими свойствами. 9) Мезомерный эффект (π-π- сопряжение на примере бутадиена – 1,3), (р-π сопряжение на примере хлористого винила), (σ-π сопряжение на примере пропилена). 10) Классификация органических реакций. 11) Классификация органических соединений. 12) Алканы, изомерия, номенклатура. Химические свойства: реакции замещения (галогенирования, нитрования, сульфирования, механизм SR). Реакция расщепления, крекинг термический и каталитический, реакция окисления. 13) Алкены, структурная и геометрическая (цис-транс) изомерия. Синтез олефинов (дегидратация спиртов, правила Зайцева, дегидрогалогенирования галогенопроизводных, дегалогенирования дигалогенопроизводных алканов, дегидрирования предельных углеводородов, металлоорганичкий синтез). Химические свойства олефинов. Гидрирование. Галогенирование (механизм реакции АЕ и АR). Гидрогалогенирование, правило Морковникова. Полимеризация. Реакция замещения. Реакция окисления. 14) Ацетилены. Гомологический ряд, изомерия, номенклатура. Способы получения. Химические свойства (галогенирование, гидрогалогенирование, гидратация- механизм АЕ). Реакция присоединения уксусной кислоты, спирта, цианистоводородной кислоты - механизм АN. Реакция окисления и реакция полимеризации. 15) Диены. Реакции присоединения. Каучук. 16) Галогеноалканы. Гомологический ряд, номенклатура, изомерия. Способы получения из алканов, спиртов, ацетиленовых и этиленовых углеводородов, из альдегтдов, кетонов и сложных эфиров. Химическик свойства. Механизм реакции SN1 , SN2 , E1 , E2 . Сравнение реакционной способности RCl , RBr ,RJ. Сравнение реакционной способности первичных, вторичных и третичных галогеноалканов в реакциях нуклеофильного замещения. 17) Спирты. Гомологический ряд, изомерия, номенклатура. Способы получения из алкилгалогенидов, гидратацией олефинов, через магнийорганический синтез, брожение сахаров. Физические свойства спиртов (температура кипения, растворимость в воде, межмолекулярная водородная связь). Химические свойства. Кислотно-основные у первичных, вторичных и третичных спиртов. Реакции нуклеофильного замещения. Дегидратация, алкилирование, окисление спиртов. 2.8.2 Вопросы для проведения контроля по материалам 9-15 недели: 1) Двухатомные спирты. Получение и свойства этиленгликоля. Глицерин, получение и свойства. Качественная реакция на многоатомные спирты. 2) Простые эфиры. Получение, свойства. 3) Тиоэфиры. Получение, свойства. 4) Амины жирного ряда. Номенклатура. Получение. Химические свойства. 5) Нитросоединения жирного ряда. Строение нитрогруппы. Химические свойства. 6) Элементоорганические соединения. Получение, свойства. 7) Альдегиды и кетоны. Гомологический ряд, номенклатура, изомерия. Электронное строение карбонила. Способы получения (окисление спиртов, пиролиз кальциевых и бариевых солей карбоновых кислот, декарбоксилирование). Сравнение реакционной способности альдегидов и кетонов. Окисление альдегидов и кетонов. Реакции присоединения с гидроксиламином, синильной кислотой и др. Полимеризация альдегидов. Реакция замещения кислорода и α – водородных атомов. 8) Карбоновые кислоты и их производные. Гомологический ряд карбоновых кислот. Изомерия, номенклатура. Электронное строение карбоксильной группы. Способы получения. Физические свойства. Химические свойства: кислотные свойства. Влияние заместителей на подвижность атома водорода. Получение солей. Основные свойства карбоновых кислот. 9) Галогенанигдриды, сложные эфиры. Ангидриды кислот. Амиды кислот. Получение и свойства. 10) Непредельные и дикарбоновые кислоты. Изомерия, номенклатура. Получение, химические свойства. Малоновый эфир. Синтез на его основе. Жиры. Масла. 11) Оксикислоты. Оптическая изомерия. Изомерия, номенклатура. Получения. Химические свойства. отношение α, β, γ –оксикислот к нагреванию. 12) Оптическая изомерия хлоряблочной, молочной и винной кислот. Оптическая активность веществ. Асимметрический атом углерода. 13) Альдегидо- и кетокислоты. Номенклатура. Ацетоуксусная кислота. Ацетоуксусный эфир. Получение. Свойства. Таутомерия. Понятие о СН –кислотах. 14) Аминокислоты. Изомерия, номенклатура. Получение, химические свойства: образование биионов, реакции по карбоксильной и аминогруппам, отношение α, β, γ – аминокислот к нагреванию. 2.8.3 Тематика письменных работ по курсу (рефераты, доклады) Обязательно: 1. Этанол, метанол. Химическая и физиологическая активность (реферат). 2. Тиоспирты. Тиоэфиры. По выбору (доклады 0 2): 1. Каменный уголь – природный источник углеводородов, сырье для синтеза органических веществ. 2. Нефть – природные источники углеводородов, сырье для синтеза органических веществ. 3. Природный газ –природный источник углеводородов, сырье для синтеза органических веществ. 4. Химический состав и классификация нефтей. Крекинг нефти. 5. Химический состав и получение горюче-смазочных материалов из нефти. 6. Синтез и свойства полимеров на основе алкенов, алкинов и их производных. 7. Химическая стабилизация моторных и реактивных топлив. 8. Синтетические каучуки. 9. Применение галогеноалканов в промышленности и медицине. 10. 11. 12. 13. 14. 15. Производство и применение спиртов. Природные многоатомные спирты. Полимерные материалы на основе альдегидов, кетонов и сложных эфиров. Жиры и липиды. Производство маргарина. Сложные эфиры – душистые вещества. Свойства и методы анализа белков. 3. ГРАФИК ВЫПОЛНЕНИЯ И СДАЧИ ЗАДАНИЙ ПО ДИСЦИПЛИНЕ График содержит перечень и виды заданий: Виды индивидуальных работ; Сроки выполнения Формы контроля (тесты, экспресс-опрос, отчет, реферат, доклад и др.) График выполнения и сдачи заданий по дисциплине «Теоретические основы органической химии» № Вид работ Цель содержание задания 1 Реферат (2) 2 Доклад (2) 3 Оппонировани е (2) Выполнение заданий СРСП (всего 14 заданий) Углубленный поиск по теме Основной доклад по теме Содоклад 4 5 6 7 Выполнение заданий СРС (упражнения, конспект) Промежуточны й контроль в виде контрольной работы Экзамен и Баллы Форма контроля Согласно теме Продолжительност ь выполнения и дата (неделя) представления работы Неделя 6,15 5% Реферат Согласно теме Неделя 8, 14 5% Согласно теме семинара Согласно теме Неделя 6, 8, 14, 15 5% Согласно графику времени, отведенному на СРСП по теме 7% Закрепление пройденного материала Согласно теме 7,5% Проверка знаний Согласно теме Согласно графику времени, отведенному на СРС по теме Недели: 8,15 Доклад на семинаре Выступление на семинаре Проверка выполнения задания, умение ответить на вопросы Собеседование Развитие аналитических и познавательных способностей Рекоменду емая литература Комплексная проверка знаний Одна работа оценивает ся в 7% Тест 40% Тест 4.КАРТА УЧЕБНО_МЕТОДИЧЕСКОЙ ОБЕСПЕЧЕННОСТИ Карта обеспеченности дисциплины основной литературой Кафедра Химии и ботаники тьютор Череватова Н.К. Дисциплина «Теоретические основы органической химии» Количество кредитов 2 № Наименование литературы В библиотеке На кафедре Наличие Обеспеченности студентов (%) Электронная версия Примеча ние 1 Типовая программа по специальности 050112 «Химия». Органическая химия.- Алматы, 2005 2 Перекалин В.В., Зонис С.А. Органическая химия.- М., 1982 2 2 100 10 100 Терней А. Современная органическая химия. - М., 1979 1 7 Петров А.А., Бальян Х.В., Трощенко А.Т. Органическая химия. М., 1974 15 100 1 25 4 100 1 25 Васильева Н.В., Буховец С.В., Журавлева Л.Б., Трошева М.П. Задачи и упражнения по органической химии. М., 1982 10 100 Смолина Т.А., Васильева Н.В., Куплетская Н.Б. Практические работы по органической химии. М., 1986 10 100 2 50 Суворов Н.Н. Задачи и упражнения по органической химии. М., 1986 10 100 Иванов. Практикум по органической химии. М., 2000 10 100 Череватова Н.К. Органическая химия. ч.1, Уральск, 2001 10 100 3 4 5 6 Нейланд Органическая М., 1990 О.Я. химия. - Несмеянов А.Н., Несмеянов Н.А. Начало органической химии. М., 1974 – Т. 1,2 7 Моррисон Р., Бойд Р. Органическая химия. М., 1974 8 9 10 11 Некрасов В.В. Руководство к малому практикуму по органической химии. М., 1975, 1988 12 13 14 - - Васильева Н.В. и др. Практические работы по органической химии. М., 1978 5 100 10 100 20 100 10 100 Череватова Н.К. Органическая химия. - ч. 1-4, Уральск, 2007. 10 100 19 Череватова Н.К. Органическая химия. Электронный учебник. – Уральск, 2007. – 300с. 1 100 20 Костарев А.С. Химия для экологов. Электронный учебник. Уральск, 2006.250с. 15 Череватова Н.К. Органическая химия. - ч. 2, Уральск, 2003 16 Череватова Н.К., Жигалин П.В. Практикум по органической химии. Уральск, 2004 17 Череватова Н.К. Органическая химия. - ч. 1-3, Уральск, 2005 1 18 1 1 5. КОНСПЕКТЫ ЛЕКЦИЙ ПО ДИСЦИПЛИНЕ Основное содержание лекций, контрольные вопросы и тесты приведены в соответствующих разделах данного силлабуса с указанием литературы, а также в электронном учебнике автора. Лекция № 1. Тема: Введение. Теория химического строения А.М.Бутлерова Содержание лекции: Предмет органической химии. Изучение соединений углерода. Связь органической химии с другими науками, ее значение для промышленности, культуры, роль в повышении благосостоянии народа. Значение органической химии в формировании материалистических мировоззрений. Теория химического строения А.М.Бутлерова. Основные положения теории. Взаимное влияние атомов в молекуле. Значение теории. Литература: 1. Перекалин В.В., Зонис С.А. Органическая химия. – М., 1982 2. Терней А. Современная органическая химия. -М., 2004 3. Петров А.А., Бальян Х.В., Трощенко А.Т. Органическая химия. – М., 1974 4. Нейланд О.Я. Органическая химия. – М., 2000 5. Несмеянов А.Н., Несмеянов Н.А. Начало Органической химии. - М., 1974. – т. 1,2. 6. Моррисон Р., Бойд Р. Органическая химия. – М., 2001 7. Череватова Н.К. Органическая химия. ч.I. Уральск, 2003 8. Череватова Н.К. Органическая химия. ч. II Уральск, 2004 9. Череватова Н.К. Органическая химия. ч. I-III Уральск, 2005 10. Череватова Н.К. Органическая химия. ч. I-IV, Уральск, 2007 11. Череватова Н.К., Жигалин П.В. Практикум по органической химии. Уральск, 2004 12. Васильева Н.В., Буховец С.В., Журавлева Л.Е., Грошева М.П. Задачи и упражнения по органической химии. – М., 1982 13. Смолина Т.А., Васильева Н.В., Куплетская Н.Б. Практические работы по органической химии. – М., 1986 14. Суворов Н.Н. Задачи и упражнения по органической химии. – М., 1988. Лекция №2 Тема: Электронная теория химической связи Содержание лекции: Влияние на развитие органической химии квантовохимических представлений и физико-химических методов исследования. Ионная и ковалентная связь. Семиполярная связь – комбинация ковалентной и ионной связи. Понятие о водородной связи. Квантовомеханическое описание ковалентной связи. Октетные формулы Льюиса. Понятие об эффективном и формальном зарядах атомов в молекулах. Понятие об изоэлектронных структурах. Литература: 1. Перекалин В.В., Зонис С.А. Органическая химия. – М., 1982 2. Терней А. Современная органическая химия. -М., 2004 3. Петров А.А., Бальян Х.В., Трощенко А.Т. Органическая химия. – М., 1974 4. Нейланд О.Я. Органическая химия. – М., 2000 5. Несмеянов А.Н., Несмеянов Н.А. Начало Органической химии. - М., 1974. – т. 1,2. 6. Моррисон Р., Бойд Р. Органическая химия. – М., 2001 7. Череватова Н.К. Органическая химия. ч.I. Уральск, 2003 8. Череватова Н.К. Органическая химия. ч. II Уральск, 2004 9. Череватова Н.К. Органическая химия. ч. I-III Уральск, 2005 10. Череватова Н.К. Органическая химия. ч. I-IV, Уральск, 2007 11. Череватова Н.К., Жигалин П.В. Практикум по органической химии. Уральск, 2004 12. Васильева Н.В., Буховец С.В., Журавлева Л.Е., Грошева М.П. Задачи и упражнения по органической химии. – М., 1982 13. Смолина Т.А., Васильева Н.В., Куплетская Н.Б. Практические работы по органической химии. – М., 1986 14. Суворов Н.Н. Задачи и упражнения по органической химии. – М., 1988. Лекция №3,4 Тема: Теория направленных валентностей. Изомерия Содержание лекции: Связь между электронной структурой элементов, зарядом их ионов и числом ковалентных связей в молекулах или ионах. Примеры изоэлектронных структур: метан, борогидридный и аммонийный ионы, метильный катион, ион гидроксония, аммиак и др. Теория гибридизации. Три валентных состояния атома углерода, правила для определения гибридизации атомов в молекуле. Тетраэдрическая (sp3)-гибридизация атомов углерода. Распределение электронной плотности в 3 sp - гибридной орбитали. Тетраэдрическая гибридизация атомов кислорода и азота. Электронное строение и валентные углы в молекулах этана, пропана, воды и аммиака. Электронное строение, схема σ – связей в молекулах метана, этана, этилового спирта, метиламина. Полярность связей и полярность молекул. Тригональная (sp2) – гибридизация. Модель молекул с двойной связью, схема σ- и π-связей, валентные углы в молекулах этилена, пропилена, бутадиена. Тригональная гибридизация атомов кислорода и азота. Схема σ- и π-связей в молекулах уксусной кислоты, нитрометана, мочевины и других соединений. Диагональная (sp) – гибридизация. Модель соединений с тройной связью, схема σ- и π-связей в молекулах ацетилена, аллена, оксида углерода (IV). Энергия, длина и поляризуемость простой, двойной и тройной связи в этане, этилене и ацетилене. Зависимость значений электроотрицательности (ЭО) и длины ковалентного радиуса от валентного состояния атома углерода. Энергия, длина и поляризуемость связей С-Н в алканах, алкенах и алкинах. Структурная изомерия (изомерия строения): изомерия строения углеродного скелета, положения функциональной группы, таутомерии и др. Стереоизомерия: конфигурационная и конформационная. Конфигурационная изомерия: оптическая и геометрическая. Оптическая изомерия. Понятие о хиральности асимметрическом центре. Энантиомеры (антиподы), рацематы и диастереомеры. Проекционные формулы Фишера. Абсолютная и относительная конфигурации. Геометрическая изомерия (цис-, транс- или Z – E ) на примере бутена-2. Физические свойства оптических и геометрических изомеров. Конформационная изомерия. Причина заторможенного вращения вокруг σ- связи. Потенциальная кривая – функция диэдрального угла. Понятие о напряжении Питцера. Литература: См. неделя №1. Лекция №5,6 Тема: Теория электронных смещений. Классификация органических реакций и соединений Содержание лекции: Индуктивный эффект. Зависимость полярности σ-связи от электроотрицательности элементов. Таблица электроотрицательности по Полингу. Зависимость знака Iэффекта (+I или – I) от ЭО заместителей. Затухание I-эффекта по цепи σ-связей. Влияние индуктивного эффекта на физические и химические свойства. Мезомерный эффект (эффект резонанса или эффект сопряжения). Перераспределение электронной плотности в системе π-связей, стабилизация системы. Неполярные (М) и полярные (+М, –М) мезомерные эффекты. Типы сопряжения: π – π, р – π, σ – π, σ – σ. Предельные (резонансные) структуры, мезоформулы. Вид единой π-молекулярной орбитали (МО), число центров и π – электронов. Энергия резонанса, влияние на устойчивость системы. Влияние мезомерного эффекта на физико-химические свойства. Классификация органических реакций по направлению: присоединение (А), отщепление (Е), замещение (S), перегруппировка. По характеру реагирующих частиц: гомолитические (SR,AR) и гетеролитические (нуклеофильные - SN AN и электрофильные - SE AE). Понятие о субстрате и реагенте, радикальных, нуклеофильных и электрофильных частицах. Понятие о моно-, би- и полимолекулярных реакциях. Литература: См. неделя № 1. Лекция №7,8 Тема: Алканы (предельные углеводороды) Содержание лекции: Гомологический ряд метана. Структурная изомерия (изомерия углеродного скелета), оптическая и конформационная изомерия. Вывод структурных формул. Первичные, вторичные и третичные атомы углерода. Номенклатура алканов: историческая, рациональная, международная или систематическая (IUPAC – ИЮПАК). Углеводородные радикалы. Нахождение алканов в природе, их промышленное значение. Лабораторные и промышленные методы выделения и синтеза алканов. Физические и химические свойства алканов. Типы превращений. Радикальные реакции в условиях фотолиза и термолиза. Механизмы реакций радикального замещения (SR). Реакции галогенирования, сульфохлорирования, нитрования (жидкофазное и парофазное), окисления, горения. Дегидрирование алканов. Крекинг. Пиролиз. Понятие о термическом и каталитическом крекинге. Изомеризация н-алканов в изоалканы. Литература: См. неделя № 1. Лекция 9,10 Тема: Алкены (этиленовые углеводороды, олефины) Содержание лекции: Гомологический ряд этиленовых углеводородов. Структурная изомерия: углеродного скелета и положения функциональной группы. Пространственная изомерия (цис- и транс-). Номенклатура: историческая, рациональная и систематическая. Способы получения алкенов: крекинг нефтепродуктов, реакции отщепления, гидрирования ацетиленоваых углеводородов. Электронное строение молекул алкенов (этилен, пропилен), схемы σ- и π-связей. Энергетические и геометрические параметры двойной углерод-углеродной связи Химические свойства алкенов. Алкены как основания Льюиса. Реакции электрофильного присоединения к молекулам алкенов, двустадийный механизм реакции (π- и σ-комплексы). Динамический и статический факторы. Правило Марковникова. Исключения из правила Марковникова, эффект Караша (А R). Оксосинтез. Полимеризация (катионная, анионная, радикальная), механизм полимеризации. Катализаторы Циглера-Натта. Теломеризация. Получение высокооктанового топлива. Реакции замещения, хлорирование алкенов при высокой температуре (получение винилхлорида и аллилхлорида). Поливинилхлорид. Окисление алкенов без разрыва С – С –связи (реакция Вагнера и др.). Окисление пропилена с разрывом С – С-связи, озонидное расщепление, установление строения алкенов. Литература: См. неделя № 1 Лекция №11, 12 Тема: Алкины (ацетиленовые углеводороды) Содержание лекции: Гомологический ряд ацетилена, изомерия, номенклатура. Электронное строение ацетилена, схемы σ- и π-связей, энергетические и геометрические параметры тройной углеродуглеродной связи. Сравнение энергии ионизации (Еи) этилена и ацетилена. Физические свойства ацетиленовых углеводородов. Способы получения алкинов. Получение ацетилена из карбида кальция и крекингом метана. Химические свойства алкинов. Получение ацетиленидов металлов, реактива Иоцича (магнийорганических соединений). Сравнение кислотных свойств спиртов, ацетилена, этилена и этана. Реакции присоединения к алкинам, механизм реакции АЕ (электрофильное присоединение). Реакция Кучерова. Правило Эльтекова – Эрленмейера, понятие о таутомерии (прототропии). Правило Марковникова. Нуклеофильное присоединение спиртов. Олигомеризация (ди-, три-, тетра-) и полимеризации алкинов, полимеры ацетилена. Применение ацетилена. Литература: См. неделя № 1 Лекция №13, 14 Тема: Алкадиены. Галогеноалканы Содержание лекции: Диеновые углеводороды. Классификация и номенклатура. Изомерия. Электронное строение 1,3-бутадиена, схемы σ- и π-связей. Неполярный мезомерный эффект (π- πсопряжение). Предельные структуры, мезоформулы, энергия мезомерии (делокализации). Методы синтеза диенов с сопряженными π-связями. Химические свойства 1,3-бутадиеновых углеводородов, реакции 1,4- присоединения (механизмы АЕ и АR). Натуральный каучук, строение, реакция Гарриеса. Пространственное строение натурального каучука и гуттаперчи. Синтетические каучуки: СКБ, СКД,СКИ,СКН. Галогенопроизводные алканов. Гомологические ряды галогеноалканов (алкилгалогенидов), историческая и систематическая номенклатуры. Изомерия углеродной цепи, положения функциональной группы, оптическая и конформационная. Первичные, вторичные и третичные алкилгалогениды. Электронное строение алкилгалогенидов, индуктивный эффект. Дипольные моменты, энергия, полярность и поляризуемость связей С – Х. Химические свойства. Реакции нуклеофильного замещения (SN). Примеры реакций: взаимодействие с водными растворами щелочей, спиртами, аминами, солями цианистоводородной кислоты и др. Механизм реакций SN1 SN2. Сравнение реакционной способности алкилгалогенидов в реакциях SN. Конкурирующие реакции дегидрогалогенирования Е1 и Е2. Правило Зайцева. Влияние различных факторов на направление реакции (замещение и отщепление). Взаимодействие алкилгалогенидов с металлами, реактивом Гриньяра. Восстановление галогеноалканов. Литература: См. неделя № 1 Лекция №15, 16 Тема: Алканолы (одноатомные спирты) Содержание лекции: Гомологические ряды спиртов. Изомерия углеродной цепи, положения функциональной группы, оптическая и конформационная. Номенклатура: историческая, рациональная (карбинольная) и систематическая. Первичные, вторичные и третичные спирты. Электронное строение этилового спирта. Схема σ-связей, их полярность. Химические свойства спиртов. Теория кислот и оснований Бренстеда - Лоури. Сопоставление силы кислот Н – Наl, Н – О, Н – N, Н – С. Кислотно-основные свойства спиртов. Нуклеофильное замещение группы ОН. Сложные эфиры минеральных кислот (серной, азотной, фосфорной), кислые и средние эфиры. Алкилирование спиртов в кислой и щелочной среде. Реакция дегидратации спиртов (внутримолекулярная, межмолекулярная). Правило Зайцева. Окисление первичных, вторичных и третичных спиртов. Правило Эльтекова. Литература: См. неделя № 1 Лекция №17, 18 Тема: Многоатомные спирты. Простые эфиры Содержание лекции: Двух- и трехатомные спирты. Гликоли, изомерия, номенклатура. Получение гликолей. Глицерин. Способы получения глицерина. Физические и химические свойства диолов и триолов, кислотно-основные свойства. Окисление глицерина, глицерат меди. Нинакон-пинаколиновая перегруппировка. Полигликоли. Простые эфиры. Номенклатура, изомерия. Способы получения простых эфиров. Основные свойства, взаимодействие с галогеноводородными кислотами, серной кислотой. Литература: См. неделя № 1 Лекция №19, 20 Тема: Амины и нитросоединения алифатического ряда Содержание лекции: Амины. Изомерия, номенклатура. Первичные, вторичные и третичные амины, их электронное строение. Четвертичные соли аммония. Стереохимия азота, оптическая изомерия четвертичных аммониевых солей. Получение аминов. Химические свойства аминов. Сопоставление кислотно-основных свойств аминов и спиртов. Реакции алкилирования, ацилирования, действие азотистой кислоты. Термический распад четвертичныз аммониевых солей. Литература: См. неделя № 1 Лекция №21, 22 Тема: Альдегиды и кетоны Содержание лекции: Функциональная карбонильная группа. Гомологические ряды альдегидов и кетонов. Изомерия и номенклатура. Спектральные характеристики альдегидов и кетонов. Электронное строение карбонильной группы (I-, М-эффекты), ее влияние на углеводородный радикал. Полярность и поляризуемость карбонильной группы. Связь строения и свойств карбонильной группы. Способы получения альдегидов и кетонов. Физические и химические свойства альдегидов и кетонов. Нуклеофильное присоединение к карбонильной группе, механизм АN, примеры реакций. Взаимодействие кетонов с гидроксиламином, бекмановская перегруппировка. Реакции с участием αводородного атома. Енолизация альдегидов и кетонов в щелочной и кислой среде. Механизм альдольной конденсации, кротоновая конденсация. Окислительно-восстановительные реакции. Окисление альдегидов и кетонов, правило Попова. Качественные реакции альдегидов: реакция «серебряного зеркала», взаимодействие с гидроксидом меди (П) и фуксинсернистой кислотой. Полимеризация альдегидов: триоксан, паральдегид, параформ, полиформальдегид. Литература: См. неделя № 1 Лекция №23, 24 Тема: Монокарбоновые кислоты. Производные карбоновых кислот Содержание лекции: Гомологический ряд, изомерия, номенклатура (историческая, рациональная, систематическая). Методы синтеза карбоновых кислот. Электронное строение карбоксильной группы: – I-эффект, +М-эффект (р-π-сопряжение), предельные структуры, мезоформула. Взаимное влияние гидроксильной и карбонильной групп. Электронное строение карбоксилат-аниона, предельные структуры, мезоформула. Химические свойства. Кислотные свойства. Сравнение кислотных свойств минеральных кислот, органических кислот, воды, спиртов, аминов. Влияние строения радикалов и заместителей в углеводородной цепи на кислотные свойства карбоновых кислот. Соли. Основные свойства карбоновых кислот. Влияние карбоксильной группы на подвижность α-водородного атома. Нуклеофильное замещение НО-группы в карбоксильной группе. Сравнение свойств карбонильной группы у альдегидов, кетонов и карбоновых кислот. Функциональные производные карбоновых кислот. Нуклеофильное замещение в ацильной группе. Общий механизм нуклеофильного замещения. Хлорангидриды, ангидриды карбоновых кислот; строение, свойства, применение. Сложные эфиры карбоновых кислот, доказательство механизма их синтеза с использованием меченых атомов. Сложные эфиры в природе, их значение в промышленности. Амиды карбоновых кислот. Электронное строение амидов. Сравнение кислотных и основных свойств амидов и аминов. Химические свойства. Мочевина. Сравнение реакционной способности в реакциях нуклеофильного замещения производных карбоновых кислот с учетом индуктивного и мезомерного эффектов в функциональных группах. Литература: См. неделя № 1 Лекция №25, 26 Тема: Элементоорганические соединения. Соединения с двумя или несколькими функциями. Дикарбоновые кислоты Содержание лекции: Элементоорганические соединения. Классификация, номенклатура. Общая характеристика, получение, свойства металлоорганических соединений элементов I, II, III, IV групп. Зависимость химических свойств от степени ионности связи углерод-металл. Использование металлоорганических соединений в органическом синтезе. Непредельные кислоты жирного ряда. Номенклатура, изомерия. Акриловая, метакриловая, кротоновая, изокротоновая, винилуксусная кислоты. Геометрическая (цис-, транс-) изомерия. Реакции присоединения. Полимеризация эфиров акриловой и метакриловой кислот (органическое стекло). Непредельные высшие карбоновые кислоты (олеиновая, элаидиновая, линолевая и линоленовая). Дикарбоновые кислоты. Предельные дикарбоновые кислоты: щавелевая, малоновая, янтарная, глутаровая и адипиновая кислоты. Строение, номенклатура, способы получения. Химические свойства. Сравнение кислотных свойств с монокарбоновыми кислотами. Дегидратация. Декарбоксилирование. Малоновый синтез. Полиэфирные синтетические волокна. Применение. Непредельные дикарбоновые кислоты. Малеиновая и фумаровая кислоты. Отношение к нагреванию. Промышленное использование. Литература: См. неделя № 1 Лекция №27, 28 Тема: Оксикарбоновые кислоты и оптическая изомерия Содержание лекции: Изомерия и номенклатура оксикарбоновых кислот. Гликолевая, молочная кислоты. Способы получения. Взаимное влияние гидроксильной и карбоксильной групп, электронные эффекты. Химические свойства. Отношение к нагреванию α-, β-, γ-, δ-оксикислот. Оптическая изомерия оксикислот. Асимметрический атом углерода. Знак вращения и конфигурация. Устройство поляриметра. Оптические изомеры, антиподы, рацематы, диастереомеры. Проекционные формулы Фишера, D- и L-ряды. Винная, мезовинная кислоты, хлоряблочная кислота. Способы разделения рацематов. Распространение в природе. Важнейшие представители. Литература: См. неделя № 1 Лекция №29, 30 Тема: Альдегидо- и кетокислоты. Аминокислдоты Содержание лекции: Простейшие альдегидо- и кетокислоты: глиоксиловая и пировиноградная кислоты. Биологическое значение. Ацетоуксусная кислота. Влияние карбонильной группы на кислотные свойства. Получение ацетоуксусного эфира. Таутомерия. Ацетоуксусный эфир – смесь таутомеров. Синтезы на основе ацетоуксусного эфира. Аминокислоты. Изомерия, номенклатура. Оптическая изомерия α-аминокислот. Гидролиз белка. Микробиологический синтез. Биологическое значение α-аминокислот. Химические свойства аминокислот. Амфотерность, образование биполярных ионов. Соли. Комплексные соединения с ионами меди (П). Реакции по карбоксильной гркппе. Реакции по аминогруппе. Отношение к нагреванию α-, β-, γ-, δ-аминокислот. Лактам-лактимная таутомерия. Понятие о полипептидах. Белки. Полиамидные полимеры: капрон, энант. Литература: См. неделя № 1 6.Планы практических (семинарских) занятий не запланированы 7. МЕТОДИЧЕСКИЕ УКАЗАНИЯ К каждому занятию лабораторного даны подробные методические указания. 8. МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ К ЛАБОРАТОРНЫМ РАБОТАМ Методические рекомендации к лабораторным работам подробно «Теоретическим основам органической химии». изложены в силлабусе по Лабораторная работа № 1,2 Тема: Техника безопасности при работе с органическими веществами. Качественный анализ органических веществ Содержание лабораторного занятия. Техника безопасности при работе с органическими веществами. Качественный анализ органических веществ: определение углерода, водорода, серы, азота и галогенов. Выполнение упражнений и задач. Литература: 1 Череватова Н.К., Жигалин П.В. Практикум по органической химии. Уральск, 2004 Лабораторная работа № 1. 2. Васильева Н.В., Буховец С.В., Журавлева Л.Е., Грошева М.П. Задачи и упражнения по органической химии. – М., 1974 3. 4. Смолина Т.А., Васильева Н.В., Куплетская Н.Б. Практические работы по органической химии. – М., 1986 Суворов Н.Н. Задачи и упражнения по органической химии. – М., 1988. Лабораторная работа № 3,4 Тема: Очистка органических соединений. Определение их важнейших констант Содержание: Перегонка, кристаллизация, перекристаллизация органических веществ. Определение температур плавления и кипения. Выполнение задач и упражнений. Литература: 1 Васильева Н.Н. Органический синтез. М., 1978. 2 Череватова Н.К., Жигалин П.В. Практикум по органической химии. Уральск, 2004 3. Васильева Н.В., Буховец С.В., Журавлева Л.Е., Грошева М.П. Задачи и упражнения по органической химии. – М., 1982 4. Смолина Т.А., Васильева Н.В., Куплетская Н.Б. Практические работы по органической химии. – М., 1986 5 Суворов Н.Н. Задачи и упражнения по органической химии. – М., 1988. Лабораторная работа № 5,6 Тема: Электронные эффекты органических соединений (семинар) Содержание: Индуктивный эффект. Зависимость полярности σ-связи от электроотрицательности элементов. Таблица электроотрицательности по Полингу. Зависимость знака I-эффекта (+I или – I) от ЭО заместителей. Затухание I-эффекта по цепи σ-связей. Влияние индуктивного эффекта на физические и химические свойства. Мезомерный эффект (эффект резонанса или эффект сопряжения). Перераспределение электронной плотности в системе π-связей, стабилизация системы. Неполярные (М) и полярные (+М, –М) мезомерные эффекты. Типы сопряжения: π – π, р – π, σ – π, σ – σ. Классификация органических реакций по направлению: присоединение (А), отщепление (Е), замещение (S), перегруппировка. По характеру реагирующих частиц: гомолитические (SR,AR) и гетеролитические (нуклеофильные - SN AN и электрофильные - SE AE). Понятие о субстрате и реагенте, радикальных, нуклеофильных и электрофильных частицах. Понятие о моно-, би- и полимолекулярных реакциях. Литература: См. неделя № 1. Лабораторная работа № 7,8 Тема: Алканы Содержание: Получение алканов, изучение их химических свойств. Углеводороды жирного ряда (алканы). Изомерия, номенклатура, углеводородные радикалы, получение алканов с сохранением, с уменьшением и увеличением углеродного скелета. Механизмы реакции химических свойств. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №2. Лабораторная работа № 9,10 Тема: Алкены Содержание: Получение этилена и изучение его химических свойств. Изучение свойств жидких олефинов. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №3. Лабораторная работа № 11,12 Тема: Алкины (ацетиленовые углеводороды) Содержание: Получение ацетилена, изучение химических свойств ацетилена. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №4. Лабораторная работа № 13, 14 Тема: Диены. Галогеноалканы Содержание: Получение галогеноалканов и изучение их свойств. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №5. Лабораторная работа № 15,16 Тема: Алканолы Содержание: Изучение свойств спиртов. Простые эфиры, сложные эфиры минеральных кислот. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №6. Лабораторная работа № 17, 18 Тема: Многоатомные спирты. Простые эфиры Содержание: Изучение свойств многоатомных спиртов, простых эфиров. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №7. Лабораторная работа № 19,20 Тема: Амины и нитросоединения алифатического ряда Содержание: Получение аминов и изучение их свойств. Изучение свойств нитросоединений. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №11. Лабораторная работа № 21,22 Тема: Альдегиды и кетоны Содержание: Получение карбонильных соединений и изучение их свойств. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №8. Лабораторная работа № 23, 24 Тема: Монокарбоновые кислоты, производные карбоновых кислот Содержание: Получение карбоновых кислот и их производных и изучение их свойств. Получение и свойства предельных высших кислот. Мыла, изучение их свойств. Сложные эфиры. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №9,10 (опыты № 35, 36). Лабораторная работа №25, 26 Тема: Производные карбоновых кислот. Непредельные и дикарбоновые кислоты Содержание: Жиры, масла. Свойства олеиновой кислоты. Получение и свойства щавелевой кислоты. Малоновая кислота. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №10, опыты № 37, 38, 39, 40. Лабораторная работа № 27, 28 Тема: Оксикарбоновые кислоты Содержание: Изучение свойств иксикарбоновых кислот Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №12. Лабораторная работа № 29, 30 Тема: Альдегидо- и кетокислоты .Аминокислоты Содержание: Получение кетокислот. Изучение свойств аминокислот, мочевины. Литература: Череватова Н.К., Жигалин П.В. Практикум по органической химии.- Уральск,2004. Лабораторная работа №13. 9. МАТЕРИАЛЫ ДЛЯ САМОСТОЯТЕЛЬНОЙ РАБОТЫ ОБУЧАЕМЫХ (СРО) Самостоятельная работа с указанием тем, заданий, форм проведения, объема часов содержится в силлабусе по дисциплине. 10. МЕТОДИЧЕСКИЕ УКАЗАНИЯ ПО ПРОХОЖДЕНИЮ УЧЕБНОЙ, ПРЕДДИПЛОМНОЙ ПРАКТИК, ФОРМЫ ОТЧЕТНОЙ ДОКУМЕНТАЦИИ ПРОИЗВОДСТВЕННОЙ И Изучаемая дисциплина не предусматривает в будущем прохождения каких-либо практик. 11. МАТЕРИАЛЫ ДЛЯ КОНТРОЛЯ ЗНАНИЙ Материалы для контроля знаний представлены в виде рефератов, докладов, сообщений, семинаров и т.д., темы которых и литература подробно изложены в данном силлабусе. Тесты для контроля знаний находятся в базе данных на кафедре химии. Некоторые примеры тестов: Ковалентная связь 1.Ковалентная связь образуется между атомами за счет обобщения электронов: A) двух B) одного C) трех D) четырех 2. Сигма связь образуется при перекрывании орбиталей: A) px – px B) py – py C) pz – pz D) px - pz 3. π- связь образуется при перекрывании орбиталей: A) pz – pz B) px – px C) s – pх D) s – py 4.Семиполярная связь присутствует в следующих группах атомов: А) – NO2 , - SO3H B) - NH2 , -SH C) – OH , - OCH3 D) – N (CH3)2 , -S (CH3) 5. Донорно-акцепторная связь присутствует в следующих группах атомов: A) – NH4+, -OH2+ B) – NH2 , -OH C) - NH4 , -OH2 D) - SR , -OR 6.Гибридизация орбиталей- это: А) смешивание В) перекрывание С) притягивание D) отталкивание 7. Первое валентное состояние атома углерода, это гибридизация: A) sp3 B) sp2 C) sp D) spd 8. Второе валентное состояние атома углерода, это гибридизация: A) sp2 B) sp3 C) sp D) spd 9. Третье валентное состояние атома углерода, это гибридизация: A) sp B) sp2 C) sp3 D) spd 10.Для С-С связи характерна гибридизация атомов углерода: A) sp3 B) sp2 C) sp D) spd 11Для С=С связи характерна гибридизация атомов углерода: A) sp2 B) sp3 C) sp D) spd 12. Для С ≡ С связи характерна гибридизация атомов углерода: A) sp B) sp2 C) sp3 D) spd 13. Электроотрицательность атомов увеличивается в ряду: A) s<sp3<sp2<sp B) sp3< sp2<sp<s C) sp<sp2< s D) s<sp2<sp<sp3 14. Большей поляризуемостью обладает связь: A) С=О B) С-О C) С=С D) С-С 15.Для сигма- связи характерны реакции: A) замещения B) присоединения C) восстановления D) окисления 16. Для π- связи характерна реакция: A) присоединения B) замещения C) восстановления D) окисления 17. Гомолитический разрыв ковалентной связи способствует образованию: A) радикалов B) ионов C) атомов D) молекул 18. Гетеролитический разрыв связи способствует образованию: A) ионов B) атомов C) радикалов D) молекул 19.Органогенами являются следующие атомы: A) C,H, N, O, S, P B) C, H, CI, Na, Ca, Mg C) C, H, Mg, Ca, P, K D) C, H. Fe, Mg ,I, N 20.Водородная связь является: A) взаимодействием через пространство B) ионной C) ковалентной D) ван-дер-ваальсовым взаимодействием Электронные эффекты 21. Индуктивным эффектом является смещение электронной плотности по σ-связи в сторону более: A) электроотрицательных атомов B) выравнивание π- электронной плотности по всей молекуле C) смещение σ- электронов к менее электроотрицательному атому D) выравнивание π- электронов на участке молекулы 22.Мезомерным эффектом является: A) выравнивание π- электронной плотности по всей молекуле B) смещение σ-электронов в сторону более электроотрицательного атома C) смещение σ- электронов в сторону менее электроотрицательного атома D) выравнивание π- электров между двумя атомами 23. СН3−СН2−СН2−СI обладает: A) отрицательным индуктивным эффектом B) положительным индуктивным эффектом C) нулевым индуктивным эффектом D) мезомерным эффектом 24. СН3−СН2−СН2−Na обладает: A) положительным индуктивным эффектом B) отрицательным индуктивным эффектом C) нулевым индуктивным эффектом D) мезомерным эффектом 25.СН3−СН=О обладает: A) σ−π−сопряжением B) индуктивным эффектом C) π−π− сопряжением D) р−π− сопряжения 26.СН2=СН−CI обладает: A) М (р−π) B) М (σ−π) C) М (π−π) D) I 27.СН2=СН−СН=СН2 обладает: A) М (π−π) B) М (σ−π) C) I D) М (р−π) 28. J эффект по цепи: A) затухает B) не затухает C) чередуется D) усиливается 29. М эффект по цепи: A) не затухает B) затухает C) чередуется D) усиливается 30.Нуклеофилы- это: A) доноры электронов B) акцепторы электронов C) радикалы D) атомы 31. Электрофилы –это: A) акцепторы электронов B) доноры электронов C) радикалы D) атомы 32.Отрицательно заряженные частицы являются: A) нуклеофилами B) электрофилами C) радикалами D) атомами 33. Положительно заряженные частицы являются: A) электрофилами B) нуклеофилами C) радикалами D) атомами 34. Реакция СН2=СН2+Br2→ CH2Br−CH2Br является: A) А B) Е C) S D) перегруппировка СН3 | 35. Реакция СН3−С−СН=СН2→СН3−С=С−СН3 относится к: | | | СН3 СН3 СН3 A) перегруппировке B) А C) S D) Е 36.Реакция СН3−СН−СН2−СН3→СН3−СH=СH−СН3 относится к: | Вr A) Е B) S C) А D) перегруппировке 37. Реакция СН4+СІ2→СН3СІ + НСІ относится к: A) S B) А C) Е D) перегруппировке 38.Для бимолекулярной реакции характерны: A) одна стадия; R-первичный B) одна стадия, R-третичный C) две стадии, R-первичный D) две стадии, R-третичный 39.Для мономолекулярных реакций характерны: A) одна стадия, R-третичный B) одна стадия; R-первичный C) две стадии, R-первичный D) две стадии, R-третичный 40.В каком ряду молекулярный эффект убывает: .. .. .. A) N > O >F .. .. .. B) F>O >N .. .. .. C) O>N>F .. .. .. D) F>N>O 41.Устойчивость радикалов уменьшается в ряду: A) (СН3)С-> (СН3)2СН->СН3СН2->СН3>Н B) (СН3)С-> СН3>Н>(СН3)2СН->СН3СН2C) СН3>Н> (СН3)2СН>(СН3)СD) Н>СН3>СН3СН2>(СН3)2СН>(СН3)3С42.Максимальным отрицательным индуктивным эффектом обладает: A) С-J B) С-N C) С-О D) С-Р 12. ПРОГРАММНОЕ И МУЛЬТИМЕДИЙНОЕ СОПРОВОЖДЕНИЕ УЧЕБНЫХ ЗАНЯТИЙ 1. Череватова Н.К. Электронный учебник по органической химии. Корпус № 1, компьютерный зал, корпус №5, ауд.26 2. Костарев А.С. Электронный учебник по химии для экологов. Корпус № 1, компьютерный зал, корпус №5, ауд.26. 13.ПЕРЕЧЕНЬ СПЕЦИАЛИЗИРОВАННЫХ АУДИТОРИЙ, КАБИНЕТОВ И ЛАБОРАТОРИЙ Корпус № 5, аудитория № 25, 13,14, химическая лаборатория ЗКГУ, аудитория № 28.