Гетероспиновые о-семихиноновые комплексы кобальта
advertisement

РОССИЙСКАЯ АКАДЕМИЯ НАУК
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ
УЧРЕЖДЕНИЕ НАУКИ
ИНСТИТУТ МЕТАЛЛООРГАНИЧЕСКОЙ ХИМИИ
ИМ. Г.А. РАЗУВАЕВА РАН
На правах рукописи
Протасенко
Наталья Алексеевна
Гетероспиновые о-семихиноновые комплексы
кобальта, марганца и железа с нейтральными,
анионными и радикальными азотсодержащими
лигандами
02.00.08 – химия элементоорганических соединений
Диссертация на соискание ученой степени кандидата химических наук
Научный руководитель:
доктор химических наук, член-корр. РАН
Черкасов Владимир Кузьмич
Нижний Новгород
2014
Оглавление
Введение ................................................................................................................... 5
Глава I. Литературный обзор ............................................................................... 11
1.1. Некоторые общие способы получения семихиноновых комплексов
переходных металлов ............................................................................... 11
1.2. Гетеролигандные семихиноновые комплексы переходных
металлов ..................................................................................................... 13
1.2.1. Кобальт....................................................................................... 13
1.2.2. Марганец .................................................................................... 24
1.2.3. Железо ........................................................................................ 31
1.3. Формазаны как лиганды в координационной химии. Строение и
координационные возможности формазанов ........................................ 39
1.4. Заключение ............................................................................................. 46
Глава II. Результаты и их обсуждение ................................................................ 48
2.1. Бис-3,6-ди-трет-бутил-о-бензосемихиноновые комплексы
переходных металлов с нейтральными донорными лигандами на
основе замещенных N-метиленанилинов ............................................... 48
2.1.1. Получение и общая характеристика комплексов .................. 48
2.1.2. Строение и свойства пятикоординационных бис-осемихиноновых комплексов на основе 2,6-диметил-N-(тиофен-2илметилен)анилина (L(I)) ................................................................. 51
2.1.3. Строение и свойства пятикоординационных бис-осемихиноновых комплексов на основе N-бензилиден-2,6диизопропиланилина (L(II))............................................................. 57
2.1.4. Строение и свойства бис-о-семихиноновых комплексов с
нейтральными донорными лигандами на основе
алкилзамещенных
N-пиридин-2-илметиленанилинов (L(III)-L(V)) ............................ 62
2
2.2. Бис-3,6-ди-трет-бутил-о-бензосемихиноновые комплексы
переходных металлов с нейтральными донорными лигандами на
основе 5,7-ди-трет-бутилбензоксазола ................................................... 67
2.3. Электрохимиче ские исследования бис-о-семихиноновых
комплексов кобальта(II) с нейтральными донорными лигандами ...... 78
2.4. Бис-3,6-ди-трет-бутил-о-бензосемихиноновые комплексы
переходных металлов с 2,2’-бихинолином и 1,4-ди-трет-бутил-1,4диазабутадиеном ....................................................................................... 80
2.4.1. Строение и свойства бис-3,6-ди-трет-бутил-обензосемихиноновых комплексов кобальта, марганца и железа с
2,2’-бихинолином.............................................................................. 81
2.4.2. Строение и свойства бис-3,6-ди-трет-бутил-обензосемихиноновых комплексов кобальта, марганца и железа с
1,4-ди-трет-бутил-1,4-диазабутадиеном ......................................... 85
2.5. Строение и магнитные свойства бис-о-семихинонового комплекса
кобальта(II) с 1,4-диазабицикло(2,2,2)октаном ..................................... 89
2.6. Гетеролигандные комплексы переходных металлов на основе 3,6-дитрет-бутил-о-бензохинона и формазанов ............................................... 92
2.6.1. Строение и свойства гетеролигандных комплексов кобальта
на основе 3,6-ди-трет-бутил-о-бензохинона и формазанов ......... 97
2.6.2. Моно-о-семихинон-формазанатные комплексы
кобальта(II) ..................................................................................... 105
2.6.3. Строение и свойства гетеролигандных комплексов марганца
на основе 3,6-ди-трет-бутил-о-бензохинона и формазанов ....... 110
2.7. Гетеролигандные комплексы кобальта и марганца на основе 3,6-дитрет-бутил-о-бензохинона
и 6-(4’-пиридил)-2,4-дифенилвердазила............................................... 113
Глава III. Экспериментальная часть .................................................................. 119
3
Выводы ................................................................................................................. 146
Список литературы ............................................................................................. 147
Нумерация соединений ....................................................................................... 162
4
Введение
Актуальность. Создание и дизайн гетероспиновых систем на основе
координационных соединений переходных металлов со стабильными
органическими радикалами представляет собой одно из актуальных
направлений современной химии, сформировавшееся на стыке нескольких
физических и химических дисциплин (магнетизм, химия стабильных
радикалов, элементоорганическая и координационная химия, магнетохимия,
кристаллохимия, супрамолекулярная химия). Гетероспиновыми называют
системы, в которых одновременно содержится несколько различных по своей
природе парамагнитных центров. Эти центры могут отличаться величиной
спина, g-фактором и характером делокализации электронной спиновой
плотности. Наличие нескольких парамагнитных центров в гетероспиновых
молекулах обусловливает повышенный интерес к их магнитным свойствам,
поскольку такие соединения - удобные объекты для изучения тонких
обменных
взаимодействий,
характер
которых
может
регулироваться
молекулярной геометрией. Поиск новых перспективных высокоспиновых
молекул (исходных элементов для формирования магнитных материалов) и
определения факторов, управляющих внутримолекулярными магнитными
обменными взаимодействиями в них, являются одними из частных
исследовательских
задач,
на
пути
к
созданию
молекулярных
ферромагнетиков. Успешное решение данной проблемы открывает путь к
новым перспективным материалам, включая прозрачные и легкие (по
сравнению с традиционными) магнитные материалы, магнитоактивные
сенсоры, новые материалы для записи и хранения информации.
В качестве исходных парамагнитных органических лигандов для
синтеза гетероспиновых соединений переходных металлов большой интерес
представляют о-семихиноновые анион-радикальные лиганды. о-Семихинон
является π-радикалом и образует с атомом металла за счет двух
координационных σ-связей прочный хелатный цикл. Для о-семихиноновых
5
комплексов переходных металлов были обнаружены такие явления как
редокс-изомерия
(внутримолекулярный
перенос
электрона)
и
спин-
кроссовер. Уникальные свойства такого рода комплексов определяются
делокализацией или переносом электрона (заряда) между металлом и
парамагнитным лигандом, а также спиновыми взаимодействиями металл–
лиганд или лиганд–лиганд. При этом можно влиять на распределение зарядов
в системе, варьируя природу иона металла, редокс-потенциал о-хинонового
лиганда
или
путем
введения
в
координационную
сферу
металла
дополнительных лигандов.
В связи с чем, цель диссертационной работы заключалась в поиске и
исследовании новых гетероспиновых молекулярных систем на основе
комплексов переходных металлов с 3,6-ди-трет-бутил-о-бензохиноном.
В соответствии с поставленной целью в работе решались следующие
задачи:
- синтез семихиноновых комплексов переходных металлов первого d-ряда
(кобальта, марганца, железа) с N-донорными лигандами различных типов
(замещенные N-метиленанилины, 1,3-диазадиены, формазаны, вердазилы)
- изучение структуры, электронного строения и магнитных свойств
полученных соединений.
Объекты
и
методы
исследования.
Гетероспиновые
комплексы
переходных металлов (кобальта, марганца и железа) на основе 3,6-ди-третбутил-о-бензохинона
и
азотсодержащих
лигандов
различных
типов:
нейтральных (замещенные N-метиленанилины, пиридин- или тиофензамещенные
5,7-ди-трет-бутилбензоксазолы,
1,4-ди-трет-бутил-1,4-
диазабутадиен, 2,2’-бихинолин, 1,4-диазабицикло(2,2,2)октан), анионных
3-(4-пиридил)-1,5-диарилформазаны)
(1,3,5-триарилформазаны,
и
радикальных (6-(4’-пиридил)-2,4-дифенилвердазил).
В результате проведенных исследований синтезировано более 30 новых
соединений.
Строение
5
соединений
в
кристаллическом
состоянии
6
установлено
методом
рентгеноструктурного
анализа
(РСА).
Для
идентификации соединений и исследования их строения использованы такие
физико-химические методы как, электронная спектроскопия поглощения,
ИК-, ЯМР-, ЭПР-спектроскопия, рентгеноструктурный анализ и измерение
магнитной
восприимчивости.
Исследование
окислительно-
восстановительных характеристик полученных комплексов проводилось
методом циклической вольтамперометрии (ЦВА).
Научная новизна и практическая ценность работы заключается в
следующем:
- Синтезирован широкий ряд новых пяти- и шестикоординационных
бис-3,6-ди-трет-бутил-о-бенхосемихиноновых комплексов кобальта, марганца
и железа вида M(3,6-SQ)2L, где L – нейтральный донорный лиганд. Впервые
охарактеризован с помощью метода РСА пятикоординационный бис-осемихиноновый комплекс кобальта(II).
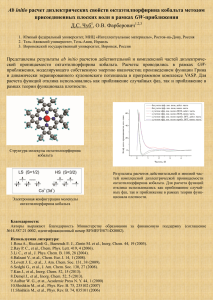
- Исследованы магнитные свойства полученных гетероспиновых бис-осемихиноновых комплексов Co(II), Mn(II), Fe(II). С использованием
экспериментальных
данных
проведено
компьютерное
моделирование
магнитного поведения соединений и определены численные значения
энергетических параметров, характеризующих обменные взаимодействия
между парамагнитными центрами. Показано, что характер температурной
зависимости эффективного магнитного момента комплекса значительно
меняется в зависимости от строения дополнительного лиганда.
- Впервые выделен в индивидуальном виде и охарактеризован с
помощью метода РСА плоско-квадратный комплекс кобальта(II), в котором
центральный атом металла одновременно связан с одним семихиноновым и
одним формазанатным лигандами.
- Разработан удобный синтетический подход для получения смешаннолигандных комплексов переходных металлов на основе 3,6-ди-трет-бутил-о7
бензохинона и формазанов. Установлено, что при взаимодействии с
карбонилом кобальта в присутствии о-хинона 1,3,5-триарилзамещенные
формазаны образуют с металлом хелатный формазанатный цикл, в то время
как
3-(4-пиридил)замещенные
1,5-диарилформазановые
лиганды
координируются в нейтральной форме через атом азота 4-пиридильной
группы.
При
этом
наблюдается
образование
соответственно
бис-о-
семихиноновых или семихинон-катехолатных комплексов кобальта(III).
Вновь полученные смешанно-лигандные комплексы охарактеризованы с
применением
электронной
спектроскопии.
Изучены
спектроскопии
магнитные
и
поглощения,
ИК-,
электрохимические
ЭПР-
свойства
комплексов.
- Впервые синтезированы гетероспиновые комплексы кобальта и
марганца, одновременно содержащие в своем составе два типа радикальных
лигандов:
семихиноновый
соединений
подтверждено
и
вердазильный.
комплексом
Строение
полученных
физико-химических
методов
исследования.
На защиту выносятся следующие положения:
- получение новых гетероспиновых комплексов кобальта, марганца и
железа на основе 3,6-ди-трет-бутил-о-бензохинона и различных N-донорных
лигандов;
- результаты исследования магнитных свойств, молекулярного и
электронного строения полученных соединений.
Личный
вклад
автора.
Анализ
литературных
данных
и
экспериментальная часть работы выполнены лично автором. Постановка
задач, обсуждение результатов и подготовка публикаций проводились
совместно с научным руководителем и соавторами работ. Эксперименты,
связанные с электронной спектроскопией поглощения, выполнены лично
автором или совместно с к.х.н. Лопатиным М.А. (ИМХ РАН), эксперименты
8
ЯМР и ЭПР выполнены д.х.н. Поддельским А.И. (ИМХ РАН), ИК спектры
записаны к.х.н. Кузнецовой О.В. и Хамалетдиновой Н.М. (ИМХ РАН),
рентгеноструктурные эксперименты проведены д.х.н. Фукиным Г.К. (ИМХ
РАН)
и
к.х.н.
Сомовым
Н.В.
(ННГУ
им.
Н.И.
Лобачевского),
электрохимические исследования выполнены к.х.н. Смоляниновым И.В. и
д.х.н., проф. Берберовой Н.Т. (АГТУ), магнетохимические измерения
проведены к.х.н. Богомяковым А.С. (МТЦ СО РАН).
Апробация работы. Результаты исследования были представлены на V,
VI
Международной
конференции
«Высокоспиновые
молекулы
и
молекулярные магнетики» (Нижний Новгород, 2010 г., Ростов-на-Дону, 2012
г.), на XIX Менделеевском съезде по общей и прикладной химии (Волгоград,
2011 г.), на II Молодежной конференции-школе «Физико-химические методы
в химии координационных соединений» в рамках XXV Международной
Чугаевской конференции по координационной химии (Суздаль, 2011 г.), на
Всероссийской научной конференции (с международным участием) «Успехи
синтеза и комплексообразования» (Москва, 2012 г.), на Международной
конференции «Organometallic and coordination chemistry: fundamental and
applied aspects» (Нижний Новгород, 2013 г.), на XVII и XVIII Нижегородских
сессиях молодых ученых (2011, 2012 гг.).
Публикации. Основное содержание работы опубликовано в 4 статьях и
8 тезисах докладов.
Структура диссертации. Диссертационная работа состоит из введения,
литературного обзора, обсуждения результатов, экспериментальной части,
выводов и списка цитируемой литературы из 116 наименований. Работа
изложена на 162 страницах машинописного текста и включает 13 таблиц и 41
рисунок.
9
Изложенный материал и полученные результаты соответствуют пунктам
1., 2. и 6. паспорта специальности 02.00.08 – химия элементоорганических
соединений.
Работа выполена при поддержке грантов РФФИ (№№ 2010-3-00788,
12-03-31367 мол_а), Президента Российской Федерации (НШ-271.2014.3,
НШ-1113.2012.3, МК-614.2011.3, НШ-7065.2010.3) и Федеральной целевой
программы «Научные и научно-педагогические кадры инновационной
России» на 2009-2013 гг. (ГК П982 от 27.05.2010).
10
Глава I. Литературный обзор
1.1. Некоторые общие способы получения семихиноновых комплексов
переходных металлов
Семихиноновые комплексы переходных металлов были впервые
получены в 1966 году по реакции карбонила металла с тетрахлоро-обензохиноном (схема 1.1) [1]:
Схема 1.1
Этот метод синтеза о-семихиноновых комплексов переходных элементов
из о-хинона и соединений нуль-валентных металлов получил большое
распространение. В основном исследовано взаимодействие о-хинона с
карбонилами Со, Ni, Fe, Mn, Cr, Mo, W, приводящее к образованию бис- и
трис-о-семихиноновых комплексов [2-7]. Этот же метод может быть
использован и для синтеза гетеролигандных семихиноновых комплексов
переходных металлов (схема 1.2):
Схема 1.2
где X = O, S, Se, Te [8].
Исследованы
реакции взаимодействия переходных металлов первой
группы (Си и Ag) с раствором о-хинона в присутствии нейтральных n- и донорных лигандов [9,10], процесс может быть отражен следующей схемой:
Схема 1.3
где М =Cu, Ag; L= PPh3, 4,4'-дипиридил
Основным методом синтеза о-семихиноновых комплексов переходных
металлов является обменная реакция соответствующих галогенидов или
11
органогалогенидов
металлов
с
пространственно
затрудненными
о-
семихинонами щелочных металлов (или Тl+1), которые легко образуются из
соответствующего о-хинона и металла (схема 1.4 и схема 1.5) [11]:
Схема 1.4
где М=W, V, La, Fe, Cu [12,13];
Схема 1.5
где
L=
PPh3,
P(OEt)3,
AsPh3,
AsEt3,
PhC≡CPh,
PhC≡CH,
CO,
циклооктадиен-1,5 (COD) [14]
Другой способ получения о-семихиноновых производных переходных
металлов заключается в окислении различных катехолатных соединений. Для
получения трис-о-семихиноновых комплексов авторы [15] использовали
реакцию, представленную на следующей схеме:
Схема 1.6
где M = Cr, Mo, W, Ti, V, Fe, La; (О) = О2, J2, К3[Ре(CN)6] и др.
Известны реакции окислительно-восстановительного вытеснения одного
семихинона другим, более электроноакцепторным [13,14]. В работе [16]
рассмотрены реакции замещения семихиноновых лигандов в комплексах
родия (схема 1.7):
Схема 1.7
12
где
Q = 3,6-ди-трет-бутил-о-бензохинон, SQ = 3,6-ди-трет-бутил-о-
бензосемихинон, Q’ = перхлороксантренхинон-1,2, SQ’ = соответствующий
анион-радикал.
Можно
использовать
реакции,
связанные
с
изменениями,
происходящими в координационной сфере металла и не затрагивающие осемихинонового лиганда (схема 1.8) [16]:
Схема 1.8
(CO)2Rh(SQ)
PPh3
(PPh3)(CO)Rh(SQ)
- CO
PPh3
(PPh3)2(CO)Rh(SQ)
Гетеролигандные семихиноновые комплексы переходных металлов
можно получить по обменной реакции между трис-о-семихинолятом металла
и нейтральным лигандом (схема 1.9) [2,13-14]:
Схема 1.9
Co(3,6-SQ)3
L
Co(3,6-Cat)(3,6-SQ)L
- 3,6Q
L = 2,2'-дипиридин [17].
1.2. Гетеролигандные семихиноновые комплексы переходных металлов
1.2.1. Кобальт
При изучении взаимодействия карбонилов переходных металлов с 9,10фенантренхиноном
Флориани
пятикоординационные
(Floriani)
семихиноновые
с
сотр.
комплексы
[2]
выделил
кобальта
с
координирующими О-донорными растворителями, такими как ТГФ и
ДМФА. При нагревании полученных комплексов до 140°С в вакууме
происходит
элиминирование
перекристаллизации
из
молекул
пиридина
растворителя,
образуется
а
при
шестикоординационный
комплекс Co(SQ)2(py)2. Данный комплекс неустойчив по отношению к
кислороду воздуха, как в растворе, так и в твердом виде. Полученные
13
соединения были охарактеризованы по данным элементного анализа и ИКспектроскопии.
Направленный синтез гетеролигандных семихиноновых комплексов
кобальта был осуществлен позднее. Так, авторами работы [18] по реакции
тетрамерного [Co(3,5-SQ)2]4 c 2,2'-дипиридилом в толуоле был синтезирован
смешаннолигандный комплекс CoIII(3,5-Cat)(3,5-SQ)(2,2'-bpy). По данным
РСА комплекс имеет геометрию искаженного октаэдра. Центральный атом
металла находится в трехвалентном состоянии. Один из хиноновых лигандов
находится в дианионной катехолатной форме, а другой - в анионрадикальной семихиноновой (длины связей С-О составили в среднем 1.35 и
1.29Å для катехолатного и семихинонового фрагментов соответственно). На
основании данных ЭПР, ЯМР-спектроскопии и магнетохимии авторы
сделали вывод о том, что данный комплекс в растворе существует в виде
равновесной смеси двух изомеров, отличающихся друг от друга валентным
состоянием металла и лиганда (схема 1.10). Это становится возможным за
счет
внутримолекулярного
переноса
электрона
между
металлом
и
координированным хиноновым лигандом.
В работе [19] представлены результаты исследования аналогичного
комплекса Co(3,6-Cat)(3,6-SQ)(2,2'-bpy). Авторы показали, что для него
редокс-изомерный переход наблюдается не только в растворе, но и в твердой
фазе. Обнаружено, что тонкие пластины данного комплекса обратимо
изгибаются под воздействием тепла и света.
Схема 1.10
R
R
Co(III), d6,
низкоспиновый,
S=0
Cat2-, S=0
N
O
Co
O
N
O
R
N
SQ1-, S=1/2
Co
O
O
O
SQ1-, S=1/2
N
Co(II), d7,
высокоспиновый,
S=3/2
O
O
SQ1-, S=1/2
R
14
При температуре 120 К спектр ЭПР данного комплекса имеет вид,
типичный для SQ-комплексов переходных металлов с неспаренным
электроном на лиганде (g┴=2.015, g║=1.994). С повышением температуры
спектр ЭПР уширяется и при температурах выше 260 К становится
ненаблюдаемым.
Были исследованы также магнитные свойства полученного комплекса.
Температурная зависимость магнитного момента Co(3,6-Cat)(3,6-SQ)(2,2'bpy) представляет собой S-образную кривую. С понижением температуры
магнитный момент уменьшается от ~ 4.5 (420 К) до 2.1В (280 К), далее
эфф(Т) практически выходит на плато со значением эфф = 1.95В.
Высокотемпературное значение эффективного магнитного момента близко к
аналогичному значению, полученному для комплекса [Co(3,5-SQ)2]4 в расчете
на фрагмент Co(II)(SQ)2, что отвечает системе спинов Сo(II) S = 3/2, 2SQ
(S1=S2=1/2)
со
слабым
низкотемпературной
области
антиферромагнитным
эфф(Т)
близко
к
обменом.
значению
В
1.73В,
соответствующему одному неспаренному электрону. Это свидетельствует о
переходе бис-семихинонового комплекса Сo(II) в форму семихинонкатехолатного комплекса Сo(III), в котором атом кобальта находится в
низкоспиновом состоянии и диамагнитен, а один неспаренный электрон
находится на семихиноновом лиганде.
Исходя из данных ЭПР и магнитной восприимчивости, авторами был
сделан вывод о том, что в поликристаллическом образце данного комплекса в
исследуемом интервале температур (70-420 К) параллельно происходят два
процесса: переход одной редокс-изомерной формы в другую и изменение
спинового
состояния
подтверждаются
кобальта
также
(т.н.
спин-кроссовер).
рентгеноструктурными
Эти
выводы
исследованиями,
проведенными при температурах 153 и 293 К.
Обнаружение
явления
валентной
таутомерии
способствовало
дальнейшему интенсивному изучению семихиноновых и
семихинон-
катехолатных комплексов кобальта с различными донорными лигандами.
15
Так, работа [20] посвящена описанию серии комплексов кобальта на основе
3,5-ди-трет-бутил-о-бензохинона
и
ряда
дииминовых
лигандов,
обладающих различным редокс-потенциалом. Показано, что комплексы,
содержащие в качестве нейтральных лигандов 4,4’-дифенил-2,2’-дипиридил
и 4,4’-диметил-2,2’-дипиридил, существуют в семихинон-катехолатной
форме, в то время как комплексы с 2,2’-дипиримидином, 2,2’-дипиразином и
1,10-фенантролином
являются
бис-семихиноновыми
при
комнатной
температуре. Исследование при разных температурах электронных спектров
поглощения толуольных растворов указанных выше комплексов показало,
что для всех комплексов в растворе наблюдается равновесие таутомерных
форм CoIII(Cat)(SQ)(L)↔CoII(SQ)2(L). И только один комплекс, в котором в
качестве дополнительного лиганда выступает 1,10-фенантролин, проявляет
способность к редокс-изомерии и в твердом виде. Причем, редокс-изомерный
переход претерпевают толуольный и хлорбензольный сольваты данного
комплекса, тогда как несольватированный CoII(SQ)2(1,10-phen) остается в
бис-семихиноновой форме от 320 до 2 К. Этот факт объясняется авторами с
позиции
изменения
энтропии
системы:
при
валентно-таутомерном
превращении сольватные молекулы растворителя изменяют свое положение
в кристаллической решетке, тем самым вносят свой вклад в ΔS и облегчают
редокс-изомерный переход.
В работе [21] описан комплекс аналогичного состава Co(SQ)2(1,10-phen),
где в качестве SQ-лиганда выступает 3,6-ди-трет-бутил-о-бензосемихинон.
При изменении температуры комплекс также претерпевает обратимый
перенос электрона металл-лиганд и спин-кроссовер в кристаллической фазе.
Редокс-изомерное превращение при ~ 250 К сопровождается фазовым
переходом. Кристаллическая упаковка данного соединения типична для
подобных комплексов: в основе упаковки лежит одномерный мотив из
плоскостей нейтральных N-донорных лигандов, формирующих скошенные
стопки в обрамлении о-хиноновых фрагментов. Существенное отличие
упаковки этого комплекса от его аналогов – отсутствие сольватных молекул
16
растворителя. Плоскости соседних о-фенантролиновых фрагментов в
цепочке кристалла параллельны, а расстояния между ними одинаковы, при
240 и 293 К они составляют 3.359 и 3.462 Å соответственно. В комплексах
Co(3,5-SQ)2(1,10-phen) плоскости соседних phen-лигандов непараллельны
(параллельны через одну), угол между соседними плоскостями равен 2.19 Å
(для толуольного сольвата) и 2.37 Å (для хлорбензольного сольвата).
Расстояния между параллельными плоскостями (через одну) составляют
6.854 Å (половина – 3.427 Å) и 6.926 Å (половина – 3.463 Å) для толуольного
и хлорбензольного сольватов соответственно [20].
Среди семихиноновых комплексов с аналогами 2,2’-дипиридила и 1,10фенантролина следует отметить соединения Co(3,6-SQ)2(NO2-phen) и Co(3,6SQ)2(dafl),
где
NO2-phen
=
5-нитро-1,10-фенантролин,
dafl
=
4,5-
диазафлуорен-9-он. Для них наблюдается нетипичное для подобных
комплексов тригонально-призматическое окружение центрального атома
металла [22].
Основания призмы, в случае комплекса Co(3,6-SQ)2(dafl) (рисунок 1.1)
образованные фрагментами N(1)O(1)O(3) и N(2)O(2)O(4), повернуты друг
относительно друга на 4.2°. Значения длины связей Со-О лежат в интервале
2.005-2.050 Å, что характерно для соединений Со(II). Длины связей Co-N
различаются на 0.24 Å и составляют 2.278(16) Å и 2.518(16) Å
соответственно. Подобная асимметрия наблюдается также для комплекса
Cu(dafl)2C12, поэтому можно отнести ее к свойствам такого рода лигандов.
Структурные характеристики хиноновых фрагментов соответствуют анионрадикальной форме лиганда: значения длин связей С-О лежат в интервале
1.28-1.29 Å, а для шестичленных углеродных колец семихиноновых лигандов
наблюдается хиноидный тип искажения, выражающийся в чередовании длин
связей С-С [23].
17
Рисунок 1.1 Молекулярное строение комплекса Co(3,6-SQ)2(dafl)
Как показали дальнейшие исследования в этой области способностью к
внутримолекулярному переносу электрона между металлом и лигандом
обладают также комплексы с третичными бидентатными аминами [22,24-25].
Исследование серии комплексов вида Co(3,6-SQ)2(N-N), где N-N =
тетраметилметилендиамин
(tmmda),
тетраметилэтилендиамин
(tmeda),
тетраметилпропилендиамин (tmpda), в ряду которых донорная способность
соответствующих азотных лигандов существенно не изменяется, зато
варьируется угол N-Co-N, показало, что самая низкая температура редоксперехода Co(III)/Co(II) как в толуольном растворе, так и в твердой фазе
наблюдается для комплекса Co(3,6-SQ)2(tmpda). Авторы связывают это с
гибкостью шестичленного хелатного цикла Co(tmpda) и положительным
вкладом в ΔS равновесия. Температура редокс-перехода в твердой фазе для
комплексов с tmmda и tmeda более чем на 150 К выше, чем для Co(3,6SQ)2(tmpda), и составляет ~ 350 К.
Для аналогичного комплекса кобальта с тетраметилэтилендиамином, но
на
основе
3,5-ди-трет-бутил-о-бензохинона
наблюдается
явление
фотоиндуцируемой валентной таутомерии (схема 1.11) [26]:
18
Схема 1.11
Время жизни метастабильного состояния при 5 К составляет 175 минут.
В работах, опубликованных за последние пять лет и посвященных
исследованию
семихиноновым
явления
редокс-изомерии,
комплексам
кобальта
много
с
внимания
различными
уделено
замещенными
пиридинами (схема 1.12) [27-30]:
Схема 1.12
Обнаружено, что для серии комплексов с 3,5-диалкоксизамещенными
пиридинами валентно-таутомерные превращения сопровождаются фазовыми
переходами между термодинамически стабильной кристаллической фазой и
расплавом [27]. Авторы [28] функционализировали пиридиновый лиганд
нонил-сложноэфирными группами в положения 3 и 5, что позволило за счет
возможности образования водородных связей между длинными алкильными
заместителями,
получить
[CoIII(C9Espy)2(3,6-SQ)(3,6-Cat)],
полиморфные
где
C9Espy
кристаллы
=
комплекса
динонил-пиридин-3,5-
дикарбоксилат. Комплекс был синтезирован по реакции карбонила кобальта
с 3,6-ди-трет-бутил-о-бензохиноном и C9Espy в толуоле. Из реакционной
смеси после медленного упаривания при 298 К были выделены фиолетовые
кристаллы (фаза К1), а перекристаллизацией из смеси толуол/ацетонитрил
при 253 К были получены полиморфные кристаллы (фаза К2), пригодные для
РСА. Основное различие между фазами К1 и К2 заключается в
кристаллической структуре, при формировании которой большую роль
играют водородные связи. Фазы К1 и К2 имеют разные температуры
19
плавления. Интересен тот факт, что данный комплекс в метастабильной
полиморфной кристаллической фазе демонстрирует феномен двойного
плавления, который сопровождается необычными валентно-таутомерными
превращениями, представленными на схеме 1.13:
Схема 1.13
Исследование ряда семихиноновых комплексов кобальта с паразамещенными пиридинами [29,30], показало, что для тех производных, где X
= СN, Br, NO2 наблюдается как термо-, так и фото-индуцируемый редоксизомерный переход (схема 1.14):
Схема 1.14
Кристаллические образцы данных комплексов выдерживали при 10 К в
SQUID-магнитометре и облучали белым светом (λ = 400 – 850 нм), при этом
образовывался CoII-изомер. Время жизни такого изомера в случае комплекса
с 4-CN-пиридином составляет 4.1010 с. Затем убирали источник света, а
образец медленно нагревали. Комплексы существуют в форме CoII-изомера
вплоть до 90 К и затем переходят в форму CoIII-изомера. Высокая
20
стабильность
CoII-формы
фото-генерированной
объясняется
авторами
эффектами кристаллической решетки.
Комплекс кобальта с незамещенным пиридином, описанный в [31] был
получен по реакции 3,5-ди-трет-бутилпирокатехина с Co(ClO4)2 в пиридине
в
присутствии
триэтиламина.
По
данным
РСА
при
130
К
кристаллографическая ячейка содержит две независимые молекулы, каждая
из которых представляет собой комплекс трехвалентного кобальта с одним
семихиноновым, одним катехолатным и двумя пиридиновыми лигандами
[CoIII(3,5-SQ)(3,5-Cat)(py)2].0.5py (рисунок 1.2).
Рисунок 1.2. Две независимые молекулы комплекса [CoIII(3,5-SQ)(3,5Cat)(py)2].0.5py
Кристаллографические данные, полученные при 295 К, обнаружили
существенные изменения длин связей в молекуле 1, в то время как длины
связей в молекуле 2 практически не изменились. Расстояния Сo-O и Co-N в
молекуле 1 увеличились в среднем на 0.15Å и составили 2.010(3)-2.042(4)Å и
2.118Å соответственно. Также для молекулы 1 наблюдается укорочение
связей С-О с 1.326(5)-1.338(5)Å до 1.295(6)-1.306(6)Å с одновременным
удлинением связи С(1)-С(2) с 1.425(6)Å до 1.444(7)Å. Все эти изменения
свидетельствуют о том, что с ростом температуры молекула 1 претерпевает
валентно-таутомерное превращение и при 295 К находится уже в форме
[CoII(3,5-SQ)2(py)2], тогда как молекула 2 остается в форме [CoIII(3,5-SQ)(3,521
Cat)(py)2]. Вероятной причиной того, что для молекулы 2 редокс-изомерный
переход не наблюдается, авторы считают наличие межмолекулярных
взаимодействий лиганд(py)-растворитель(py) в форме π-π-стекинга, которые
имеют место только для этой независимой молекулы комплекса.
Большинство описанных в литературе семихиноновых гетеролигандных
комплексов
кобальта
являются
моноядерными.
Би-
и
полиядерные
соединения встречаются гораздо реже. Жанг (Jung) и сотр. в работе [32]
сообщают о синтезе комплексов кобальта на основе 3,5- и 3,6- ди-трет-бутило-бензохинона, где в качестве нейтрального лиганда выступает потенциально
тетрадентатный
1,1,4,7,10,10-гексаметилтриэтилентетрамин
(hmteta),
изображенный на схеме 1.15.
Схема 1.15
Указанные комплексы выделяются в виде биядерных продуктов [Co 2(3,5SQ)4(hmteta)]
установлена
и
[Co2(3,6-SQ)2(3,6-Cat)2(hmteta)],
методом
РСА.
Измерение
структура
температурной
которых
зависимости
эффективного магнитного момента показало, что последний комплекс
подвергается редокс-изомерному переходу в твердой фазе при ~ 330 К.
К полиядерным гетеролигандным семихиноновым комплексам кобальта
можно отнести координационные полимеры. На рисунке 1.3 представлена
кристаллическая
образующегося
структура
в
одномерного
результате
координационного
взаимодействия
полимера,
3,5-ди-трет-
бутилпирокатехина с Co(CH3COO)2.4H2O в присутствии 4,4’-дипиридила
[33].
22
Рисунок 1.3. Кристаллическая структура координационного полимера
[Co(3,5-SQ)(3,5-Cat)(4,4’-bpy)]n
Комплекс аналогичного полимерного строения можно получить по реакции
3,6-ди-трет-бутил-о-бензохинона с Co2(CO)8 и пиразином (pyz) в гексане
[34]. Данные полимерные продукты также обладают способностью к
внутримолекулярному
переносу
электрона
между
металлом
и
координированным хиноновым лигандом.
В работе [35] описан комплекс {[CoIII(3,5-Сat)(3,5-SQ)]2(TPOM)} 8H2O
2C2H5OH, где TPOM = тетракис-(4-пиридилоксиметилен)метан, который
является первым примером двумерного координационного полимера,
обнаруживающего способность к термо- и фотоиндуцируемой валентной
таутомерии (Рисунок 1.4).
Рисунок 1.4. Молекула ТРОМ (слева) и фрагмент кристаллической упаковки
комплекса [CoIII(3,5-Сat)(3,5-SQ)]2(TPOM) (справа)
23
В
литературе
наиболее
подробно
описаны
бис-семихиноновые
комплексы с N-, и О-донорными лигандами, однако, встречаются работы,
посвященные и другим нейтральным лигандам. Так в работе [17] по
обменной реакции с трис-о-семихинолятом кобальта получены биссемихиноновые комплексы, содержащие в качестве нейтрального лиганда
PPh3, AsEt3. Комплексы охарактеризованы по данным ИК и электронной
спектроскопии,
ЭПР
и
магнитной
восприимчивости.
ИК
спектры
традиционны для семихиноновых комплексов переходных металлов и
состоят
из
совокупности
полос
SQ-лиганда
и
координированного
нейтрального лиганда. Характерной особенностью спектров можно назвать
широкую полосу с вершиной 3500-4000 см-1.
Комплексы были исследованы методом ЭПР в растворе и в порошках.
При комнатной температуре, в растворе спектры ЭПР данных соединений
отсутствуют. При охлаждении ниже ~250 К спектр ЭПР появляется в виде
широкой линии без СТС (ΔН~220 Гс). При дальнейшем охлаждении
интенсивность спектра растет без существенного сужения. Спектры ЭПР
порошков комплексов представляют собой симметричные широкие линии
без СТС (g=1.989). С понижением температуры ширина линии уменьшается
(L = PPh3 ΔН(290K)=220 Гс, ΔН(170K) = 40 Гс; L = AsEt3 ΔН(300K) = 174 Гс,
ΔН(176K) = 83 Гс) при одновременном росте интегральной интенсивности. В
этих комплексах редокс-изомерный переход также имеет место не только в
растворе, но и в кристаллической фазе. Это подтверждается температурной
зависимостью магнитного момента комплекса
Co(3,6-SQ)2(PPh3). Его
значение монотонно возрастает с ростом температуры, начиная с плато эфф =
1.6В (90-240 К) до 2.0В при ~400 К.
1.2.2. Марганец
Вскоре
после
семихиноновых
открытия
комплексах
феномена
кобальта
валентной
подобные
таутомерии
исследования
на
были
24
проведены и для родственных соединений марганца [7]. Обнаружено, что
толуольный раствор комплекса MnIV(3,5-Cat)2(py)2 демонстрирует сильный
термохромный эффект. При температурах ниже 240 К раствор окрашен в
темно-фиолетовый цвет, а в электронном спектре поглощения наблюдаются
полосы характерные для Mn(IV) при 824 и 515 нм. С повышением
температуры интенсивность этих полос уменьшается и появляется новая
полоса при 780 нм, цвет раствора при этом становится зелено-коричневым
(298 К). Похожее поведение наблюдалось ранее для комплекса [MnII(3,5SQ)2]4 [36], что позволило авторам сделать вывод о существовании
равновесия (схема 1.16):
Схема 1.16
С целью получить более подробные характеристики Mn(II)-компоненты
данного равновесия, а также для того, чтобы наблюдать возможно
образующуюся
промежуточную
форму
MnIII(Cat)(SQ)(L),
были
синтезированы и исследованы семихиноновые комплексы марганца с такими
N-донорными лигандами как 2,2'-дипиридин (2,2´-bpy), 4,4'-дипиридин (4,4´bpy), 1,10-фенантролин, 5-нитро-1,10-фенантролин (NO2-phen), пиразин и 4трет-бутилпиридин (tBu-py) [37-39].
В качестве метода синтеза комплексов использовали облучение
видимым светом раствора, содержащего Mn2(CO)10, 3,6-ди-трет-бутил-обензохинон и соответствующий нейтральный лиганд. В случае 2,2'дипиридина данная реакция приводит к образованию MnIV(3,6-Cat)2(2,2´bpy), который, в отличие от аналогичного комплекса кобальта, не проявляет
способности к редокс-изомерии. В электронном спектре поглощения,
записанном для твердого образца MnIV(3,6-Cat)2(2,2´-bpy), имеются две
интенсивные полосы при 440 и 750 нм, ответственные за глубокую
фиолетовую окраску комплекса. Эти переходы сопоставимы с теми, что
наблюдались ранее для MnIV(3,5-Cat)2(py)2.
25
Центральный атом марганца в комплексе MnIII(3,6-SQ)(3,6-Cat)(4,4´bpy)2 находится в искаженном октаэдрическом окружении. Средняя длина
связи Mn-O слегка короче, чем в комплексе MnIV(3,6-Cat)2(2,2´-bpy) и
составляет 1.886(4) Å. Длина связи Mn-N равна 2.273(7) Å, что характерно
для высокоспинового Mn(III). Разница в распределении заряда в комплексах
MnIV(3,6-Cat)2(2,2´-bpy) и MnIII(3,6-SQ)(3,6-Cat)(4,4´-bpy)2 могла бы повлиять
на
магнитное
поведение
комплексов.
Однако,
вследствие
антиферромагнитного обмена между SQ-лигандом и металлом, магнитные
свойства двух соединений отличаются незначительно: высокотемпературное
значение магнитного момента комплекса MnIII(3,6-SQ)(3,6-Cat)(4,4´-bpy)2
составляет 4.26В (350 К), низкотемпературное 3.69В (10 К). Основное
спиновое состояние комплекса – квадруплетное (S = 3/2). Электронный
спектр поглощения данного комплекса содержит две интенсивные полосы
при 550 и 880 нм, и одну полосу в инфракрасной области спектра с
максимумом около 2170 нм. Похожие полосы имеются в спектрах трансMnIII(3,6-SQ)(3,6-Cat)(thf)2 (2100 нм) и MnIII(3,6-SQ)3 (2300 нм) [40].
Комплекс
MnII(3,6-SQ)2(NO2-phen)
имеет
геометрию
искаженной
тригональной призмы (рисунок 1.5).
Рисунок 1.5. Молекулярное строение комплексов MnII(3,6-SQ)2(NO2phen) (слева) и MnIII(3,6-SQ)(3,6-Cat)(phen) (справа)
26
Длины связей Mn-O и Mn-N в среднем составляют 2.139(5) Å и 2.290(6)
Å соответственно, что типично для высокоспинового Mn(II) при данном типе
геометрии. Магнитный момент данного комплекса уменьшается с 4.36В при
350 К до 3.50В при 5 К. Основное спиновое состояние комплекса квадруплетное (S = 3/2), что соответствует спиновой системе, состоящей из
высокоспинового Mn(II) (SMn = 3/2) и двух антиферромагнитно связанных
анион-радикальных
поглощения
семихиноновых
лигандов.
Электронный
спектр
MnII(3,6-SQ)2(NO2-phen)
содержит
две
низкой
полосы
интенсивности при 420 и 750 нм.
Использование в качестве нейтрального лиганда незамещенного 1,10фенантролина позволяет получить комплекс, который в твердом виде при
комнатной температуре представляет собой смесь двух редокс-изомеров
MnIV(Cat)2/MnIII(Cat)(SQ). В электронном спектре поглощения твердого
образца комплекса наблюдаются две интенсивные полосы при 438 и 752 нм
(характерные для MnIV) и одна полоса средней интенсивности при 2030 нм
(соответствующая
MnIII-изомеру).
С
понижением
температуры
интенсивность последней уменьшается, что говорит о сдвиге равновесия в
сторону MnIV-изомера (схема 1.17):
Схема 1.17
Аналогичные процессы наблюдаются и для комплекса марганца с 4-третбутилпиридином [38].
Фотолиз в присутствии пиразина смеси Mn2(CO)10/3,6-Q в гексане
позволяет получить полимерный комплекс [Mn(3,6-SQ)(3,6-Cat)(pyz)]n,
который может быть выделен в виде кристаллов двух разных морфологий.
При кристаллизации из чистого гексана образуются тонкие пластинки,
характеризующиеся такой же тетрагональной элементарной ячейкой, как и у
[Co(3,6-SQ)(3,6-Cat)(pyz)]n,
а
при
использовании
смеси
ТГФ/гексан
формируются крупные ромбические кристаллы с моноклинной ячейкой [39].
27
Последние, согласно данным рентгеноструктурных исследований, обладают
характерной для комплексов Mn(III) аксиально вытянутой структурой. Длина
аксиальной связи Mn-N составляет 2.375(5) Å, что немного выше
аналогичного значения для комплекса MnIII(3,6-SQ)(3,6-Cat)(4,4´-bpy)2, и
значительно превышает величины 2.018(3) and 2.034(11) Å, наблюдаемые для
комплексов четырехвалентного марганца MnIV(3,5-Cat)2(py)2 и MnIV(3,6Cat)2(tBu-py)2. Значения длин экваториальных связей
Mn-O хорошо
согласуются с таковыми для комплекса Mn(III) с 4,4’-дипиридином и равны
1.878(3) and 1.885(3) Å. По сравнению же с пиридиновыми комплексами
Mn(IV)
для
полимерного
[MnIII(3,6-SQ)(3,6-Cat)(pyz)]n
наблюдается
незначительное удлинение связей Mn-O на ~ 0.02 Å.
Электронный спектр поглощения твердого образца [Mn(3,6-SQ)(3,6Cat)(pyz)]n при комнатной температуре содержит две интенсивные полосы
при 880 и 2090 нм, характерные для Mn(III)-изомера. С ростом температуры
интенсивность обеих полос уменьшается, и происходит смещение полосы
переноса заряда лиганд-лиганд в область более низких энергий. Такие
изменения свидетельствуют о смещении равновесия в сторону Mn(II)изомера (схема 1.18):
Схема 1.18
В отличие от всех рассмотренных выше комплексов марганца, для
которых удается наблюдать одну пару изомеров (либо MnIV/MnIII, либо
MnIII/MnII),
авторам
работы
[41]
на
примере
комплекса
с
3,5-
дидодецилоксипиридином (C12Opy) удалось зафиксировать все три формы,
вовлеченные в двухступенчатое валентно-таутомерное превращение (схема
1.19).
28
Схема 1.19
Анализ рентгеноструктурных данных и электронных спектров поглощения
кристаллического образца комплекса при 293 К позволяет идентифицировать
его в качестве [MnIV(3,6-Cat)2(C12Opy)2]. При нагревании до 352 К
фиолетовые кристаллы комплекса превращаются в изотропный коричневый
расплав с высокой текучестью, а в ИК-спектре появляется полоса переноса
заряда между лигандами с максимумом поглощения в области 4700 см-1,
характерная для семихинон-катехолатных комплексов Mn(III). Дальнейшее
нагревание расплава приводит к снижению интенсивности указанной полосы
и сдвигу максимума поглощения в область более низких энергий.
Одновременно с этим уменьшается интенсивность полосы поглощения при
1260 см-1, отвечающая валентным колебаниям одинарной С-О связи. Эти
спектральные изменения указывают на тот факт, что в расплаве происходит
уже
вторая
ступень
валентно-таутомерного
превращения,
а именно
частичный переход Mn(III)-формы в Mn(II). При охлаждении расплава
описанные
процессы,
связанные
с
внутримолекулярным
переносом
электрона между металлом и координированным хиноновым лигандом,
протекают в обратном направлении.
Нужно отметить, что не только комплексы на основе 3,5- и 3,6-ди-третбутил-о-бензохинонов подвергаются редокс-изомерным превращениям. В
работе [42] описаны два полимерных комплекса марганца, в которых роль
редокс-активного
лиганда
выполняет
тетрахлоро-о-бензохинон:
29
[Mn2III(H2L1)(Cl4Cat)4•2H2O]n и [Mn2III(H2L2)(Cl4Cat)4•2CH3CN•2H2O]n, где L1 =
N,N’-бис(2-пиридилметил)-1,2-этандиамин, L2 = N,N’-бис(2-пиридилметил)1,3-пропандиамин, Cl4Cat = дианион тетрахлоро-о-бензохинона (схема 1.20).
Схема 1.20
Спектральные характеристики растворов данных комплексов в ДМФА
указывают на наличие таутомерного равновесия (схема 1.21):
Схема 1.21
Кроме того, для твердых образцов были проведены магнетохимические
исследования, которые показали, что комплексы существуют в виде смеси
[Mn2III(Cl4Cat)4)(H2L)]:[Mn2III(Cl4Cat)2(Cl4SQ)2(L)]
с
соотношением
компонентов 12,7:1 и 2,8:1 для комплексов с L1 и L2 соответственно.
Оказалось,
мостикового
что
протонирование
лиганда
приводит
или
к
депротонирование
окислению
или
атома
азота
восстановлению
координированного хинонового лиганда. Для дальнейшего изучения этого
явления были синтезированы и исследованы 2D полимерные комплексы
{[MnIII(H2L3)(Cl4Cat)2][MnIII(Cl4Cat)2(H2O)2]}n (1)
,
{[MnIII(H2L3)(Br4Cat)2][MnIII(Br4Cat)2(H2O)2]•4DMF}n (2)
,
{[MnIII(H2L4)(Br4Cat)2][MnIII(Br4Cat)2(DMF)2]}n (3), где L3 = N,N’-бис(2пиридилметил)-1,4-бутандиамин,
L4
=
N,N’-бис(2-пиридилметил)-1,6-
гександиамин, Br4Cat = дианион тетрабромо-о-бензохинона [43]. С помощью
метода кислотно-основного титрования было установлено влияние pH
раствора комплекса на степень окисления хинонового лиганда в нем. Все три
30
комплекса подвергаются в растворе редокс-изомерным превращениям
согласно следующей схеме (схема 1.22):
Схема 1.22
Важно отметить, что представленные на схеме процессы, происходящие при
изменении pH, сопровождаются кардинальным изменением оптических
свойств. Это позволяет рассматривать данные комплексы в качестве
объектов для создания оптических сенсоров.
1.2.3. Железо
Первые
семихиноновые
комплексы
железа
с
нейтральными
азотсодержащими лигандами были синтезированы Флориани с сотр.
(Floriani) в 1972 году по реакции Fe(9,10-phenSQ)3 с пиридином и 2,2’дипиридином [2]. Полученные соединения были охарактеризованы по
данным элементного анализа и ИК-спектроскопии.
31
Линч и Хендриксон (Lynch, Hendrickson) продолжили исследование
подобных комплексов и получили целый ряд соединений железа на основе
9,10-фенантренхинона и 3,5-ди-трет-бутил-о-бензохинона с различными Nдонорными лигандами [44]. Комплексы FeIII(9,10-phenSQ)(9,10-phenCat)(NN),
где
=
N-N
2,2’-дипиридин,
5,5’-диметил-2,2’-дипиридин,
1,10-
фенантролин, стабильны на воздухе в твердом виде некоторое время, тогда
как в растворе быстро окисляются. Семихинон-катехолатная форма
комплексов подтверждается наличием полосы переноса заряда между
лигандами с максимумом около 1100 нм в ЭСП твердых образцов и
растворов данных комплексов в растворителях с низкой диэлектрической
проницаемостью
(толуол,
ТГФ,
ацетон).
Согласно
данным
57
Fe
мёссбауэровской спектроскопии и магнетохимии железо в этих комплексах
трехвалентное и находится в высокоспиновом состоянии, кроме того
наблюдается антиферромагнитное обменное взаимодействие между Fe(III) и
координированным семихиноновым лигандом.
Комплексы FeIII(3,5-SQ)(3,5-Cat)(N-N), где N-N = пиридин, 2,2’дипиридин, 5,5’-диметил-2,2’-дипиридин, 1,10-фенантролин, этилендиамин
(en), представляют собой олигомерные продукты слаборастворимые в
органических
растворителях.
Измерения
температурной
зависимости
магнитной восприимчивости показали, что при температурах жидкого гелия
(~4.2 К) указанные комплексы диамагнитны. С повышением температуры
значение эффективного магнитного момента растет и достигает величины 4-5
μB при 286 К. Теоретическое значение μэфф, рассчитанное для комплекса
FeIII(3,5-SQ)(3,5-Cat)(N-N)
при
учете
сильного
взаимодействия Fe-SQ, составляет 4.9 μB. Данные
антиферромагнитного
57
Fe мёссбауэровской
спектроскопии однозначно указывают на трехвалентное высокоспиновое
состояние центрального атома железа. В электронных спектрах поглощения
указанных пяти комплексов отсутствует полоса межлигандного переноса
заряда, наблюдаемая для FeIII(9,10-phenSQ)(9,10-phenCat)(N-N). Однако в
поддержку смешанно-лигандного строения комплексов свидетельствуют их
32
ИК-спектры,
которые
характеризуются
наличием
полос
валентных
колебаний как одинарной, так и полуторной С-О связей.
Первым
структурно
охарактеризованным
гетеролигандным
семихиноновым комплексом железа является FeIII(3,6-SQ)(3,6-Cat)(tBu-py)2,
описанный в работе [38]. Молекулярное строение данного комплекса
представлено на рисунке 1.6.
Рисунок 1.6. Молекулярное строение комплекса FeIII(3,6-SQ)(3,6-Cat)(tBupy)2
Значения длин связей Fe-N и Fe-O(1,2) равны соответственно 2.205(5) и
1.968(4), 1.973(5) Å, что типично для высокоспинового Fe(III). Длины связей
С-О в хиноновых фрагментах занимают промежуточное положение между
значениями, наблюдаемыми для семихиноновой и катехолатной форм
лиганда, и составляют 1.307(8) и 1.315(8) Å. Электронный спектр
поглощения раствора комплекса FeIII(3,6-SQ)(3,6-Cat)(tBu-py)2 в смеси
толуол/пиридин 4:1 характеризуется наличием трех полос с максимумами
при 413, 563 и 835 нм. В спектре твердого образца первые две
низкоэнергетические полосы сливаются в одну с максимумом около 538 нм,
при этом положение третьей полосы не изменяется, но заметно возрастает ее
интенсивность. Кроме того, в спектре появляется слабоинтенсивная полоса в
33
области 2100 нм, которая также наблюдается и для аналогичного комплекса
FeIII(3,6-SQ)(3,6-Cat)(py)2.
Семихиноновые
комплексы
железа
с
N-N
хелатными лигандами, описанные ранее в работах [44-46], таким свойством
не обладают. Авторы предполагают, что появление данной полосы в случае
транс-FeIII(3,6-SQ)(3,6-Cat)(L)2 обусловлено переносом заряда Сat→Fe(III).
Железо в ряду переходных металлов располагается между марганцом и
кобальтом, семихиноновые комплексы которых обладают уникальной
способностью к обратимому внутримолекулярному переносу электрона
между металлом и координированным хиноновым лигандом. С целью
обнаружения подобных свойств у соединений железа авторами работы [47]
были проведены исследования серии комплексов общего вида FeIII
(SQ)(Cat)(N-N),
где
N-N
=
2,2'-дипиридин,
N,N,N',N'-
тетраметилэтилендиамин; SQ и Cat - семихиноновые и катехолатные
лиганды полученные из 3,5- и 3,6-ди-трет-бутил-о-бензохинонов.
Кристаллы
Fe(3,6-SQ)(3,6-Cat)(2,2'-bpy),
пригодные
для
рентгеноструктурного анализа, были выращены из смеси CH2Cl2/гексан.
Аналогичный
комплекс
Fe(3,5-SQ)(3,5-Cat)(2,2'-bpy)
удалось выделить
только в виде мелкодисперсного порошка. Кристаллы комплекса Fe(3,6SQ)(3,6-Cat)(2,2'-bpy) изоморфны комплексам CoIII(3,6-SQ)(3,6-Cat)(2,2'-bpy)
и MnIV(3,6-Cat)2(2,2'-bpy), для которых наблюдается явление редоксизомерии как в растворе, так и в твердой фазе. Значения длин связей С-О
лежат в интервале 1.307(5)-1.308(4) Å, что сопоставимо с величинами,
наблюдаемыми для CoIII(3,6-SQ)(3,6-Cat)(2,2'-bpy) [19]. Длины связей Fe-O
(1.971(2)-1.984(2) Å) и Fe-N (2.154(4)Å) типичны для Fe(III).
В случае комплексов Fe(3,5-SQ)(3,5-Cat)(tmeda) и Fe(3,6-SQ)(3,6Cat)(tmeda) кристаллы, пригодные для РСА, удалось получить при
перекристаллизации продукта взаимодействии Fe(CO)5, tmeda и 3,5- или 3,6ди-трет-бутил-о-бензохинона
комплексах
центральный
из
атом
смеси
металла
толуол/пропанол-2.
находится
в
В
обоих
искаженном
октаэдрическом окружении. В отличие от комплекса Fe(3,6-SQ)(3,6-Cat)(2,2'34
bpy), анализ длин связей в хиноновых фрагментах в данном случае позволяет
однозначно определить тип координации лиганда. Средняя длина С-О связи в
комплексах
Fe(3,6-SQ)(3,6-Cat)(tmeda)
и
Fe(3,5-SQ)(3,5-Cat)(tmeda)
в
семихиноновом фрагменте составляет 1.26(2) Å и 1.28(1) Å, а в катехолатном
– 1.35(2) и 1.34(1) Å соответственно.
Авторами
также
представлены
результаты
магнетохимических
исследований. Высокотемпературное значение магнитного момента для
комплекса Fe(3,6-SQ)(3,6-Cat)(2,2'-bpy)
составляет 5.64В (350 К), а
низкотемпературное 0.81В (5 К). Центральный атом Fe(III) находится в
высокоспиновом состоянии (S = 5/2). Значение магнитного момента в
интервале 300-350 К больше теоретического 4.90В для спиновой системы с
S = 2 (при наличии антиферромагнитного обмена между металлом и
семихиноновым лигандом), но меньше теор = 6.16В, рассчитанного для
системы из двух невзаимодействующих спиновых центров: Fe(III) (S = 5/2) и
SQ-лиганд (S = 1/2). Аномальное падение магнитного момента с понижением
температуры авторы объясняют межмолекулярным взаимодействием через
2,2'-bpy лиганды смежных молекул, расположенных друг над другом в
кристаллической упаковке комплекса. Родственный комплекс железа на
основе тетрахлоро-о-бензохинона Fe(Cl4SQ)(Cl4Cat)(bpy) [45] в интервале
300-100 К демонстрирует слабую зависимость эффективного магнитного
момента от температуры. Величина эфф составляет ~ 5.4В (300-100 К), что
сопоставимо со значениями, наблюдаемыми для Fe(3,6-SQ)(3,6-Cat)(2,2'-bpy).
При температурах ниже 50 К происходит увеличение эффективного
магнитного момента, и при 9.4 К его значение достигает 6.15В. Этот факт
авторы объясняют наличием ферромагнитных межмолекулярных обменных
взаимодействий.
Магнитные свойства комплекса Fe(3,6-SQ)(3,6-Cat)(tmeda) и его 3,5-Q
аналога похожи. Магнитный момент в интервале температур 350-20 К
изменяется незначительно с 5.29 до 4.82В и более резко падает до 4.50В при
5 К. В данном случае, в отличие от дипиридиновых производных,
35
межмолекулярный обмен не вносит существенного вклада в магнитное
поведение комплексов.
В электронных спектрах Fe(3,6-SQ)(3,6-Cat)(2,2'-bpy), Fe(3,6-SQ)(3,6Cat)(tmeda) и Fe(3,5-SQ)(3,5-Cat)(tmeda) наблюдается сильная зависимость
поглощения от сольватирующей способности растворителя и незначительная
зависимость от температуры. В инфракрасной области спектра отсутствуют
полосы, являющиеся характерными для подобных комплексов Co(III) и
Mn(III).
Равновесие редокс-изомеров, представленное на схеме 1.23 для членов
серии FeIII(SQ)(Cat)(N-N) не наблюдается.
Схема 1.23
FeIII(N-N)(SQ)(Cat)
FeII(N-N)(SQ)2
Отсутствие редокс-изомерии авторы работы [47] объясняют, сопоставляя
значения термодинамических функций для редокс-пар FeIII/FeII, CoIII/CoII и
MnIV/MnII.
Все рассмотренные выше соединения железа имеют мономерное
строение. В качестве примера биядерного комплекса можно привести димер
[Fe(3,6-SQ)2(μ-OMe)]2 с мостиковыми метокси-группами [48], молекулярная
структура которого представлена на рисунке 1.7. Значения длин связей С-О
лежат в интервале 1.269(7)-1.285(9) Å, что позволяет отнести их к типично
семихиноновым. В соответствии с хиноидным типом искажения структуры,
характерном для анион-радикальной формы лиганда, длины С-С связей в
бензольном кольце неодинаковы: связи C(3)-C(4) и C(5)-C(6) немного короче
остальных. Связи Fe-O типичны для Fe(III), при этом длина связи транс FeOSQ в среднем составляет 2.032(4) Å, а cis Fe-OSQ 2.024(5) Å. Длины
мостиковых Fe-O(5) и Fe-O(5’) связей равны 1.972(5) и 1.975(4) Å
соответственно, что сопоставимо с величиной 1.979(4) Å, наблюдаемой для
родственного биядерного комплекса [Fe(асас)2(μ-OЕt)]2 [49]. Расстояние
36
между атомами железа в димере [Fe(3,6-SQ)2(μ-OMe)]2 составляет 3.093(1) Å,
что несколько меньше, чем в комплексе [Fe(асас)2(μ-OЕt)]2 (3.116(1) Å).
Рисунок 1.7. Молекулярная структура комплекса [Fe(3,6-SQ)2(μ-OMe)]2
Эффективный магнитный момент комплекса [Fe(3,6-SQ)2(μ-OMe)]2
сильно зависит от температуры. Значение μэфф постепенно увеличивается с
1.91μВ при 5 К до 6.04μВ при 350 К. Теоретическая кривая зависимости
эффективного магнитного момента от температуры, наиболее хорошо
согласующаяся с экспериментальными данными, получена при следующих
параметрах: JFe-Fe = - 22.5 см-1, gFe = 2.37 и TIP = 6.1.10-4, что свидетельствует
о наличие антиферромагнитного обменного взаимодействия между атомами
железа внутри димера.
Первым
семихиноновым
комплексом
железа,
демонстрирующим
подобно соединениям кобальта и марганца способность к валентной
таутомерии, является комплекс FeIII(Cl4Cat)(Cl4SQ)(bispicen), где bispicen =
N,N’-бис(2-пиридилметил)-1,2-этандиамин
семихинон-катехолатная
претерпевает
форма
внутримолекулярное
[50].
комплекса
с
Смешанно-лигандная
ростом
редокс-превращение
температуры
и
происходит
образование FeII(Cl4SQ)2(bispicen) изомера, что подтверждается данными ИКи
УФ-спектроскопии. В электронном спектре поглощения раствора
37
комплекса FeIII(Cl4Cat)(Cl4SQ)(bispicen) в метаноле в интервале 250-1100 нм
наблюдаются две интенсивные полосы с максимумами поглощения при 590 и
300 нм. При этом более низкоэнергетическую полосу можно отнести к
переносу заряда Cat→FeIII, а полосу с большей энергией к π-π* переходам в
хиноновом лиганде. В таких растворителях как ацетонитрил и ДМФА
максимум поглощения первой полосы сдвигается до 550 и 570 нм
соответственно, тогда как положение более высокоэнергетической полосы
практически не изменяется. Подобный сольватохромный эффект наблюдался
и ранее для семихиноновых комплексов железа с N-N хелатными лигандами
[44,47]. Однако в данном случае в электронном спектре поглощения раствора
комплекса FeIII(Cl4Cat)(Cl4SQ)(bispicen) в ацетонитриле или ДМФА помимо
двух указанных полос присутствует полоса, обусловленная переносом заряда
между хиноновыми лигандами, находящимися в разных степенях окисления
(Cat→SQ), в области 1932 нм. Такая же полоса с максимумом при 1925 нм
присутствует и в спектре твердого образца комплекса.
Авторами работы [50] было также проведено исследование электронных
спектров поглощения раствора комплекса FeIII(Cl4Cat)(Cl4SQ)(bispicen) в
ДМФА при разных температурах (рисунок 1.8).
Рисунок 1.8. Температурная зависимость электронных спектров
поглощения растворов комплекса FeIII(Cl4Cat)(Cl4SQ)(bispicen) в ДМФА
38
С
ростом
температуры
интенсивность
полосы
с
максимумом
поглощения при 570 нм постепенно снижается, при этом на графике имеется
изобестическая точка при 650 нм. Для полосы в области 1932 нм
температурная зависимость интенсивности аналогичная, изобестическая
точка наблюдается при 1880 нм. Наличие изобестической точки прямо
указывает на присутствие в растворе двух равновесных форм комплекса
(схема 1.24):
Схема 1.24
1.3. Формазаны как лиганды в координационной химии. Строение и
координационные возможности формазанов
Формазанами называют соединения, содержащие азогидразонную
систему связей, общей формулы:
Схема 1.25
Наиболее изучены 1,3,5-тризамещенные формазаны. Традиционно в
химии формазанов заместители при атомах азота N1 и N5 принято обозначать
как R1 и R5, а при атоме углерода в положении 3 – R3 (схема 1.25).
Заместители в формазановом фрагменте перечисляют в порядке увеличения
номеров атомов азогидразонной цепи.
Молекулы всех известных типов формазанов являются чрезвычайно
конформационно и таутомерно подвижными, причем виды изомерии зависят
от природы заместителей, в первую очередь при атомах N1 и N5 [51]. Так, для
1,5-диарилформазанов характерна прототропная таутомерия типа N1H↔N5H.
39
Если при одном из атомов азота в молекуле формазана находится αазагетероциклический заместитель, добавляется амино-иминная таутомерия с
участием
атома
азота
гетероцикла.
Для
N5-ацилформазанов
также
реализуются поворотные конформеры за счет заторможенности вращения
вокруг амидной связи N5 – С(=О).
Присутствие в формазановой цепи двух кратных связей и атома азота с
неподеленной парой электронов позволяет образоваться единой сопряженной
системе. Результатом такого процесса является увеличение порядка связей
N2-C3, N4-N5 и барьера внутреннего вращения вокруг них, что приводит к
появлению геометрических изомеров. По этой причине для обозначения
конфигурации всех связей формазанового фрагмента используют Z,Eноменклатуру.
Исследования методом рентгеноструктурного анализа, выполненные для
большой группы формазанов, показывают, что в кристаллах реализуются три
варианта конфигурации азогидразонной цепи, представленные на схеме 1.26.
Схема 1.26
Конфигурация формазанов определяется, в основном двумя факторами:
стерическим эффектом заместителя при атоме углерода в положении 3 и
возможностью образования водородных связей, стабилизирующих ту или
иную геометрическую структуру [52].
В настоящее время и в растворах четко фиксируют возможность
реализации тех же трех форм, что и в кристаллах: красная (EZZ-изомер),
оранжевая (EEZ-изомер) и желтая (EEE-изомер).
40
Для большинства формазанов в форме EZZ-изомера характерно
отсутствие полос поглощения νNH при 3100-3500 см-1 в ИК-спектрах, а также
наличие слабопольного сигнала NH (12-15 м.д.) в спектрах ЯМР 1Н. В ЭСП
формазанов в EZZ-форме наблюдается интенсивная полоса поглощения с
максимумом около 480-500 нм. В спектрах ЯМР
13
С таких соединений
наблюдается химический сдвиг сигнала мезо-углеродного атома при 148-151
м.д. Такое строение имеют большинство 1,3,5-триарилформазанов.
Оранжевая форма (EEZ-изомер) наиболее характерна для 3-алкил-1,5дифенилформазанов с объемными алкильными заместителями. В случае же
если при атоме углерода в третьем положении находится метильная группа
или заместители вообще отсутствуют, то преимущественной становится
желтая форма или EEE-изомер. Спектральными признаками оранжевой
формы является наличие интенсивной полосы поглощения при 470 нм в
видимом спектре, а также полос при 1410 и 1190 см -1 в КР-спектре. Тогда как
для так называемой желтой формы характерно поглощение в области 400 нм,
и наличие полос при 1410, 1210 и 1150 см-1 в КР-спектре [53].
Азогидразонная цепь формазанов обычно компланарна. Плоское
строение этого фрагмента характерно как для EZZ-, так и для EEZ- и EEEизомеров формазанов. Стерические затруднения в их молекулах разрешаются
обычно поворотом заместителей при атомах азота вокруг связей N5-R, реже
N1-R.
Соединения класса формазанов относятся к семейству хелатирующих
анионных π-сопряженных N-донорных лигандов. Широкая вариабельность
заместителей в положениях 1,3,5 позволяет вводить дополнительные
комплексообразующие группы, повышающие дентатность формазанового
лиганда. Металлокомплексы на основе формазанов являются одним из
широко
известных
классов
тетраазакоординационных
соединений
[51].Формазанаты металлов применяются не только как экологически
безопасные красители, но и как компоненты оптических регистрирующих
сред, фото-, термочувствительные элементы, высокоактивные катализаторы.
41
Металлокомплексы
формазанов
также
представляют
интерес
как
молекулярные магнетики и в качестве исходных блоков для сборки
различных полимеров и супрамолекулярных ансамблей.
Впервые бисформазанаты металлов были получены Хатером и
Робертсом (Hunter, Roberts) в 1941 году [54,55] на основе 1,5-дифенил-3арилформазанов и двухвалентных меди, кобальта и никеля.
1,5-Диарилформазаны образуют с металлами бициклические соединения
трех типов (схема 1.27): с двумя шестичленными (1), с двумя пятичленными
(2) и с шестичленным и пятичленным металлоциклами (3), причем строение
комплексов сильно зависит от центрального атома металла.
Схема 1.27
Металлохелаты никеля, палладия и меди с диарилформазанами имеют
координационный узел MN4 и шестичленный металлоцикл [56-58]. В
качестве примера можно привести комплекс никеля(II) c 1,5-п-толил-3нитроформазаном [56], молекулярная структура которого изображена на
рисунке 1.9.
42
Рисунок 1.9. Молекулярная структура бис(1,5-п-толил-3нитроформазаната) никеля(II)
В данном соединении центральный атом никеля имеет плоскоквадратное
окружение. Наличие объемных арильных заместителей при донорных атомах
азота в формазане препятствует компланарному расположению плоскостей,
образованных координационным узлом NiN4 и двумя формазановыми
фрагментами,
в
результате
шестичленный
металлоцикл
принимает
конформацию несимметричной “ванны”. Расстояние от атома никеля до
плоскости каждого из лигандов составляет 0.83 Å. Длины связей Ni-N(2) и
Ni-N(4) равны 1.867(2) и 1.880(2) Å соответственно.
Бисформазанаты кобальта, аналогично никелевым комплексам, в
основном имеют плоско-квадратное строение, что подтверждается данными
исследований спектральных характеристик и магнитной восприимчивости
[59-61]. Но при этом, необходимо отметить, что пока ни один бисформазанат
кобальта не охарактеризован РСА.
Координация формазана через атомы N1 и N4 с образованием двух
пятичленных металлоциклов была подтверждена данными РСА на примере
комплекса одновалентной меди с 1,5-дифенилформазаном, выделенном в
43
виде перхлората (рис.1.10) [62]. Следует отметить, что в этом случае атом
меди координирует не анион, а нейтральную молекулу формазана.
Рисунок 1.10. Молекулярная структура перхлората бис(1,5дифенилформазан)меди(I)
Смешаннолигандные комплексы на основе формазанов были получены
для палладия путем кипячения одного эквивалента соответствующего
формазана с бис(1,1,1,5,5,5-гексафторацетонатом) палладия(II) в метаноле в
течение двух часов (схема 1.28) [63]. Структура комплексов подтверждена
методом РСА. Координационный узел состава PdN2O2 представляет собой
плоскость, которая расположена под углом ~ 27° относительно плоскости
формазанового фрагмента.
Схема 1.28
Введение дополнительных комплексообразующих групп в молекулу
формазана позволяет не только расширить круг металлов, с которыми
данный тип лигандов образует комплексные соединения, но и создать новые
44
центры координации. Формазаны, содержащие в качестве заместителей при
N1 и N5 гидрокси-, карбоксигруппы или α-азагетероциклы, обладают
повышенной хелатирующей способностью и могут выступать в качестве трии тетрадентатных лигандов. Примеры металлокомплексов на основе
формазанов, функционализированных подобным образом, представлены на
схеме 1.29.
Схема 1.29
Недавние исследования группы ученых из Нидерландов показали, что
формазаны подобно о-хинонам могут выступать в качестве редокс-активных
лигандов (схема 1.30), что открывает новые возможности для их применения
в координационной химии [73].
Схема 1.30
45
1.4. Заключение
Таким образом, в первых двух частях литературного обзора собраны
сведения о методах синтеза, строении и физико-химических свойствах осемихиноновых комплексов кобальта, марганца и железа. Основным методом
получения указанных соединений является взаимодействие карбонила
соответствующего
металла
с
раствором
о-хинона
с
последующим
облучением реакционной смеси видимым светом. Анализ литературных
данных показал, что к настоящему моменту наиболее подробно изучены
строение и свойства гомолигандных семихиноновых комплексов переходных
элементов. Кроме того, синтезирован и исследован ряд гетеролигандных бисо-семихиноновых и семихинон-катехолатных комплексов кобальта, железа и
марганца с моно- и бидентатными нейтральными лигандами, на основе
производных дипиридила, фенантролина, вторичных и третичных аминов.
Обнаружено,
что
некоторые
из
полученных
соединений
обладают
уникальной способностью к внутримолекулярному переносу электрона с
лиганда на металл, сопровождающимуся редокс-изомерным переходом
между бис-катехолатной, семихинон-катехолатной и бис-семихиноновой
формой комплекса. При этом можно влиять на положение редоксравновесия, варьируя природу иона металла, редокс-потенциал о-хинонового
лиганда
или
дополнительных
путем
введения
лигандов.
в
координационную
Магнитные
свойства
сферу
металла
гетеролигандных
о-
семихиноновых комплеков переходных металлов определяются спиновыми
взаимодействиями металл-лиганд и/или лиганд-лиганд. Успешное решение
задачи
определения
обменными
факторов,
взаимодействиями
управляющих
внутримолекулярными
в гетероспиновых
системах, позволит
получать новые магнитные материалы с заданными свойствами.
Третья часть литературного обзора посвящена формазанам и их
использованию в качестве хелатирующих анионных N-донорных лигандов в
координационной химии. Возможность введения в структуру формазанов
дополнительных
комплексообразующих
групп
позволяет
варьировать
46
дентатность данного типа лигандов. Литературные данные показывают, что
синтезировано и исследовано большое число бисформазанатов металлов на
основе лигандов различной дентатности. Металлокомплексы формазанов
нашли применение в качестве красителей натуральных и синтетических
волокон в текстильной промышленности, а также как компоненты
оптических регистрирующих сред. Кроме того, они представляют интерес в
качестве компонентов для молекулярных магнетиков и исходных блоков для
сборки полимеров и супрамолекулярных ансамблей. Комплексы металлов,
содержащие одновременно с формазановым другие органические лиганды,
встречаются в литературе крайне редко и пока еще мало изучены.
47
Глава II. Результаты и их обсуждение
2.1. Бис-3,6-ди-трет-бутил-о-бензосемихиноновые комплексы переходных
металлов с нейтральными донорными лигандами на основе замещенных
N-метиленанилинов
2.1.1. Получение и общая характеристика комплексов
Впервые синтезирована серия пяти- и шестикоординационных бис-3,6ди-трет-бутил-о-бензосемихиноновых комплексов кобальта, марганца и
железа вида M(3,6-SQ)2L, где L – нейтральный донорный лиганд на основе
фенил, пиридин- или тиофен-замещенного N-метиленанилина (Схема 2.1).
Схема 2.1
Методы получения указанных соединений представлены на схеме 2.2.
Для синтеза комплексов кобальта 1-5 подходят все три перечисленных
метода. Взаимодействие карбонила кобальта Co2(CO)8 с 3,6-ди-трет-бутил-обензохиноном и нейтральным лигандом в молярном соотношении 1:4:2
(схема 2.2, метод 1) происходит достаточно быстро даже при комнатной
температуре, образующиеся в результате комплексы выделяются в виде
48
мелкодисперсных
аморфных
глубоко-окрашенных
порошков.
Причем,
независимо от применяемого растворителя (гексан, толуол, диэтиловый
эфир) их выделение не представляет трудностей, и выходы целевого
продукта составляют 80-90%. Однако, получить таким образом образцы,
пригодные для рентгеноструктурного анализа, весьма затруднительно
вследствие большой скорости осаждения продукта.
Схема 2.2
Обмен о-хинонового лиганда в трис-о-семихиноляте кобальта(III) на
нейтральный лиганд в диэтиловом эфире (схема 2.2, метод 2) происходит
медленнее,
что
позволяет
выделить
мелкокристаллические
образцы
комплексов. Однако, в некоторых случаях требуется дополнительная очистка
продукта
от
3,6-ди-трет-бутил-о-бензохинона,
образующегося
в
ходе
реакции. Комплексы железа 9-10 также синтезировали по методу 2, причем
чтобы исключить координацию молекул растворителя, вместо диэтилового
эфира использовали гексан.
Обменная реакция о-семихинолята таллия(I) с хлоридом переходного
металла в присутствии донорного лиганда (схема 2.2, метод 3) является
классическим методом получения о-семихиноновых комплексов переходных
металлов
[14].
Этот
метод
более
всего
подходит
для
получения
кристаллических образцов, но с препаративной точки зрения является
49
наиболее многостадийным, требующим неоднократного очищения раствора
продукта от осадка неорганической соли, выделяющейся в процессе реакции.
Метод
3
оказался
наиболее
подходящим
для
синтеза
комплексов
марганца 6-8.
Полученные комплексы 1-10 в кристаллическом виде устойчивы к
действию кислорода и
растворителях
как
влаги
толуол,
воздуха, легко
хлористый
метилен,
растворимы
ТГФ,
в таких
ДМЭ,
слабо
растворимы в гексане.
ИК спектры полученных соединений характеризуются набором полос
колебаний
лигандов,
входящих
в
состав
комплексов.
Образование
комплексов, содержащих о-хиноновые лиганды в анион-радикальной форме,
подтверждается характерным набором полос в области 700-1600 см-1. Так, в
ИК-спектре комплексов 1-10 в области 1350-1450 см-1 наблюдаются
интенсивные полосы валентных колебаний полуторных связей C-O осемихинонов и отсутствуют типичные полосы в интервале 1150-1250 см-1,
отвечающие колебаниям одинарной С-О связи в дианионной катехолатной
форме лиганда. Спектры указанных комплексов в ближнем ИК-диапазоне
также не содержат полос межлигандного переноса заряда в области 40009000 см-1, характерных для семихинон-катехолатных комплексов.
Присутствие в комплексах координированных нейтральных N-донорных
лигандов определяли по следующим полосам: валентные колебания
ν(С=N)сопряж – 1610-1540 см-1, валентные колебания ν(Саром-N) – 1360-1250 см1
. Для пиридинового фрагмента характеристичными являются полосы,
соответствующие скелетным колебаниям 1572-1580 см-1, 1437-1480 см-1 и
деформационным колебаниям (С-H)аром и (С-С)аром. 745 и 700 см-1.
Тиофеновый фрагмент определяли по интенсивной полосе в области 770-680
см-1 [74].
50
2.1.2. Строение и свойства пятикоординационных бис-о-семихиноновых
комплексов на основе 2,6-диметил-N-(тиофен-2-илметилен)анилина
(L(I))
В соответствии со схемой 2.2 были получены пятикоординационные
комплексы кобальта, марганца и железа 1, 6 и 9.
Молекулярное строение комплекса 1 установлено с помощью метода
рентгеноструктурного анализа. Основные длины связей и валентные углы
приведены в таблице 2.1. Кристаллы 1 содержат кристаллизационный толуол
– по одной молекуле толуола на каждую молекулу комплекса. Как показано
на
рисунке
2.1,
центральный
атом
кобальта
в
комплексе
1
пятикоординационный, а сам комплекс имеет искаженную квадратнопирамидальную геометрию. Нужно отметить, что комплекс 1 является
первым структурно-охарактеризованным примером пятикоординационного
бис-о-семихинонового комплекса кобальта.
Рисунок 2.1. Молекулярное строение комплекса Co(3,6-SQ)2L(I) (1). Атомы
водорода не показаны
51
Таблица 2.1. Основные длины связей [Å] и валентные углы [°] в
комплексе 1
Связь
Угол
Co(1)-O(1)
2.022(3)
O(3)-Co(1)-O(2)
94.68(10)
Co(1)-O(2)
2.006(2)
O(3)-Co(1)-O(4)
80.55(10)
Co(1)-O(3)
1.977(2)
O(2)-Co(1)-O(4)
156.53(11)
Co(1)-O(4)
2.020(3)
O(3)-Co(1)-O(1)
143.08(10)
Co(1)-N(1)
2.054(3)
O(2)-Co(1)-O(1)
79.77(10)
O(1)-C(1)
1.288(4)
O(4)-Co(1)-O(1)
90.26(11)
O(2)-C(6)
1.287(4)
O(3)-Co(1)-N(1)
117.84(11)
O(3)-C(20)
1.292(4)
O(2)-Co(1)-N(1)
104.67(11)
O(4)-C(15)
1.289(4)
O(4)-Co(1)-N(1)
97.78(11)
N(1)-C(29)
1.286(5)
O(1)-Co(1)-N(1)
98.75(11)
N(1)-C(34)
1.432(4)
C(29)-N(1)-C(34)
120.2(3)
S(1)-C(33)
1.710(4)
C(29)-N(1)-Co(1)
119.4(2)
S(1)-C(30)
1.739(4)
C(34)-N(1)-Co(1)
120.3(2)
C(1)-C(2)
1.440(5)
C(1)-C(6)
1.471(5)
C(2)-C(3)
1.351(5)
C(3)-C(4)
1.421(5)
C(4)-C(5)
1.359(5)
C(5)-C(6)
1.430(5)
C(15)-C(16)
1.429(5)
C(15)-C(20)
1.467(5)
C(16)-C(17)
1.363(5)
C(17)-C(18)
1.419(5)
C(18)-C(19)
1.370(5)
C(19)-C(20)
1.426(5)
52
В основании пирамиды лежат четыре атома кислорода О(1)-О(4)
семихиноновых лигандов, а апикальное положение занимает атом азота N(1)
нейтрального лиганда L(I). Координация атома серы S(1) тиофенового
фрагмента на атом кобальта не наблюдается. Сумма углов O(1)-Co-O(2),
O(2)-Co-O(3), O(3)-Co-O(4) и O(1)-Co-O(4) основания пирамиды составляет
345.25º. При этом валентные углы O(1)-Co-O(3) и O(2)-Co-O(4) равны
143.08(10) и 156.53(11)º. Отклонение атома кобальта от плоскости фрагмента
O(1)O(2)O(3)O(4) равно 0.52 Å.
Длины связей C-O составляют 1.289±0.003 Å, что соответствует
величинам длин связей координированных о-семихиноновых лигандов в
различных комплексах металлов (1.28-1.31 Å) [23, 75]. Кроме этого, для
связей C-C между атомами углеродов шестичленных углеродных колец
наблюдается хиноидный тип искажения длин связей, при котором
межатомные расстояния C(1)-C(2), C(3)-C(4), C(5)-C(6), C(1)-C(6) одного осемихинонового кольца и C(15)-C(16), C(17)-C(18), C(19)-C(20) и C(15)-C(20)
второго о-семихинонового кольца изменяются в пределах 1.421(5)-1.471(5) Å
и являются значительно более длинными, чем межатомные расстояния C(2)C(3), C(4)-C(5), C(16)-C(17) и C(18)-C(19) (1.351(5)-1.370(5) Å).
Длины связей кобальт-кислород Co-O(1-4) близки между собой и
составляют 1.977-2.022(3) Å, что свидетельствует о высокоспиновом
состоянии центрального атома кобальта(II) в комплексе 1, т.к. ожидаемый
диапазон значений длин связей Co-O для низкоспинового кобальта(II)
составляет 1.86-1.89 Å, а для высокоспинового – 1.95-2.07 Å [20]. Связь
Co(1)-N(1) (2.054(3) Å) является более короткой, по сравнению с другими
бис-семихиноновыми комплексами кобальта(II) с N-донорными лигандами
[23].
Таким
образом,
согласно
данным
двухвалентный ион кобальта Co(II) и
РСА
комплекс
1
содержит
два анион-радикальных о-
бензосемихиноновых лиганда.
53
Были исследованы магнитные свойства комплекса 1 в интервале
температур 2 - 300 К. Температурная зависимость эффективного магнитного
момента для данного комплекса представлена на рисунке 2.2.
Рисунок 2.2. Температурные зависимости эффективных магнитных моментов
комплексов 1(●) и 11 (▲).
Высокотемпературное значение μэфф для 1 составляет 4.62 μВ (300 К),
что близко к теоретическому 4.58 μВ, рассчитанному для системы, состоящей
из трех радикальных центров: одного со спином S = 3/2 и двух с S = 1/2.
Такое состояние системы соответствует в данном случае комплексу
высокоспинового Co(II) (d7, S = 3/2) с двумя семихиноновыми лигандами (S =
1/2). В интервале температур 100 – 2 К происходит резкое уменьшение
эффективного магнитного момента до величины 3.77 μВ при 2 К, это немного
ниже чисто-спинового значения 3.87 μВ, ожидаемого для одного иона Co(II).
Такое
поведение
указывает
на
наличие
в
комплексе
1
слабых
антиферромагнитных обменных взаимодействий между анион-радикальными
SQ-лигандами, а также слабого межмолекулярного антиферромагнитного
обмена.
54
Параметры обменного взаимодействия в комплексе 1 были определены c
применением модели, содержащей три обменно-связанных спиновых центра
(схема 2.3), с использованием Гамильтониана
H = -2J(S1S2 + S2S3) – 2J1S1S3,
(1)
где S1 = S3 = 1/2 – спины семихиноновых лигандов, S2 – спин парамагнитного
иона металла (S2 = 3/2 для Co(II) иона), с учетом межмолекулярного
обменного взаимодействия (zJ’) в приближении молекулярного поля.
Схема 2.3
Удовлетворительное
воспроизведение
экспериментальных
данных
μэфф(Т) было получено при следующих параметрах: gSQ = 2 (фиксированное),
gCo = 2.06, J = 0 (фиксированное), J1 = - 13 см-1, zJ’ = - 0.06 см-1, R2 = 3.2.10-4.
Соответствующая данным параметрам теоретическая кривая μэфф(Т)
приведена на рисунке 2.2 (сплошная линия).
Нужно отметить, что в литературе ранее упоминалось только о двух
пятикоординационных
семихиноновых
комплексах
кобальта
Co(3,6-
SQ)2(AsEt3) и Co(3,6-SQ)2(PPh3) (11) [17], причем магнитное поведение
последнего сильно отличается от того, что наблюдается для комплекса 1
(рисунок 2.2). Значение эффективного магнитного момента комплекса
Co(3,6-SQ)2(PPh3) в температурном интервале 300 - 2 К изменяется
незначительно от 2.08 μВ при 300 К до 1.76 μВ при 25 К. Низкотемпературное
55
значение μэфф ненамного превышает чисто спиновое значение 1.73 μ В,
рассчитанное для одного неспаренного электрона (S = 1/2). Спектры ЭПР,
зафиксированные в стеклообразной матрице растворителя (120 К, Et2O) и в
порошке (g┴ ≈ g║ ≈ gтв ≈ 1.989), свидетельствуют о том, что единственный
неспаренный электрон локализован на семихиноновом лиганде [76]. Таким
образом, электронное состояние комплекса 11 не изменяется с температурой
и может быть описано формулой CoIII(3,6-SQ)(3,6-Cat)(PPh3). Неизменность
электронного состояния комплекса находит свое отражение в температурной
зависимости теплоемкости: в интервале от 7 до 350 К теплоемкость
комплекса 11 плавно увеличивается с ростом температуры.
Сравнение
магнитных
свойств
соединений
1
и
11
наглядно
демонстрирует влияние природы нейтрального лиганда на электронное
строение семихиноновых комплексов и распределение зарядов в системе. В
пятикоординационном комплексе с азотным донорным лигандом (L(I))
кобальт - двухвалентный высокоспиновый, связан с двумя
анион-
радикальными семихиноновыми лигандами, тогда как в комплексе с
трифенилфосфином
координированный
кобальт
одним
трехвалентный
семихиноновым
и
низкоспиновый,
одним
дианионным
катехолатным лигандами.
Электронное строение комплексов 1, 6 подтверждается данными
электронной спектроскопии поглощения в видимом и УФ-диапазоне. Как
представлено на рисунке 2.3 в спектрах толуольных растворов обоих
комплексов при комнатной температуре наблюдаются высокоинтенсивные
полосы в области 350-450 нм, обусловленные π-π* и n-π* переходами в осемихиноновых лигандах.
56
Рисунок 2.3. Электронные спектры поглощения растворов комплексов
Co(3,6-SQ)2L(I) (1) и Mn(3,6-SQ)2L(I) (6)
(толуол, 298 К, l = 1 см, С = 2.10-4 моль/л)
Менее
интенсивные
широкие
полосы
поглощения,
соответствующие
переносу заряда между семихиноновыми лигандами (SQ-SQ), а также
переносу металл-SQ, в спектре комплекса 1 располагаются в области 560-780
нм,
тогда
как
в
спектре
комплекса
6
они
смещены
в
более
низкоэнергетическую область (660-850 нм). В спектрах также присутствуют
полосы межлигандного переноса заряда между семихиноновым и Nдонорным лигандом при 826 и 883 нм для соединений 1 и 6 соответственно.
Наличие максимумов поглощения в указанных областях характерно и для
других бис-семихиноновых комплексов Co(II) и Mn(II) с дополнительными
нейтральными лигандами [7,20,22,37,77-78].
2.1.3. Строение и свойства пятикоординационных бис-о-семихиноновых
комплексов на основе N-бензилиден-2,6-диизопропиланилина (L(II))
При использовании в качестве N-донорного лиганда N-бензилиден-2,6диизопропиланилина (L(II)) (схема 2.2, метод 1) нами был получен
57
пятикоординационный комплекс кобальта Co(3,6-SQ)2L(II) (2). К сожалению,
выделить
кристаллы
рентгеноструктурного
данного
анализа,
не
комплекса,
удалось.
пригодные
Однако,
по
для
реакции,
представленной на схеме 2.4, нами был синтезирован аналогичный комплекс
цинка Zn(3,6-SQ)2L(II) (12), молекулярное строение которого подтверждено
методом РСА (рисунок 2.3). Основные длины связей и валентные углы
приведены в таблице 2.2.
Схема 2.4
Комплекс 12 был выделен путем медленной кристаллизации из толуола
после отделения реакционной смеси от избытка металла и представляет
собой темно-зеленые стержневидные кристаллы. Согласно данным РСА
геометрия координационного окружения центрального атома цинка в
соединении 12 квадратно-пирамидальная. Как и в случае комплекса 1
основание
пирамиды
координированных
образовано
хиноновых
атомами
лигандов,
а
кислорода
в
аксиальной
О(1)-О(4)
вершине
располагается атом азота N(1) нейтрального лиганда. Сумма углов O(1)-ZnO(2), O(2)-Zn-O(4), O(3)-Zn-O(4) и O(1)-Zn-O(3) основания пирамиды
составляет 343.23º. При этом валентные углы O(1)-Zn-O(4) и O(2)-Zn-O(3)
равны 158.00(3) и 134.95(3)º. Расстояние от атома цинка до плоскости
фрагмента O(1)O(2)O(3)O(4) составляет 0.584 Å. Двугранный угол между
плоскостями о-хиноновых лигандов равен 64.92°.
58
Рисунок 2.4. Молекулярное строение комплекса Zn(3,6-SQ)2L(II) (12). Атомы
водорода и трет-бутильные группы в о-семихиноновых лигандах не
показаны
Значения длин связей C-O лежат в интервале 1.2794(14) - 1.2867(13) Å,
характерном для полуторных связей С-О в о-семихиноновых комплексах
металлов [23]. Расстояние Zn(1)-N(1) составляет 2.0500(10) Å, что близко к
значению
2.0459(18)
Å,
наблюдающемуся
для
родственного
пятикоординационного комплекса Zn(3,6-SQ)2(py) [79]. Для сравнения в
шестикоординационном бис-о-семихиноновом
комплексе
цинка
с
N-
донорным лигандом Zn(3,6-SQ)2(tmeda) связь Zn-N значительно длиннее, ее
величина составляет в среднем 2.191 Å [80]. Средняя длина связи Zn–O
2.0384±0.0160 Å находится в интервале значений, типичных для осемихиноновых комплексов цинка [79,80]. Таким образом, соединение 12
представляет собой бис-о-семихиноновый комплекс Zn(II), связанный с
одним N-донорным лигандом (L(II)).
59
Таблица 2.2. Основные длины связей [Å] и валентные углы [°] в комплексе 12
Связь
Угол
Zn(1)-O(1)
2.0544(8)
O(4)-Zn(1)-O(2)
89.78(3)
Zn(1)-O(2)
2.0365(8)
O(4)-Zn(1)-O(3)
80.52(3)
Zn(1)-O(3)
2.0408(8)
O(2)-Zn(1)-O(3)
134.95(3)
Zn(1)-O(4)
2.0224(8)
O(4)-Zn(1)-N(1)
103.14(4)
Zn(1)-N(1)
2.0500(10)
O(2)-Zn(1)-N(1)
116.17(4)
O(1)-C(1)
1.2867(13)
O(3)-Zn(1)-N(1)
108.88(3)
O(2)-C(2)
1.2843(14)
O(4)-Zn(1)-O(1)
158.00(3)
O(3)-C(15)
1.2864(13)
O(2)-Zn(1)-O(1)
79.85(3)
O(4)-C(16)
1.2794(14)
O(3)-Zn(1)-O(1)
93.09(3)
N(1)-C(29)
1.2828(14)
N(1)-Zn(1)-O(1)
98.85(3)
N(1)-C(36)
1.4514(15)
C(29)-N(1)-C(36)
122.47(10)
C(1)-C(2)
1.4745(16)
C(29)-N(1)-Zn(1)
117.77(8)
C(1)-C(6)
1.4455(16)
C(36)-N(1)-Zn(1)
119.73(7)
C(2)-C(3)
1.4373(15)
C(3)-C(4)
1.3708(17)
C(4)-C(5)
1.4230(17)
C(5)-C(6)
1.3599(16)
C(15)-C(16)
1.4845(16)
C(15)-C(20)
1.4348(16)
C(16)-C(17)
1.4389(16)
C(17)-C(18)
1.3647(16)
C(18)-C(19)
1.4268(16)
C(19)-C(20)
1.3710(16)
Полученные нами данные ИК, УФ-спектроскопии и элементного
анализа для комплексов 2 и 12, позволяют сделать вывод о том, что данные
60
комплексы имеют сходное строение, которое отвечает общей формуле
МII(3,6-SQ)2L(II).
Нужно
отметить,
что
температурная
зависимость
эффективного
магнитного момента комплекса кобальта 2 (рисунок 2.5) сильно отличается
от описанных выше кривых для пятикоординационных комплексов 1 и 11. В
интервале температур 300-20 К значение μэфф уменьшается от 2.96 μВ при 300
К до 1.87 μВ при 20 К. Высокотемпературное значение магнитного момента
соответствует теоретическому для спиновой системы, состоящей из трех
радикальных
центров
с
S
=
1/2
для
каждого
(μ теор=3.0
μВ),
а
низкотемпературное указывает на то, что при данной температуре основное
спиновое состояние комплекса 2 – дублетное (Sсистемы = 1/2).
Рисунок 2.5. Температурная зависимость эффективного магнитного момента
комплекса 2. Экспериментальная (●) и теоретическая (сплошная линия)
кривые
Был проведен расчет зависимости μэфф(Т) для комплекса 2 c
применением модели, содержащей три обменно-связанных спиновых центра,
61
с использованием Гамильтониана (1) (S2 = 1/2 для иона Co(II) (н.с.) иона), с
учетом межмолекулярного обменного взаимодействия (zJ’) и параметра
температурно-независимого
парамагнетизма
(TIP).
Наилучшее
воспроизведение экспериментальных μэфф(Т) данных было получено при
следующих параметрах: gSQ = 2 (фиксированное), gCo = 2.13, J = 0
(фиксированное), J1 = - 66 см-1, zJ’ = 0.55 см-1, TIP = 0.00021.
Соответствующая
данным
параметрам
теоретическая
кривая
μэфф(Т)
приведена на рисунке 2.5. Данные свидетельствуют о том, что дублетное
спиновое состояние комплекса при низких температурах в данном случае
достигается путем антиферромагнитного обменного взаимодействия между
о-семихиноновыми лигандами, и при этом атом кобальта(II) находится в
низкоспиновом состоянии (Co(II), d7, н.с., SCo = 1/2).
2.1.4. Строение и свойства бис-о-семихиноновых комплексов с
нейтральными донорными лигандами на основе алкилзамещенных Nпиридин-2-илметиленанилинов (L(III)-L(V))
В соответствии со схемой 2.2 были получены шестикоординационные
бис-о-семихиноновые комплексы кобальта, марганца и железа 3-5, 7-8 и 10.
Из литературного обзора видно, что шестикоординационные комплексы
переходных металлов на основе различных о-хинонов довольно подробно
изучены. Однако ранее в качестве дополнительных лигандов в основном
использовались замещенные пиридины, дипиридилы и разнообразные
амины,
характеризующиеся
относительно
симметричным
строением.
Поэтому в данной работе нами в качестве нейтральных лигандов были
выбраны несимметричные иминопиридины, отличающиеся заместителями
при N-арильной группе L(III)-L(V). На примере комплексов кобальта,
содержащих указанные лиганды, можно продемонстрировать влияние
строения дополнительного лиганда на магнитное поведение комплекса
(рисунок 2.6).
62
Рисунок 2.6. Температурные зависимости эффективных магнитных моментов
комплексов 3 (●), 4(○), 5(■)
Так для ряда комплексов 3-5 обнаружено, что величина магнитного
момента и тип обменного взаимодействия между парамагнитными центрами
изменяются в зависимости от заместителей в бензольном кольце донорного
иминопиридинового лиганда. Для комплекса 3 (в L(III) оба орто-заместителя
у N-арила – метильные группы) в интервале 30-200 К магнитный момент
практически не изменяется со значением 3.71 μВ близким к расчетным 3.87 μВ
для S = 3/2, что свидетельствует в пользу антиферромагнитного обмена
между о-семихиноновыми лигандами. В интервале 200-300 К μэфф заметно
растет достигая 4.18 μВ при 300 К, но не выходя на плато. Таким образом, в
комплексе 3 между лигандами наблюдается антиферромагнитное обменное
взаимодействие лиганд-лиганд со средней энергией обмена. Комплекс 4 (в
L(IV) в орто-положениях N-арила находятся изопропильная и метильная
группы), при 300 К имеет магнитный момент 4.87 μВ, при понижении
температуры μэфф постоянно падает до 4.05 μВ при 30 К, что несколько выше,
чем расчетное значение 3.87 μВ для S = 3/2. Характер кривой говорит о
незначительном антиферромагнитном обмене между семихиноновыми
63
лигандами. Комплекс 5, у которого в нейтральном лиганде L(V) в 2,5положениях N-арильной группы находятся объемные трет-бутильные
группы,
демонстрирует
взаимодействия
между
превалирование
ферромагнитного
анион-радикальными
лигандами
обменного
(об
этом
свидетельствует характер кривой зависимости μэфф(T), при котором в
интервале температур 50-300 К μэфф постепенно падает со значения 5.61 μВ до
5.54 μВ, что значительно выше теоретических 4.58 μВ). При 2 К магнитный
момент составляет 4.93 μВ.
Такое изменение магнитных свойств в данном случае вероятно можно
объяснить
изменением
общей
геометрии
комплекса
(в
частности
диэдрального угла между плоскостями анион-радикальных семихиноновых
лигандов), происходящей при замене одного нейтрального лиганда на другой
с более объемными заместителями.
Электронные спектры поглощения толуольных растворов комплексов 35 (рисунок 2.7, таблица 2.3) характеризуются наличием высокоинтенсивных
полос в области 335-340 нм, а также наличием трех широких полос меньшей
интенсивности в области 580-810 нм. Нужно отметить, что по сравнению со
спектром пятикоординационного бис-семихинонового комплекса кобальта 1,
в спектрах шестикоординационных комплексов 3-5 наблюдается смещение
полос, соответствующих переносу заряда между семихиноновыми лигандами
(SQ-SQ), а также переносу металл-лиганд, в более высокоэнергетическую
область.
64
Рисунок 2.7. Электронные спектры поглощения растворов комплексов 3-5
(толуол, 298 К)
Таблица 2.3. Параметры электронных спектров поглощения комплексов 3-5
Комплекс
λ / нм
(ε / М-1 . см-1)
Co(3,6-SQ)2L(III) (3)
340 пл.(11700), 586(2300), 699(2800), 806 пл.(2400)
Co(3,6-SQ)2L(IV) (4)
335 пл.(9200), 580(1400), 699(1800), 807 пл.(1400)
Co(3,6-SQ)2L(V) (5)
341 пл.(12000), 586(1900), 721(2500), 804 пл.(2300)
Магнетохимические
шестикоординационного
исследования,
комплекса
марганца
проведенные
Mn(3,6-SQ)2L(III)
для
(7)
в
температурном интервале 5 - 300 К, показали, что высокотемпературное
значение эффективного магнитного момента для данного соединения
составляет 3.74 μВ (300 К). При понижении температуры значение μэфф
плавно убывает в интервале температур 300 – 25 К до величины 3.50 μВ (25
К), а при дальнейшем снижении температуры падает до 3.11 μ В при 5 К
(рисунок 2.8).
65
Рисунок 2.8. Температурная зависимость эффективного магнитного момента
комплекса Mn(3,6-SQ)2L(III) 7. Экспериментальная (●) и теоретическая
(сплошная линия) кривые
Нами был проведен расчет зависимости μэфф(Т) для комплекса 7 c
применением модели, содержащей три обменно-связанных спиновых центра,
с использованием Гамильтониана (1) (S2 = 5/2 для иона Mn(II) (в.с.)) и с
учетом межмолекулярного обменного взаимодействия (zJ’). Наилучшее
воспроизведение экспериментальных μэфф(Т) данных было получено при
следующих параметрах: gSQ = 2 (фиксированное), gMn = 1.92, J = - 153 см-1, J1
= 0 (фиксированное), zJ’ = -1.19 см-1, R2 = 9.41.10-5. Соответствующая данным
параметрам теоретическая кривая μэфф(Т) приведена на рисунке 2.8. Таким
образом, согласно полученным данным соединение 7 представляет собой
комплекс двухвалентного высокоспинового марганца, антиферромагнитно
связанного с двумя семихиноновыми лигандами.
66
2.2. Бис-3,6-ди-трет-бутил-о-бензосемихиноновые комплексы переходных
металлов с нейтральными донорными лигандами на основе 5,7-ди-третбутилбензоксазола
Бензоксазолы принадлежат к классу биологически активных веществ, их
производные привлекают внимание исследователей благодаря проявлению
антибактериальной, противогрибковой и противоопухолевой активности [8185]. Они также представляют интерес в качестве флуоресцентных зондов,
поскольку обладают высокой термической и фотофизической стабильностью
и демонстрируют большой Стоксов сдвиг [86].
Получен
ряд
новых
бис-3,6-ди-трет-бутил-о-бензосемихиноновых
комплексов кобальта, марганца и железа вида M(3,6-SQ)2L, где L –
нейтральный донорный лиганд на основе пиридин- или тиофен-замещенного
5,7-ди-трет-бутилбензоксазола (схема 2.5).
Схема 2.5
Для синтеза комплексов кобальта 13 и 16 использовали реакцию обмена
между трис-3,6-ди-трет-бутил-о-бензосемихинолятом кобальта(III) и 5,7-дитрет-бутил-2-(пиридин-2-ил)бензоксазолом,
протекающую
в
среде
диэтилового эфира за несколько часов (схема 2.2, метод 2). В случае
комплекса железа подобное обменное взаимодействие происходит гораздо
медленнее, а для трис-о-семихинонового комплекса марганца вообще не
67
имеет места. Поэтому для синтеза соединений Mn(3,6-SQ)2L(VI) (14) и
Fe(3,6-SQ)2L(VI) (15) был использован другой метод, а именно обменное
взаимодействие о-семихинолята таллия(I) с хлоридом соответствующего
металла в присутствии донорного лиганда в молярном соотношении
реагентов 2:1:1 (схема 2.2, метод 3). Нужно отметить, что комплекс 15
возможно получить по методу 2, однако это потребует большего времени
проведения реакции.
Комплексы 13-16 в кристаллическом виде устойчивы к действию
кислорода и влаги воздуха, легко растворимы в таких полярных
растворителях как ТГФ, ДМЭ, слабо растворимы в гексане.
ИК спектры полученных соединений характеризуются набором полос
колебаний характерных для семихиноновых и бензоксазольных лигандов
соответственно.
Электронный спектр поглощения комплекса кобальта Co(3,6-SQ)2L(VI)
13 содержит три широкие интенсивные полосы при 483, 541 и 800 нм
(рисунок 2.9). Наличие поглощения в данных областях характерно и для
других комплексов CoII(SQ)2L, где L-бидентатный N-донорный лиганд
[20,22,77-78]. В электронном спектре поглощения комплекса марганца 14
наблюдаются две полосы: одна высокоинтенсивная с максимумом около 410
нм (ε ≈ 6×103 л . моль-1 . см-1), а другая с меньшей интенсивностью в области
590 нм (ε ≈ 102 л
комплексов
.
моль-1
.
см-1). Для родственных бис-о-семихиноновых
MnII(3,5-SQ)2(py)2
и
MnII(3,6-SQ)2(NO2-phen)
максимумы
поглощения приходятся на области 420 и 760-780 нм [7,37]. В ЭСП
комплекса железа Fe(3,6-SQ)2L(VI) 15 наблюдается широкая полоса средней
интенсивности с максимумом около 670 нм.
68
Рисунок 2.9. Электронные спектры поглощения растворов комплексов 13-15
(толуол, 298 К, l = 1 см, С = 1.5.10-4 М)
Молекулярное строение комплекса Co(3,6-SQ)2L(VI) 13 подтверждено
методом
рентгеноструктурного
анализа
(рисунок
2.10).
Кристаллы
соединения, пригодные для РСА, получены медленной кристаллизацией из
диэтилового эфира. Основные длины связей и валентные углы приведены в
таблице 2.4.
69
Рисунок 2.10. Молекулярная структура комплекса 13. Атомы водорода и
трет-бутильные группы в о-семихиноновых лигандах не показаны
Кристаллы 13 содержат кристаллизационный диэтиловый эфир – по
одной молекуле эфира на каждую молекулу комплекса.
Как показано на рисунке 2.10, атом кобальта шестикоординационный и
комплекс 13 имеет геометрию искаженной тригональной призмы. В
основаниях призмы лежат фрагменты N(1)O(1)O(4) и N(2)O(2)O(3).
Диэдральный угол между основаниями призмы составляет 1.62°. Атом
кобальта располагается на расстоянии 1.257 Å от плоскости фрагмента
N(1)O(1)O(4) и на расстоянии 1.328 Å от плоскости N(2)O(2)O(3).
Семихиноновые фрагменты расположены под углом 57.51° друг к другу.
Значения длин связей С-О лежат в интервале 1.258(3)-1.282(3) Å, что
характерно для анион-радикальной формы хиноновых лигандов [23].
70
Таблица 2.4. Основные длины связей [Å] и валентные углы [°] в
комплексе 13
Связь
Угол
Co(1)-O(1)
2.065(2)
O(3)-Co(1)-O(2)
89.00(8)
Co(1)-O(2)
2.037(2)
O(3)-Co(1)-O(4)
78.10(8)
Co(1)-O(3)
2.040(2)
O(2)-Co(1)-O(4)
135.88(9)
Co(1)-O(4)
2.051(2)
O(3)-Co(1)-O(1)
144.36(8)
Co(1)-N(1)
2.142(3)
O(2)-Co(1)-O(1)
77.89(8)
Co(1)-N(2)
2.259(3)
O(4)-Co(1)-O(1)
88.49(8)
O(1)-C(1)
1.282(3)
O(3)-Co(1)-N(1)
125.59(9)
O(2)-C(6)
1.281(3)
O(2)-Co(1)-N(1)
132.03(10)
O(3)-C(20)
1.258(3)
O(2)-Co(1)-N(2)
82.83(9)
O(4)-C(15)
1.276(3)
O(3)-Co(1)-N(2)
79.98(9)
N(1)-C(29)
1.290(4)
O(4)-Co(1)-N(1)
87.62(9)
N(1)-C(35)
1.434(3)
O(1)-Co(1)-N(1)
86.02(9)
O(5)-C(29)
1.367(3)
C(29)-N(1)-C(35)
103.56(3)
O(5)-C(36)
1.404(3)
C(29)-N(1)-Co(1)
116.45(2)
C(1)-C(2)
1.437(4)
C(35)-N(1)-Co(1)
139.98(2)
C(1)-C(6)
1.476(4)
C(2)-C(3)
1.369(4)
C(3)-C(4)
1.426(4)
C(4)-C(5)
1.352(4)
C(5)-C(6)
1,431(4)
C(15)-C(16)
1.420(4)
C(15)-C(20)
1.479(4)
C(16)-C(17)
1.373(4)
C(17)-C(18)
1.426(4)
C(18)-C(19)
1.354(4)
C(19)-C(20)
1.437(4)
71
Для шестичленных углеродных колец семихиноновых лигандов наблюдается
хиноидное альтернирование длин связей С-С. Так, расстояния C(1)-C(2),
C(5)-C(6), C(3)-C(4), C(1)-C(6) одного о-семихинонового кольца и C(15)C(16), C(17)-C(18), C(19)-C(20) и C(15)-C(20) второго о-семихинонового
кольца изменяются в пределах 1.420(4)-1.479(4) Å, в то время как связи C(2)C(3), C(4)-C(5), C(16)-C(17) и C(18)-C(19) являются более короткими, их
длина составляет 1.352(4)-1.373(4) Å.
Длина связи Co-O в комплексе 13 в среднем составляет 2.051±0.014 Å.
Эта величина хорошо укладывается в интервал соответствующих длин связей
характерных
для
высокоспиновых
комплексов
кобальта(II)
с
о-
семихиноновыми лигандами (2.007-2.080 Å) [77-78,87-89]. Нужно отметить,
что большинство подобных комплексов имеют октаэдрическое окружение
центрального атома кобальта. В литературе встречается лишь несколько
соединений, обладающих тригональнопризматической геометрией, в их
числе два бис-о-бензосемихиноновых комплекса кобальта(II) с такими
нейтральными
лигандами,
как
5-нитро-1,10-фенантролин
и
4,5-
диазафлуорен-9-он [22]. Комплекс 13, также как и Co(3,6-SQ)2(dafl),
демонстрирует асимметрию в длинах связей между металлом и нейтральным
лигандом: одна из связей Co-N на 0.117 Å короче другой (таблица 2.4).
Поскольку бис-о-семихиноновые комплексы кобальта(II) с другими N,Nдонорными лигандами не обладают такой особенностью, то несимметричную
координацию в данном случае можно отнести к общему свойству лигандов
L(I) и dafl. Таким образом, согласно данным РСА, соединение 13
представляет собой высокоспиновый комплекс Co(II) с двумя анионрадикальными о-семихиноновыми лигандами.
Результаты
магнетохимических
исследований,
проведенных
для
соединений 13-15 в интервале температур 2-300 К, представлены на рисунке
2.11.
72
Рисунок 2.11. Температурные зависимости эффективных магнитных
моментов комплексов кобальта 13 (●), марганца 14(○), железа 15(■)
Значение μэфф для комплекса Co(3,6-SQ)2L(VI) 13 плавно уменьшается
при понижении температуры с 4.21 μB при 300 К до 3.93 μB при 50 К,
последнее близко к ожидаемой чисто спиновой величине 3.87 μ B для
высокоспинового Co(II). Ниже 50 К значение эффективного магнитного
момента резко уменьшается до величины 2.81 μB при 2 К. Плавное
уменьшение эффективного магнитного момента при понижении температуры
можно
объяснить
сильным
антиферромагнитным
обменным
взаимодействием между семихиноновыми лигандами, входящими в состав
комплекса, тогда как резкое падение μэфф при низких температурах вероятно
связано с наличием слабых межмолекулярных обменных взаимодействий
также антиферромагнитного характера. Похожее поведение наблюдается для
родственных комплексов кобальта(II): Co(3,6-SQ)2(NO2-phen) [22], Co(3,5SQ)2(bpyz) (bpyz = 2,2’- бипиразин) и Co(3,5-SQ)2(phen) [89].
Эффективный магнитный момент комплекса марганца Mn(3,6-SQ)2L(VI)
14 постепенно уменьшается в интервале температур 300-180 К от 3.92 μB до
3.76
μB,
и
затем
практически
не
изменяется
вплоть
до
25
К.
73
Низкотемпературное значение μэфф составляет 3.55 μB (5 К). В температурном
интервале 180-25 К значение эффективного магнитного момента близко к
теоретическому 3.87 μB, рассчитанному для систем с суммарным спином S =
3/2. В данном случае такому состоянию системы будет отвечать комплекс
высокоспинового Mn(II), связанного антиферромагнитно с двумя осемихиноновыми лигандами.
На рисунке 2.11 видно, что с понижением температуры от 300 до 30 К
значение эффективного магнитного момента комплекса железа Fe(3,6SQ)2L(VI) 15 изменяется незначительно (от 4.97 до 4.89 μB), при этом его
величина в данном температурном интервале хорошо согласуется с
теоретическим 4.90 μB для систем с S = 2. Не смотря на то, что такие
смешанно-лигандные комплексы железа(III) как Fe(3,6-SQ)(3,6-Cat)(tmeda)
[47] и Fe(phenSQ)(phenCat)(phen) [44] демонстрируют похожее магнитное
поведение, мы полагаем, что соединение 15 представляет собой комплекс
высокоспинового
железа(II),
содержащий
два
анион-радикальных
о-
семихиноновых лиганда. В ИК-спектре данного соединения имеются
характерные полосы валентных колебаний полуторных С-О связей при 14601420 см-1 и отсутствуют полосы, соответствующие колебаниям одинарных СО связей в катехолатных лигандах, наблюдающиеся, например, для
комплексов Fe(3,5-SQ)(3,6-Cat)(bpy) и Fe(3,5-SQ)(3,5-Cat)(py) при 1260-1280
см-1 [44]. Кроме того, в спектрах семихинон-катехолатных комплексов Fe(III)
наблюдается полоса межлигандного переноса заряда с максимумом около
1100 нм, отсутствующую в спектре комплекса 15 (рисунок 2.9). Таким
образом, совокупность всех данных позволяет идентифицировать соединение
15, как комплекс высокоспинового двухвалентного железа, в котором
имеется достаточно сильное антиферромагнитное обменное взаимодействие
между двумя о-семихиноновыми лигандами.
Параметры обменного взаимодействия в комплексах 13-15 были
определены c применением модели, содержащей три обменно-связанных
74
спиновых центра, с использованием Гамильтониана (1), где S1 = S3 = 1/2 –
спины семихиноновых лигандов, S2 – спин парамагнитного иона металла (S2 =
3/2 для Co(II), S2 = 5/2 для Mn(II) и S2 = 2 для Fe(II) иона), с учетом
межмолекулярного
молекулярного
обменного
поля.
взаимодействия
Наилучшее
(zJ’)
воспроизведение
в
приближении
экспериментальных
μэфф(Т) данных было получено при следующих параметрах: для комплекса
кобальта 13 gSQ = 2 (фиксированное), gCo = 2.08 ± 0.01, J = 0 (фиксированное),
J1 = - 390 ± 20 K (- 271 см-1), zJ’ = - 1.29 ± 0.03 K (- 0.90 см-1); для комплекса
марганца 14 gSQ = 2 (фиксированное), gMn = 1.94, J = -185 ± 3 K (- 128 см-1), J1
= 0 K (фиксированное), zJ’ = - 0.24 ± 0.02 K (- 0.17 см-1); для комплекса
железа 15 gSQ = gFe = 2 (фиксированное), J = -26 ± 1 K (- 18 см-1), J1 = - - 305 ±
18 K (- 212 см-1), zJ’ = - 0.25 ± 0.01 K (- 0.17 см-1). Соответствующие данным
параметрам теоретические кривые μэфф(Т) приведены на рисунке 2.11
(сплошные линии).
Нужно отметить, что для о-семихиноновых комплексов кобальта,
обладающих такой же, как и комплекс 13, тригональнопризматической
геометрией и демонстрирующих похожее магнитное поведение (например,
Co(3,6-SQ)2(NO2-phen) [89]), количественная интерпретация магнитных
данных ранее не проводилась. Dei и Gatteschi обнаружили, что магнитное
поведение о-семихинонового комплекса СоII(Me4cyclam)(SQ)PF4 (где SQ –
или
3,5-ди-трет-бутил-о-бензосемихиноновый
9,10-
фенантренсемихиноновый лиганд, Me4cyclam – 1,4,8,11-тетраметил-1,4,8,11тетраазациклотетрадекан)
может
быть
описано
только
при
низких
температурах с использованием модели Изинга с сильной анизотропией
величин J и g ввиду орбитального вырождения октаэдрического Со(II) в этом
комплексе [90]. Мы полагаем, что реализация тригональнопризматической
геометрии координационного окружения иона кобальта в комплексе 13
приводит к снятию орбитального вырождения, а общий спин системы
отвечает эффективному спину кобальта(II) S = 3/2 с умеренной анизотропией
g-фактора (gCo = 2.08 ± 0.01).
75
Таким
образом,
согласно
магнетохимическим
исследованиям
в
комплексах кобальта 13 и железа 15 наблюдается преимущественно
антиферромагнитное обменное взаимодействие лиганд-лиганд, тогда как для
комплекса марганца 14 более ярко выраженным является обмен металллиганд также антиферромагнитного типа.
Относительно строения родственного комплекса кобальта 16 мы
полагаем, что несмотря на то, что лиганд L(VII) является потенциально
бидентатным, указанный комплекс, в отличие от соединений 13-15,
представляет собой не шести-, а пятикоординационный бис-семихиноновый
комплекс, причем координация нейтрального лиганда осуществляется за счет
атома азота бензоксазольного лиганда. Атом серы тиофенового фрагмента,
как и в случае комплекса 1, остается не координированным, что
подтверждается данными ИК-спектроскопии. В ИК-спектре комплекса 16
наблюдается лишь незначительное смещение положения характеристичной
полосы тиофена по сравнению со спектром свободного лиганда (728 и 722
см-1 для комплекса 16 и лиганда L(VII) соответственно).
Кроме того, набор и расположение полос в электронном спектре
поглощения комплекса 16: λ (ε, М-1 . см-1.): 400 (5500), 591 (1700), 769 (3300),
803 (3200) (рисунок 2.12) практически полностью совпадают с таковыми для
пятикоординационного
комплекса
кобальта
1.
Тогда
как
шестикоординационных
комплексах
кобальта
3-5
и
полосы,
13
в
соответствующие переносу заряда между семихиноновыми лигандами, а
также переносу металл-SQ, расположены в более высокоэнергетической
области.
76
Рисунок 2.12. Электронный спектр поглощения раствора комплекса 16
(толуол, 298 К, l = 1 см, С = 2.10-4 М)
На рисунке 2.13 представлена зависимость μэфф(Т) для комплекса 16.
Значение эффективного магнитного момента комплекса 16 в температурном
интервале 260 – 80 К увеличивается с понижением температуры и при 80 К
достигает
максимальной
величины
4.80
μВ,
которая
совпадает
с
теоретическим, ожидаемым для спиновой системы, состоящей из одного
центра с S = 3/2 и двух ферромагнитно-связанных центров с S = 1/2.
Рисунок 2.13. Температурная зависимость эффективного магнитного
момента комплекса 16(●)
77
Такие
магнитные
свойства
соответствуют
бис-о-семихиноновому
комплексу высокоспинового Co(II), в котором между анион-радикальными
лигандами имеют место ферромагнитные обменные взаимодействия. При
дальнейшем
понижении
температуры
значение
магнитного
момента
уменьшается до величины 4.24 μВ, очевидно вследствие межмолекулярных
обменных взаимодействий антиферромагнитного характера.
2.3. Электрохимиче ские исследования бис-о-семихиноновых комплексов
кобальта(II) с нейтральными донорными лигандами
Электрохимические исследования комплексов переходных металлов
позволяют получить дополнительные сведения об электронном строении
данных соединений, а также о характере взаимодействий между редоксактивными лигандами. Для бис-о-семихиноновых комплексов кобальта 1, 35, 13 и 16 были измерены электрохимические потенциалы (Таблица 2.5) и
составлена общая схема редокс-переходов (Схема 2.6).
Схема 2.6
Исходя из схемы видно, что исследуемые комплексы кобальта
подвергаются двум последовательным обратимым одноэлектронным стадиям
восстановления, происходящим по координированным семихиноновым
лигандам с образованием соответственно моно- и дианионных форм. Кроме
пиков восстановления семихиноновых фрагментов в катодной области
78
наблюдаются
лигандов.
процессы
Значения
восстановления
потенциалов
координированных
полуволн
семихиноновых
иминовых
лигандов
отличаются незначительно только на первой стадии, что очевидно связано с
влиянием нейтрального лиганда, для второго же редокс-процесса потенциал
полуволны одинаков.
Таблица 2.5. Электрохимические потенциалы комплексов кобальта
(DMF, V = 0.5 B/c, Ag/AgCl/KCl0, C=3.10-3 М, СУ-электрод, 0.1 М Bu4NClO4)
Комплекс
E1/2
Red.1
, В E1/2
Red.2
,B E1/2
Red.3
Ox.1
,B E
,В
p
Ox.2
E
p
,В
Co(3,6-SQ)2L(I) 1
-0.18
-0.66
-2.00
0.20
1.50
Co(3,6-SQ)2L(III) 3
-0.22
-0.67
-1.83
0.23
1.52
Co(3,6-SQ)2L(IV) 4
-0.20
-0.66
-1.84
0.21
1.53
Co(3,6-SQ)2L(V) 5
-0.15
-0.66
-1.78
0.23
1.64
Co(3,6-SQ)2L(VI) 13
-0.15
-0.65
-1.87
0.22
-
Co(3,6-SQ)2L(VII) 16
-0.16
-0.66
-2.2<
0.21
-
Для
исследуемых
соединений
первая
стадия
окисления
носит
необратимый одноэлектронный характер и происходит по семихинолятному
фрагменту с образованием о-хинона. Образующийся катионный комплекс
неустойчив: о-хинон подвергается декоординации, и на ЦВА в катодной
области наблюдается пик восстановления свободного 3,6-ди-трет-бутил-обензохинона при -0,46 В. Кроме пиков окисления семихиноновых
фрагментов,
на
ЦВА
регистрируется
электрохимическая
активность
азотсодержащих лигандов, очевидно находящихся в свободном состоянии
вследствие деструкции комплекса, происходящей после первого редокспроцесса.
79
2.4. Бис-3,6-ди-трет-бутил-о-бензосемихиноновые комплексы
переходных металлов с 2,2’-бихинолином и 1,4-ди-трет-бутил-1,4диазабутадиеном
Получен ряд новых шестикоординационных бис-3,6-ди-трет-бутил-обензосемихиноновых комплексов кобальта, марганца и железа вида M(3,6SQ)2L, где в качестве нейтрального лиганда (L) выступают 2,2’-бихинолин и
1,4-ди-трет-бутил-1,4-диазабутадиен (схема 2.7)
Схема 2.7
Молекулы, содержащие в своем составе 1,4-диаза-1,3-бутадиеновый
фрагмент, к которым в частности относятся использованные нами Biq и
DAD, благодаря своим широким координационным возможностям давно
используются в качестве лигандов в координационной химии. Они образуют
как гомо-, так и гетеролигандные комплексы практически со всеми
металлами
Периодической системы.
Координационные соединения с
лигандами такого типа обладают рядом интересных и уникальных свойств,
некоторые из них находят свое применение в каталитических процессах [9194].
80
2.4.1. Строение и свойства бис-3,6-ди-трет-бутил-о-бензосемихиноновых
комплексов кобальта, марганца и железа с 2,2’-бихинолином
2,2’-бихинолин является структурным аналогом 2,2’-дипиридила, биссемихиноновые комплексы кобальта с которым обладают способностью к
редокс-изомерии и обратимому внутримолекулярному переносу электрона
между металлом и хиноновым лигандом [18-19]. Однако аналогичные
комплексы с Biq в литературе ранее описаны не были.
Комплекс
взаимодействия
Co(SQ)2Biq
между
(17)
синтезирован
трис-о-семихинолятом
путем
обменного
кобальта(III)
и
2,2’-
бихинолином в среде диэтилового эфира (выход ~ 80%). Аналогичный
комплекс марганца Mn(SQ)2Biq (18) удалось получить по реакции карбонила
марганца с раствором 3,6-ди-трет-бутил-о-бензохинона и 2,2’-бихинолина в
толуоле. Для синтеза комплекса железа Fe(SQ)2Biq (19) использовали
реакцию между дихлоридом железа и раствором о-семихинолята таллия в
присутствии стехиометрических количеств 2,2’-бихинолина.
Полученные нами комплексы 17-19 представляют собой зеленые
порошки устойчивые в твердом виде к действию влаги и кислорода воздуха,
и хорошо растворимые в большинстве органических растворителей.
На рисунке 2.14 представлены электронные спектры поглощения
растворов комплексов 17-19 в толуоле. Спектр соединения 17 по своим
параметрам (таблица 2.6) схож с описанными выше спектрами для
шестикоординационных бис-о-семихиноновых комплексов кобальта 3-5 с
бидентатными нейтральными лигандами на основе алкилзамещенных
иминопиридинов.
81
Рисунок 2.14. Электронные спектры поглощения растворов комплексов 17-19
(толуол, 298 К, l = 1 см)
Таблица 2.6. Параметры электронных спектров поглощения
комплексов 17-19
Комплекс
λ / нм
(ε / М-1 . см-1)
Co(3,6-SQ)2Biq (17)
591 пл.(1900), 725(2800), 808 пл.(2500)
Mn(3,6-SQ)2Biq (18)
405(4900), 585(400)
Fe(3,6-SQ)2Biq (19)
360(13000), 421 пл.(3200), 643(4000)
Электронные спектры соединений 18 и 19 аналогичны таковым для
родственных бис-о-семихинолятов марганца(II) и железа (II) с 5,7-ди-третбутил-2-(пиридин-2-ил)бензоксазолом (комплексы 14 и 15 соответственно).
Таким образом, согласно данным ЭСП комплексы 17-19 в растворе при
комнатной температуре существуют в виде M(3,6-SQ)2Biq.
82
Для твердых образцов комплексов 17-19 были проведены измерения
температурной зависимости магнитной восприимчивости. Кривые μэфф(Т) для
указанных комплексов приведены на рисунке 2.15.
Рисунок 2.15. Температурные зависимости эффективных магнитных
моментов комплексов 17 (■), 18(●), 19(▲). Экспериментальные и
теоретические (сплошные линии) кривые
Значение эффективного магнитного момента комплекса 17 в интервале
300-50 К плавно убывает при понижении температуры с 4.29 μ B до 3.81 μB (50
К).
Последнее
значение несколько
ниже
чисто-спинового
3.87
μB,
ожидаемого для иона высокоспинового кобальта(II) с S = 3/2. Дальнейшее
понижение температуры сопровождается резким уменьшением μ эфф до 2.75
μB при 2 К.
Параметры обменного взаимодействия в комплексе 17 были определены
c применением модели, содержащей три обменно-связанных спиновых
центра (схема 2.3), с использованием Гамильтониана
83
учитывающего параметр расщепления в нулевом поле [95]. Результаты
проведенных расчетов представлены в таблице 2.7. Соответствующая
параметрам теоретическая кривая μэфф(Т) приведена на рисунке 2.15.
Согласно полученным данным в комплексе 17 между парамагнитными
семихиноновыми лигандами наблюдается достаточно сильное обменное
взаимодействие антиферромагнитного характера (J1 = -206 см-1).
Таблица 2.7. Результаты моделирования магнитных свойств
комплексов 17-19
Параметр
Комплекс
17
18
19
J, см-1
0
- 83
0(фиксир.)
J1, см-1
- 206
0(фиксир.)
- 240
2.23
2.08
g(M)
g║ = 2.0023(фиксир.)
g┴ = 2.02
g(SQ)
2(фиксир.)
2(фиксир.)
2(фиксир.)
Deff, см-1
21.0
-
-
zJ’, см-1
- 0.64
- 1.07
- 0.09
TIP, см3.моль-1.К
0.00027
0
0
R2
3.5.10-4
8.5.10-4
1.7.10-5
(Deff – параметр расщепления в нулевом поле)
Эффективный магнитный момент комплекса марганца 18 в исследуемом
температурном интервале 300 - 5 К постепенно уменьшается с понижением
температуры с 5.05 μB (300 К) до 3.84 μB (5 К). Такое поведение характерно
для систем с антиферромагнитным типом обмена между спиновыми
84
центрами. Низкотемпературное значение μэфф близко к теоретическому 3.87
μB, рассчитанному для систем с эффективным спином S = 3/2.
Как видно из рисунка 2.15 значение эффективного магнитного момента
комплекса железа 19 лишь не значительно увеличивается с ростом
температуры, при этом низкотемпературное значение составляет 4.91 μ B (5
К), а высокотемпературное – 5.27 μB. Ожидаемое чисто-спиновое значение
μэфф для иона высокоспинового железа(II) равно 4.90 μB.
Параметры обменного взаимодействия в комплексах 18-19 (таблица 2.7)
были определены c применением модели, описанной выше для комплекса 1.
В комплексе железа 19, также как и в комплексе кобальта 17, превалируют
антиферромагнитные
обменные
взаимодействия
лиганд-лиганд
(J1 = -240 см-1), в то время как аналогичный комплекс марганца 18
демонстрирует более ярко выраженный антиферромагнитный обмен металллиганд (J = -83 см-1).
Нужно отметить, что исследованные комплексы кобальта, марганца и
железа общего вида M(3,6-SQ)2Biq, в отличие от родственных комплексов с
2,2’-дипиридилом, не проявляют способности к редокс-изомерии.
2.4.2. Строение и свойства бис-3,6-ди-трет-бутил-о-бензосемихиноновых
комплексов кобальта, марганца и железа с 1,4-ди-трет-бутил-1,4диазабутадиеном
1,4-диазабутадиеновые лиганды также как и хиноновые лиганды
относятся к классу редокс-активных и в комплексах с металлами могут
существовать в трех редокс-состояниях (схема 2.8) [96-99]:
85
Схема 2.8
Полученные в ходе данной работы комплексы 20-22 одновременно
содержат в своем составе редокс-активные лиганды различной природы,
причем оба хиноновых лиганда находятся в анион-радикальной форме, а
один диазабутадиеновый – в нейтральной.
Комплексы кобальта Co(3,6-SQ)2DAD (20) и железа Fe(3,6-SQ)2DAD
(22) получены с хорошим выходом (~ 85%) по реакции между хлоридом
соответствующего металла и раствором о-семихинолята таллия(I) в
присутствии 1,4-ди-трет-бутил-1,4-диазабутадиенового лиганда. Комплекс
марганца Mn(3,6-SQ)2DAD (21) удалось синтезировать только путем
взаимодействия карбонила марганца с раствором 3,6-ди-трет-бутил-обензохинона при четырехкратном мольном избытке диазадиена. При другом
соотношении исходных компонентов вместо желаемого продукта образуется
трис-о-семихинолят марганца(III).
Для твердых образцов полученных комплексов 20-22 были проведены
магнетохимические
исследования.
Температурные
зависимости
эффективного магнитного момента для данных комплексов приведены на
рисунке 2.16. Параметры обменного взаимодействия в комплексах 20-22
(таблица 2.8) были определены c применением модели, описанной выше для
комплекса 1, соответствующие теоретические кривые μэфф(Т) также
представлены на рисунке 2.16 (сплошные линии).
86
Рисунок 2.16. Температурные зависимости эффективных магнитных
моментов комплексов 20 (■),21(●), 22(▲)
Значение эффективного магнитного момента комплекса 20 постепенно
уменьшается при понижении температуры с 5.03 μB при 300 К до 4.78 μB при
30 К, а затем резко падает до 3.97 μB (3 К), очевидно вследствие
87
межмолекулярных
антиферромагнитных
взаимодействий.
Высокотемпературное значение μэфф превышает теоретическое значение 4.58
μB, рассчитанное для системы, включающей высокоспиновый Co(II) c S = 3/2
и два семихиноновых лиганда с S = 1/2, при отсутствии в ней каких-либо
обменных взаимодействий. Оно скорее близко к расчетному 4.796 μ B,
соответствующему
комплексу
высокоспинового
Co(II)
и
двух
ферромагнитно-связанных SQ-лигандов. Однако для данного комплекса
наблюдается уменьшение μэфф при понижении температуры, а подобный
характер зависимости μэфф(Т) свойственен системам с антиферромагнитным
типом обмена между спиновыми центрами. В результате моделирования
магнитных свойств комплекса 20 с помощью программных средств Mjollnir
для параметров обмена J и J1 были получены нулевые значения. Это можно
объяснить тем, что в данном комплексе антиферромагнитные SQ-SQ
взаимодействия и ферромагнитные металл-SQ взаимно скомпенсированы.
Таблица 2.8. Результаты моделирования магнитных свойств
комплексов 20-22
Параметр
Комплекс
20
21
22
J, см-1
0
- 102
0(фиксир.)
J1, см-1
0
0(фиксир.)
- 218
g(M)
2.16
2.09
2.00
g(SQ)
2(фиксир.)
2(фиксир.)
2(фиксир.)
zJ’, см-1
- 0.54
- 0.28
- 0.43
TIP, см3.моль-1.К
0.0008
0
0
R2
6.3.10-5
9.6.10-6
4.1.10-5
88
Низкотемпературное значение эффективного магнитного момента для
комплекса марганца 21 составляет 3.89 μВ, что соответствует расчетному μэфф
для спиновых систем с S = 3/2. Такое состояние системы в данном случае
возможно,
когда
имеют
место
антиферромагнитные
обменные
взаимодействия между высокоспиновым Mn(II) (S = 5/2) и двумя
семихиноновыми лигандами. При повышении температуры значение μ эфф
комплекса 21 растет, достигая величины 4.51 μВ при 300 К. Что значительно
меньше величины 6.40 μВ, ожидаемой при отсутствии указанного обмена в
той же системе. Полученное в результате моделирования магнитных свойств
значение параметра J равное – 102 см-1 хорошо согласуется с предложенным
электронным строением комплекса 21.
Характер зависимости μэфф(Т) комплекса железа 22 также указывает на
наличие
в
данном
комплексе
антиферромагнитных
обменных
взаимодействий: значение μэфф в исследуемом температурном интервале
постепенно убывает при понижении температуры с 5.09 μ В при 300 К до 4.39
μВ при 5 К. Комплекс 22 имеет строение аналогичное родственному
комплексу Fe(SQ)2Biq и включает в себя ион высокоспинового железа(II) (S =
2) и два антиферромагнитно-связанных семихиноновых лиганда (параметр J1
= –218 см-1).
2.5. Строение и магнитные свойства бис-о-семихинонового комплекса
кобальта(II) с 1,4-диазабицикло(2,2,2)октаном
Взаимодействие
трис-о-семихинолята
кобальта(III)
c
1,4-
диазабицикло(2,2,2)октаном (DABCO) в соотношении реагентов 1:1 в среде
диэтилового эфира (схема 2.9) с количественным выходом приводит к
образованию темно-зеленого нерастворимого в большинстве органических
растворителей
олигомерного
комплекса
23,
охарактеризованного
элементным анализом и методом ИК-спектроскопии.
89
Схема 2.9
Нужно отметить, что образование подобных олигомерных структур
наблюдалось и ранее при взаимодействии DABCO c бис-о-семихинолятами
меди(II) и цинка [79,100], причем строение комплекса Cu(3,6-SQ)2(DABCO)n
было подтверждено данными рентгено-структурного анализа.
Проведенные в ходе данной работы магнетохимические исследования
порошка комплекса 23 в интервале температур 5 – 300 К показали, что
соединение Co(3,6-SQ)2(DABCO) имеет самые высокие значения μэфф среди
всех выше рассмотренных комплексов кобальта. Температурная зависимость
μэфф(Т) для данного комплекса представлена на рисунке 2.17.
Значение эффективного магнитного момента несколько увеличивается с
понижением температуры от 6.44 μВ при 300 К до 6.62 μВ при 140 К, что
характерно
для
систем
с
ферромагнитным
типом
обмена
между
радикальными центрами. Значение 6.62 μВ близко к теоретическому 6.51 μВ,
соответствующему системе с эффективным спином S = 5/2 (gi = 2.2). Такое
состояние системы возможно, когда имеет место ферромагнитный обмен
между высокоспиновым Co(II) (S = 3/2) и двумя семихиноновыми лигандами
(SSQ = 1/2). В интервале 140-40 К магнитный момент плавно уменьшается до
6.12 μВ (40 К) и затем резко падает до 3.86 μВ при 5 К. Низкотемпературное
значение 3,86μВ близко к теоретическому 3.87 μВ для системы с тремя
90
неспаренными электронами на одном центре. Это говорит о том, что при
низких температурах в комплексе 23 превалируют межмолекулярные
обменные взаимодействия антиферромагнитного характера.
Рисунок 2.17. Температурная зависимость эффективного магнитного
момента комплекса 23. Экспериментальная (●) и теоретическая (сплошная
линия) кривые
Нами были определены параметры обменного взаимодействия в
комплексе 23 c применением модели, описанной выше для комплекса 1.
Наилучшее воспроизведение экспериментальных μэфф(Т) данных было
получено при следующих параметрах: gSQ = 2 (фиксированное), gCo = 2.52, J =
106 см-1, J1 = 0 (фиксированное), zJ’ = - 1.69 см-1, R2 = 5.74.10-5.
Соответствующая
данным
параметрам
теоретическая
кривая
μэфф(Т)
приведена на рисунке 2.17 (сплошная линия). Согласно расчетным
параметрам комплекс 23, подобно аналогичному комплексу меди [100],
демонстрирует наличие ферромагнитных обменных взаимодействий между
металлом и парамагнитными семихиноновыми лигандами.
91
2.6. Гетеролигандные комплексы переходных металлов на основе 3,6-дитрет-бутил-о-бензохинона и формазанов
В
качестве
анионных
азотсодержащих
лигандов
для
синтеза
гетероспиновых комплексов кобальта и марганца на основе 3,6-ди-третбутил-о-бензохинона в настоящей работе использованы формазановые
лиганды, представленные на схеме 2.10.
Схема 2.10
Для получения формазанов использовали метод, в котором ключевой
реакцией является взаимодействие фенилгидразонов арилкарбальдегидов с
арендиазониевыми солями при температуре 0-5°С в среде пиридин/метанол
(схема 2.11) [101-102].
Схема 2.11
92
Нужно отметить, что формазаны 25 и 29 впервые синтезированы и
охарактеризованы данными ИК, УФ-видимой и ЯМР-спектроскопии. Для
данных формазанов характерно отсутствие полос поглощения νNH при 31003500 см-1 в ИК-спектрах и наличие слабопольного сигнала NH (15.3 – 15.5
м.д.) в спектрах 1Н ЯМР. В электронных спектрах формазанов 25 и 29
наблюдается
интенсивная
полоса
поглощения
при
490
и
477
нм
соответственно. Таким образом, спектральные характеристики данных
формазанов свидетельствуют о том, что их молекулы существуют в хелатной
EZZ-форме.
Формазан 29 способен координироваться как нейтральный лиганд за
счет атома азота пиридинового фрагмента. Этот факт подтверждается
рентгеноструктурными данными для синтезированного нами 3,6-ди-третбутилкатехолата трифенилсурьмы(V) с 5-(2,6-диметилфенил)-3-(4-пиридил)1-фенилформазаном (схема 2.12).
Схема 2.12
Кристаллы комплекса 30, пригодные для РСА, получены медленной
кристаллизацией из толуола при 0°С (30а) и перекристаллизацией из
диэтилового эфира при комнатной температуре (30б). Кристаллы 30а
содержат кристаллизационный толуол – по одной молекуле толуола на
каждую молекулу комплекса. Основные длины связей и валентные углы в
комплексах 30а и 30б приведены в таблице 2.9.
93
Таблица 2.9. Основные длины связей [Å] и валентные углы [°]
в комплексах 30а и 30б
Связь
30а
30б
Sb(1)-O(1)
2.0457(13)
2.038(4)
Sb(1)-O(2)
2.0416(13)
2.024(4)
Sb(1)-N(1)
2.4242(16)
2.556(5)
Sb(1)-C(35)
2.1623(19)
2.141(6)
Sb(1)-C(41)
2.143(2)
2.145(6)
Sb(1)-C(47)
2.1536(19)
2.157(6)
C(1)-O(1)
1.356(2)
1.367(7)
C(2)-O(2)
1.362(2)
1.361(7)
N(2)-N(3)
1.311(2)
1.317(7)
N(2)-C(20)
1.327(3)
1.345(8)
N(4)-N(5)
1.288(2)
1.283(7)
N(4)-C(20)
1.379(3)
1.377(8)
N(5)-C(29)
1.420(3)
1.433(10)
N(5)···HN(3)
1.882
1.887
Угол
30а
30б
O(1)-Sb(1)-N(1)
81.30(5)
79.09(16)
O(2)-Sb(1)-N(1)
77.13(5)
76.38(16)
C(35)-Sb(1)-N(1)
84.84(6)
89.4(2)
C(41)-Sb(1)-N(1)
170.11(7)
168.9(2)
C(47)-Sb(1)-N(1)
88.55(6)
84.1(2)
По данным РСА формазановый лиганд в составе комплекса 30
находится
в
EZZ-конфигурации,
которая
стабилизирована
за
счет
образования водородной связи N(5)…HN(3) (рисунок 2.18). Центральная
азогидразонная
группировка
в
лиганде
плоская
и
характеризуется
94
незначительной степенью делокализации (таблица 2.9). В структуре 30б
пиридиновый заместитель повернут относительно плоскости формазановой
группы на 10.75°, а два других заместителя при атомах N(3) и N(5)
практически планарны с ней. В структуре 30а угол поворота пиридинового
заместителя составляет уже 16.92°, а заместители при атомах азота выведены
из плоскости формазановой группировки. Торсионные углы для 2,6диметилфенильного и фенильного заместителей составляют 6.91° и 31.84°
соответственно.
Длины связи Sb-N(1) в комплексах 30а и 30б (2.4242(16) и 2.556(5) Å
соответственно)
лежат
в
интервале
значений,
типичных
для
шестикоординационных донорно-акцепторных комплексов сурьмы(V) с
нейтральными лигандами R3(Cat)SbL (2.266 – 2.595 Å) [103-104].
Рисунок 2.18. Молекулярное строение комплекса 30б. Тепловые эллипсоиды
30% вероятности
95
Формазаны 24-29 были использованы для синтеза гетеролигандных 3,6ди-трет-бутил-о-бензосемихиноновых комплексов кобальта и марганца.
Необходимо отметить, что в литературе описан единственный метод
получения металлокомплексов на основе формазанов, заключающийся во
взаимодействии растворов формазана и неорганической соли металла
(хлорида, ацетата, нитрата), происходящем при быстром смешивании
соответствующих растворов с последующим нагреванием [54-55,58-59] или в
условиях медленной диффузии раствора соли в раствор лиганда [102]. При
использовании первого варианта данного метода довольно затруднительно
получить кристаллические образцы комплексов, пригодные для РСА, кроме
того, в этих реакциях не велики выходы целевого продукта. Синтез
формазанатов в условиях медленной диффузии позволяет выделять
комплексы в виде монокристаллов, однако требует длительного времени
проведения реакции (10-20 суток) и побора подходящих пар растворителей.
В данной работе для получения смешанно-лигандных комплексов кобальта и
марганца
на основе
формазанов мы
впервые
использовали
метод,
включающий взаимодействие нейтральной формы формазанового лиганда с
карбонилом металла и раствором о-хинона (схема 2.13).
Схема 2.13
Данная реакция легко (за несколько часов) протекает в толуоле даже при
комнатной температуре и позволяет с количественным выходом выделять
мелкокристаллические образцы комплексов.
96
2.6.1. Строение и свойства гетеролигандных комплексов кобальта на
основе 3,6-ди-трет-бутил-о-бензохинона и формазанов
Установлено, что при взаимодействии с карбонилом кобальта в
присутствии о-хинона 3-фенилзамещенные формазаны 24-26 образуют с
металлом хелатный формазанатный цикл, в то время как 3-(4-пиридил)замещенные формазановые лиганды 27-29 координируются в нейтральной
форме через атом азота 4-пиридильной группы. При этом наблюдается
образование соответственно бис-о-семихиноновых (комплексы 31-33) или
семихинон-катехолатных (комплексы 34-36) комплексов кобальта(III) (схема
2.14).
Схема 2.14
Комплексы 31-36 были выделены в виде мелкокристаллических
порошков черного или красного цвета, устойчивых в твердом виде к
действию кислорода и влаги воздуха.
Нужно отметить, что комплексы 31-36 можно получить и путем
обменного взаимодействия между трис-о-семихинолятом кобальта(III) и
соответствующим формазановым лигандом, однако это требует большего
97
времени проведения реакции и, по сравнению с синтезом из карбонила,
данное взаимодействие протекает с меньшим выходом (~ 50%).
Полученные комплексы охарактеризованы по данным ИК, УФспектроскопии, спектроскопии ЭПР, элементного анализа и магнетохимии.
Отличия в способе координации 3-фенил- и 3-(4-пиридил)-замещенных
формазановых
лигандов находят отражение в ИК- и УФ-спектрах
полученных комплексов. Чтобы продемонстрировать данный факт, мы
подробнее рассмотрим соответствующие спектральные характеристики
комплексов 31 и 34. Так, полоса валентных колебаний двойных N=N связей в
спектре бис-о-семихинонового комплекса кобальта с формазанат анионом
(комплекс 31) (1552 см−1) сдвинута в область более слабых колебаний
относительно данной полосы в исходном 1,3,5-трифенилформазане (1598
см−1). В то время как в спектре семихинон-катехолатного комплекса 34 с
формазаном, координированным в нейтральной форме, данные колебания
наоборот сдвинуты в область колебаний более сильных связей (1613 см −1). С
другой стороны, для комплекса 34 несколько ослаблены ароматические C–N
связи 4-пиридильной группы (1550 см–1) относительно таковых в исходном 3(4-пиридил)-1,5-дифенилформазане (1556 см–1).
В ИК-спектрах комплексов 34-36 в области 2800 нм (ближний ИКдиапазон) наблюдается интенсивная полоса, относящаяся к переносу заряда
между
лигандами
в
различных
степенях
окисления.
Это
является
дополнительным подтверждением одновременного присутствия в данных
комплексах семихинонового и катехолатного лигандов.
Электронный спектр поглощения бис-о-семихинонового комплекса 31
(рисунок 2.19) содержит набор полос, характерный для комплексов типа
Co(SQ)2L. Присутствие в данном комплексе формазанового лиганда в
анионной форме подтверждается наличием интенсивной полосы переноса
заряда с максимумом при 593 нм (ε = 1.12·104 М−1·см−1). ЭСП смешанно98
лигандного комплекса 34 характеризуется наличием интенсивной полосы с
максимумом при 479 нм (ε = 1.0·104 М−1·см−1), что свидетельствует о
присутствии
в
составе
данного
комплекса
нейтральной
формы
формазанового лиганда.
Рисунок 2.19. Электронные спектры поглощения растворов комплексов 31 и
34 (толуол, 298 К, l = 1 см, С = 1.10-4 М)
Различия в строении соединений 31 и 34 проявляются и в ЭПР-спектрах
указанных соединений (рисунок 2.20).
Рисунок 2.20. Спектры ЭПР твердых образцов комплексов 31 (а) и 34 (б)
(298 К)
99
Спектр бирадикального комплекса 31 представляет собой широкую
линию (более 1000 Гс) с g =2.02. В то время как ширина линии в спектре
комплекса 34 составляет уже 70 Гс, g = 1.999. В этом комплексе
диамагнитный ион связан с двумя хиноновыми лигандами, находящимися в
разных степенях окисления: один в анион-радикальной семихиноновой
форме, а другой в дианионной катехолатной. Комплекс 36 имеет аналогичное
строение, при температурах 250-150 К для него наблюдается практически
изотропный сигнал при g = 2.000 без разрешенной сверхтонкой структуры.
Результаты магнетохимических измерений, выполненных для твердых
образцов комплексов 31 и 34, также служат подтверждением строения
данных соединений. Так, в случае бис-о-семихинонового комплекса 31
зависимость μэфф(Т) соответствует таковой для спиновой системы, состоящей
из двух обменно-связанных радикальных центров. Такое состояние системы
возможно в случае комплекса Co(III) с двумя анион-радикальными
семихиноновыми
лигандами
и
одним
анионом
формазана.
Экспериментальная и теоретическая кривые температурной зависимости
эффективного
магнитного
момента,
а
также
параметры
обменного
взаимодействия для данного комплекса представлены на рисунке 2.21.
Рисунок 2.21. Температурная зависимость эффективного магнитного
момента комплекса 31. Экспериментальная (●) и теоретическая кривые
100
Эффективный магнитный момент семихинон-катехолатного комплекса
34 практически не зависит от температуры во всем исследуемом интервале 5300 К (рисунок 2.22). Значение μэфф для него близко к таковому для систем с
одним неспаренным электроном, что в данном случае соответствует
комплексу
Co(III),
связанного
с
одним
семихиноновым
и
одним
катехолатным лигандами.
Рисунок 2.22. Температурная зависимость эффективного магнитного
момента комплекса 34
Способность гетеролигандных комплексов 31 и 34 вступать в
окислительно-восстановительные
циклической
превращения
вольтамперометрии.
была
оценена
Электрохимические
методом
характеристики
исследуемых соединений представлены в таблице 2.10.
Комплекс
обусловленных
31
отличается
широким
редокс-превращениями
набором
редокс-состояний,
координированных
лигандов
(рисунок 2.23, схема 2.15). В катодной области развертки потенциала до -1.0
В
регистрируются
две
квазиобратимые
одноэлектронные
стадии.
Фиксируемые для них значения потенциалов полуволн восстановления
близки
к
аналогичным
шестикоординационных
значениям,
наблюдаемым
бис-о-семихиноновых
для
комплексов
пяти-
и
кобальта,
101
содержащих
вспомогательные
N-донорные
лиганды.
Это
позволяет
предполагать, что данные катодные процессы относятся к восстановлению осемихиноновых лигандов до катехолатных.
Таблица 2.10. Электрохимические характеристики комплексов 31 и 34
Комплекс
31
34
E1/2Red.1, В
-0.22
-0.22
n
1
-
Ia/Ic
0.81
квазиобратим.
E1/2Red.2, B
-0.53
-0.51
n
1
-
Ia/Ic
0.90
квазиобратим.
E1/2Red.3, B
-1.29
-1.03
Ia/Ic
0.80
квазиобратим.
E1/2Red.4, B
-1.45
-
E1/2Ox.1, B
0.76
0.96
n
1
-
Ic/Ia
0.85
-
E1/2Ox.2, B
0.99
-
Ic/Ia
0.90
-
(СУ-электрод, CH2Cl2, V = 0.2 B/c, 0.1 M NBu4ClO4, C = 2.10-3 М, Ar, отн.
Ag/AgCl/KCl (нас.), Ia/Ic – коэффициент обратимости; n-число переносимых
электронов по сравнению со стандартом – ферроценом; E1/2Ox./Red. – потенциал
полуволны окисления/восстановления)
102
Рисунок 2.23. ЦВА комплекса 31 (CH2Cl2, V = 0.2 В/с, Ag/AgCl/KCl,
С=2∙10-3 М, СУ-электрод, Ar, 0.1 М Bu4NClO4)
Схема 2.15
103
Расширение развертки потенциала до -1.80 В приводит к фиксации еще
двух катодных стадий (E1/2Red.3, E1/2Red.4). Третий редокс-процесс является
квазиобратимым, одноэлектронным (рисунок 2.23, схема 2.15) и протекает по
формазанатному
фрагменту
с
образованием
стабильного
металл-
вердазильного радикала (значение коэффициента обратимости Ia/Ic = 0.80).
Полученное значение потенциала (E1/2Red.3 = -1.29 В) сопоставимо с
результатами, описанными в литературе для бис-формазанатов никеля(II) и
цинка(II) [73,105]. Четвертый катодный процесс также квазиобратим и, по
всей видимости, относится к восстановлению иона кобальта Co(III)→Co(II).
В анодной области для комплекса 31 наблюдаются две квазиобратимых
одноэлектронных стадии (рисунок 2.23). Регистрируемое значение первого
потенциала окисления сильно смещено в анодную область по сравнению с
данными, полученными для комплексов CoII(3,6-SQ)2L, где L – нейтральный
донорный лиганд. Можно предположить, что смещение потенциала в данном
случае вызвано наличием в комплексе 31 иона металла в форме Со(III).
Регистрируемый на ЦВА при 0.99 В второй анодный процесс относится к
окислению формазанат-аниона до соответствующего радикала (схема 2.15).
Семихинон-катехолатный
комплекс
34
с
координированной
в
нейтральной форме молекулой формазана очень плохо растворяется и
сорбируется на поверхности электродов, поэтому невозможно было
определить число электронов и можно говорить только об обратимости
процессов. Полученные значения потенциалов восстановления хорошо
согласуются с данными для ранее изученных бис-о-семихинолятов кобальта
(II) с вспомогательными N-донорными лигандами. На ЦВА фиксируются два
катодных
процесса,
протекающих
по
о-семихиноновым
лигандам
с
образованием соответственно моно- и дианионного комплексов. Третий
катодный процесс отвечает восстановлению формазана и сопровождается
сильной адсорбцией продуктов электрохимической реакции, пассивирующих
рабочий электрод. В анодной области при потенциале +0.96 В наблюдается
104
необратимый пик окисления по формазановому лиганду. В виду адсорбции
исходного соединения не удалось зафиксировать редокс-переходы по осемихинолятным лигандам.
2.6.2. Моно-о-семихинон-формазанатные комплексы кобальта(II)
Обнаружено, что при взаимодействии карбонила кобальта с 1,3,5трифенилформазаном и 3,6-ди-трет-бутил-о-бензохиноном в толуоле при
соотношении реагентов 1:4:2 помимо бис-семихинонового гетеролигандного
комплекса 31, описанного выше, в качестве минорного продукта происходит
образование о-семихинон-формазанатного комплекса кобальта 37 (схема
2.16).
Схема 2.16
Соединение
37
представляет
интерес
как
смешанно-лигандный
моноформазанатный металлокомплекс, поскольку подобные соединения к
настоящему моменту времени известны только для рутения [106], бора [107109], и палладия [63]. Для того чтобы получить комплекс 37 в качестве
основного продукта, в реакции, представленной на схеме 2.16, мы изменили
соотношение исходных реагентов, а именно в 2 раза уменьшили количество
3,6-ди-трет-бутил-о-бензохинона. В результате соединение 37 было выделено
в виде темно-коричневого мелкокристаллического порошка с выходом ~
80%. Комплекс 37 охарактеризован по данным ИК-спектроскопии и
105
элементного анализа. Кристаллы данного комплекса, пригодные для РСА,
были выращены путем медленной кристаллизации из смеси толуол/гексан
при ~ 0°C. Основные длины связей и валентные углы в комплексе 37
приведены в таблице 2.11.
Таблица 2.11. Основные длины связей [Å] и валентные углы [°] в
комплексе 37
Связь
Угол
Co(1)-O(1)
1.8742(7)
N(1)-Co(1)-N(4)
90.22(4)
Co(1)-O(2)
1.8651(8)
N(4)-Co(1)-O(2)
92.56(4)
Co(1)-N(1)
1.8118(9)
N(1)-Co(1)-O(2)
171.97(4)
Co(1)-N(4)
1.8085(8)
N(4)-Co(1)-O(1)
173.37(4)
O(1)-C(1)
1.2971(13)
N(1)-Co(1)-O(1)
93.37(3)
O(2)-C(2)
1.2960(12)
O(2)-Co(1)-O(1)
83.16(3)
N(1)-N(2)
1.3118(12)
C(28)-N(4)-Co(1)
120.59(7)
N(2)-C(15)
1.3403(13)
C(16)-N(1)-Co(1)
119.67(7)
N(3)-C(15)
1.3401(13)
N(2)-N(1)-Co(1)
128.22(7)
N(3)-N(4)
1.3093(12)
N(3)-N(4)-Co(1)
127.84(6)
N(1)-C(16)
1.4341(12)
N(4)-C(28)
1.4353(12)
C(1)-C(2)
1.4421(13)
C(1)-C(6)
1.4263(13)
C(2)-C(3)
1.4263(15)
C(3)-C(4)
1.3719(14)
C(4)-C(5)
1.4240(14)
C(5)-C(6)
1.3717(15)
Центральный атом кобальта в комплексе 37 имеет плоско-квадратное
координационное окружение (рисунок 2.24). Плоскость металлхелатного
узла
Со(1)N(1)N(4)O(1)O(2)
расположена
относительно
плоскости
106
формазанового фрагмента под углом 27.95°. Аналогичной геометрией
обладает описанный в литературе смешанно-лигандный комплекс (3-нитро1,5-пара-толилформазанато)(1,1,1,6,6,6-гексафторацетонато)палладий(II)
[63].
Рисунок 2.24. Молекулярная структура комплекса 37. Атомы водорода не
показаны. Тепловые эллипсоиды 50% вероятности
107
Фенильные заместители при атомах азота N(1) и N(4) повернуты по
отношению к плоской азогидразонной цепи на угол 36.35°. N-N и C-N связи
внутри хелатной части формазанового фрагмента делокализованы (N(1)-N(2)
1.3118(12) Å, N(2)-C(15) 1.3403(13) Å, N(3)-C(15) 1.3401(13) Å, N(3)-N(4)
1.3093(12) Å), что характерно для анионной формы лиганда. Длины связей в
хиноновом фрагменте типичны для координированных семихиноновых
лигандов. Атом кобальта в данном комплексе находится в низкоспиновом
состоянии, о чем свидетельствуют значения длин связей Сo-O и Co-N,
которые составляют в среднем 1.87 и 1.81 Å соответственно.
Как представлено на рисунке 2.25, в кристаллической упаковке
комплекса 37 имеются короткие контакты двух типов: Co…C (3.420(2) и
3.659(2) Å) между атомом кобальта одной молекулы и атомами углерода
фенильной группы формазана другой молекулы, и CH…O (2.625(2) Å) между
атомом углерода фенильной группы формазанового лиганда и атомом
кислорода о-семихинонового лиганда соседних молекул комплекса.
Рисунок 2.25. Фрагмент кристаллической упаковки комплекса 37
108
При взаимодействии бис-формазаната кобальта(II) с 3,6-ди-трет-бутило-бензохиноном в толуоле получен еще один моно-о-семихиноновый
комплекс кобальта (38), содержащий уже не один, а два формазановых
лиганда в депротонированной форме (схема 2.17).
Схема 2.17
Комплекс 38 демонстрирует хорошо разрешенный изотропный спектр
ЭПР в среде толуола при комнатной температуре (рисунок 2.26).
Рисунок 2.26. Спектр ЭПР комплекса 38 (толуол, 298 К),
* - примесный сигнал от свободного SQ-радикала
109
Спектр
представляет
вследствие
собой
сверхтонкого
магнитным ядром
59
октет
(1:1:1:1:1:1:1:1)
взаимодействия
триплетов
неспаренного
(1:2:1)
электрона
с
Co (I = 7/2; 100%; N = 1/322) и двумя протонами в
положениях 4 и 5 о-семихинонового лиганда (ai(59Co) = 14.05 Гс и ai(1H) = 3.0
Гс). Значения g-фактора (gi =2.0004) и констант СТВ в спектре ЭПР
комплекса 38 указывают на локализацию неспаренного электрона на
органическом фрагменте – о-семихиноновом лиганде – с небольшим
переносом спиновой плотности на атом кобальта(III). Выделить комплекс 38
в индивидуальном виде, к сожалению, не удалось, что, по-видимому, связано
с его частичной диссоциацией в растворе.
2.6.3. Строение и свойства гетеролигандных комплексов марганца на
основе 3,6-ди-трет-бутил-о-бензохинона и формазанов
В
результате
трифенилформазаном
присутствии
взаимодействия
или
карбонила
марганца
с
1,3,5-
3-(4-пиридил)-1,5-дифенилформазаном
3,6-ди-трет-бутил-о-бензохинона
были
в
получены
гетеролигандные комплексы марганца 39 и 40 соответственно (схема 2.18).
Схема 2.18
110
Комплексы 39-40 охарактеризованы по данным ИК-спектроскопии,
элементного анализа и магнетохимии.
Комплекс
марганца
с
1,3,5-трифенилформазаном
(комплекс
39),
согласно данным ИК-спектроскопии, имеет строение подобное аналогичному
комплексу кобальта 31, в котором трехвалентный ион металла связан с двумя
семихиноновыми лигандами и одним анионом формазана. Характер
зависимости μэфф(Т) для комплекса 39 указывает на наличие в данном
комплексе
антиферромагнитных
обменных
взаимодействий
между
спиновыми центрами (рисунок 2.27).
Рисунок 2.27. Температурная зависимость эффективного магнитного
момента комплекса 39. Экспериментальная (▲) и теоретическая (сплошная
линия) кривые
Параметры обменного взаимодействия в комплексе 39 были определены
с применением модели, описанной выше для комплекса 1 (Mn(III), в.с., d4, S2
= 2). Наилучшее воспроизведение экспериментальных μ эфф(Т) данных
наблюдается при следующих параметрах: gSQ = 2 (фиксированное), gMn =
1.94, J = 0 (фиксированное), J1 = - 38 см-1, zJ’ = - 1.18 см-1, R2 = 3.73.10-4.
Согласно полученным значениям параметров J и J1 магнитное поведение
111
данного комплекса в основном обусловлено слабыми антиферромагнитными
обменными взаимодействиями между анион-радикальными семихиноновыми
лигандами.
Относительно строения комплекса марганца 40 с нейтральным 3-(4пиридил)замещенным формазановым лигандом можно сказать, что в отличие
от аналогичного комплекса кобальта 34, соединение 40 представляет собой
не
семихинон-катехолатный,
а
бис-о-семихиноновый
комплекс
двухвалентного марганца. В ИК-спектре комплекса 40 в области 2800 нм
(ближний
ИК-диапазон)
отсутствует
характерная
для
семихинон-
катехолатных комплексов полоса, относящаяся к переносу заряда между
лигандами в различных степенях окисления.
Эффективный магнитный момент комплекса 40 практически не зависит
от температуры в интервале 10-300 К и составляет ~ 3.15 μВ (рисунок 2.28).
Рисунок 2.28. Температурная зависимость эффективного магнитного
момента комплекса 40. Экспериментальная (■) и теоретическая (сплошная
линия) кривые
Теоретическая
кривая
наилучшим
образом
воспроизводящая
экспериментальные данные была получена при следующих параметрах: g SQ =
112
2 (фиксированное), gMn = 1.94, J = -265 см-1, J1 = 0 (фиксированное), zJ’ = 0.69 см-1, p = 3 мол. % (содержание диамагнитной примеси), R2 = 4.74.10-5.
Моделирование было проведено для системы, состоящей из трех обменносвязанных центров (S1 = S3 = 1/2 – спины семихиноновых лигандов, S2 = 3/2
для иона Mn(II)), с учетом межмолекулярного обменного взаимодействия
(zJ’). Согласно полученным данным в комплексе 40 имеют место сильные
антиферромагнитные взаимодействия между металлом и семихиноновыми
лигандами.
2.7. Гетеролигандные комплексы кобальта и марганца на основе 3,6-дитрет-бутил-о-бензохинона и 6-(4’-пиридил)-2,4-дифенилвердазила
По обменной реакции трис-о-семихинолята кобальта с 6-(4’-пиридил)·
2,4-дифенилвердазилом (Verd ) впервые получен смешанно-лигандный
комплекс, одновременно содержащий в своем составе семихиноновый и
вердазильный радикальные лиганды (схема 2.19).
Схема 2.19
Комплекс
41
охарактеризован
по
данным
ИК-,
УФ-,
ЭПР-
спектроскопии, элементного анализа и магнетохимии. На рисунке 2.29
113
представлены электронные спектры поглощения толуольных растворов
комплекса
и
свободного
вердазильного
радикала.
Видно,
что
при
координации вердазильного лиганда интенсивная полоса поглощения при
710 нм смещается в длинноволновую область, а также уменьшается
интенсивность полосы при 445 нм. Это позволяет полагать, что при
образовании комплекса вердазильный лиганд сохраняет свою радикальную
природу и не происходит его окисления до вердазилий-катиона. Наличие в
данном комплексе хиноновых лигандов в разных степенях окисления
подтверждается присутствием в ИК-спектре интенсивных полос в интервале
900 – 1200 см-1, а также наличием интенсивной полосы переноса заряда в
области 2800 нм в ближнем ИК-диапазоне (рисунок 2.30).
Рисунок 2.29. Электронные спектры поглощения комплекса 41 и свободного
·
радикала Verd (толуол, 298 К, 3.10-4 М)
114
2.0
1.8
1.6
1.4
1.2
1.0
0.8
12000
10000
8000
-1
6000
4000 см
Рисунок 2.30. Ближний ИК-спектр комплекса 41
В ЭПР-спектре комплекса 41 при температурах 230-130 К наблюдается
практически изотропный сигнал при g = 2.00 без разрешенной сверхтонкой
структуры. Ширина линии при 130 К составляет ~ 10 Гс.
Электрохимические превращения комплекса 41 были исследованы
методом циклической вольтамперометрии в растворе хлористого метилена,
соответствующие электрохимические характеристики приведены в таблице
2.12.
Таблица 2.12. Данные ЦВА для комплекса 41
Комплекс
41
E1/2
Red.1
,В
E1/2
-0.52
Red.2
,B
E1/2
-0.71
Ox.1
,B
0.20
E1/2
Ox.2
,B
0.38
(СУ-электрод, CH2Cl2, V = 0.2 B/c, 0.1 M NBu4ClO4, C = 2.10-3 М, Ar, отн.
Ag/AgCl/KCl
(нас.),
E1/2Ox./Red.
–
потенциал
полуволны
окисления/восстановления)
Согласно
данным
ЦВА
комплекс
41
характеризуется
двумя
квазиобратимыми процессами восстановления. При этом первая катодная
115
стадия аналогична второй для комплексов кобальта с формазанами
(комплексы 31 и 34) и соответствует восстановлению о-семихинонового
фрагмента до катехолатного. Второй квазиобратимый редокс-переход при 0.71 В отвечает восстановлению координированного вердазильного радикала
до моноаниона. В данном случае наблюдается незначительное смещение
редокс-показателей в анодную область по сравнению со свободным
вердазильным радикалом [63], что обусловлено смещением электронной
плотности к атому кобальта(III).
В анодной области регистрируются две квазиобратимых волны при
потенциалах +0.20 и +0.38 В, первая из которых, по-видимому, соответствует
окислению катехолатного лиганда до о-семихинонового, а вторая отвечает
редокс-превращению вердазильного лиганда (схема 2.20).
Схема 2.20
116
Измерения температурной зависимости магнитной восприимчивости,
проведенные для комплекса 41, показали, что значение эффективного
магнитного момента плавно убывает с понижением температуры в интервале
300-70 К от 2.62 μВ до 2.2 μВ (рисунок 2.31). Последнее значение близко к
теоретическому
соответствует
для
систем
из
двух
неспаренных
предполагаемому строению
комплекса
электронов,
что
CoIII(3,6-SQ)(3,6-
·
Cat)Verd , включающего в себя атом кобальта в низкоспиновом состоянии,
дианионный
катехолатный
лиганд
и
два
радикальных
лиганда:
семихиноновый и вердазильный.
Синтезированный нами аналогичный комплекс марганца 42 согласно
спектральным данным и данным магнетохимии представляет собой комплекс
двухвалентного низкоспинового марганца, связанного с тремя радикальными
лигандами: двумя семихиноновыми и одним вердазильным (схема 2.21).
Рисунок 2.31. Температурные зависимости эффективных магнитных
моментов комплексов кобальта 41 (■) и марганца 42 (▲)
117
Схема 2.21
Значение μэфф для него практически не зависит от температуры (рисунок
2.31) и близко к теоретическому 3.46 μВ, рассчитанному для системы,
состоящей из четырех спиновых центров с S = 1/2 для каждого.
118
Глава III. Экспериментальная часть
Все операции по синтезу о-семихиноновых комплексов кобальта,
марганца и железа проводили в условиях отсутствия кислорода и влаги
воздуха. Использованные в работе растворители очищали и обезвоживали по
стандартным методикам
[110-111]. Коммерчески доступные реактивы
(безводные CoCl2, MnCl2, FeCl2; 2,2’-бихинолин, анилин, п-иоданилин, пфторанилин,
2,6-диметифениланилин,
фенилгидразин,
формальдегид,
бензальдегид, 4-пиридинкарбоксальдегид) использовали без дополнительной
очистки. Исходные трис-о-семихиноновые комплексы кобальта(III) [17] и
железа(III) [48], Co(3,6-SQ)(3,6-Cat)(PPh3) (11) [17], а также формазановые
лиганды 24-29 и 6-(4-пиридил)-2,4-дифенилвердазильный радикал [101-102]
получали по известным методикам. Нейтральные азотсодержащие лиганды
L(I)-L(VII) были любезно предоставлены сотрудниками лаборатории ХЭОС.
Амальгамы металлов получали согласно рекомендациям [112].
ИК-спектры регистрировали в вазелиновом масле в кюветах из KBr на
ИК-Фурье-спектрометрах ФСМ–1201 (диапазон 4000–450 см−1), а также на
Bruker Vertex 70 (диапазон 12000–4000 см−1). Электронные спектры
поглощения регистрировали на УФ-спектрометре Perkin–Elmer Lambda 25
UV–Vis в диапазоне 300–1100 нм. C, H, N - анализ был проведен на
элементном анализаторе Euro EA 3000. Спектры ЭПР были зафиксированы
на спектрометре Bruker-EMX (рабочая частота ~ 9.7 ГГц). В качестве
стандарта при определении g-фактора использовали дифенилпикрилгидразил
(gi = 2.0037). Спектры ЯМР регистрировали в CDCl3 на приборе Bruker DPX200 (200 МГц), внутренний эталон – тетраметилсилан.
Измерения магнитной восприимчивости комплексов проведены в
Международном
Российской
Томографическом
академии
наук
(г.
Центре
Новосибирск)
Сибирского
на
Отделения
MPMS-5S
SQUID
магнетометре (магнитное поле 0.5 Тл) в температурном интервале 2-300 К.
119
Компьютерное моделирование магнитных свойств комплексов 1, 2, 7,
17-23, 38-39 и определение параметров обменного взаимодействия между
парамагнитными центрами в них проведено с помощью программных
средств Mjollnir [113-114].
Электрохимические
исследования
проведены
в
ФГОУ
ВПО
«Астраханский государственный технический университет». Измерение
потенциалов окисления/восстановления проводилось методом циклической
вольтамперометрии
(ЦВА)
в
трехэлектродной
ячейке
с
помощью
потенциостата «IPC-pro» в среде аргона. Рабочий электрод – стационарный
стеклоуглеродный (СУ) или платиновый электроды с диаметром 2 мм,
вспомогательный электрод – платиновая пластина (S = 18 мм2). Электрод
сравнения
(Ag/AgCl/KCl)
с
водонепроницаемой
диафрагмой.
Число
электронов, переносимых в ходе электродного процесса оценивалось
относительно стандарта – ферроцена. Скорость развертки потенциала
0.2 В∙с-1. Фоновый электролит – 0.1 М Bu4NClO4 (99% ,«Acros») дважды
перекристаллизованный из водного EtOH и высушенный в вакууме 48 ч при
50 0С.
Рентгеноструктурный анализ комплексов проведен на дифрактометрах
Smart Apex (Bruker AXS), Oxford Diffraction (Gemini S) и Bruker D8 Quest.
Кристаллографические данные для полученных соединений, а также
основные детали рентгеноструктурного эксперимента и уточнения структур
приведены в таблице 3.1.
120
Таблица 3.1. Кристаллографические данные и параметры рентгеноструктурного анализа соединений
Соединение
Формула
Молекулярная масса
Температура, К
Длина волны, Å
Сингония
Пространственная группа
a, Å
b, Å
c, Å
α, град
β, град
γ, град
Объем, Å3
Z
dвыч, г/см3
Коэффициент адсорбции, мм-1
Общее число измеренных отражений
Число независимых отражений
Число уточняемых параметров
R1/wR2 [I>2σ(I)]
R1/wR2 (по всем данным)
GOF(F2)
Остаточная электронная
плотность, e.Å-3
Co(3,6-SQ)2L(I).C7H8
(1.C7H8)
C48H61CoNO4S
806.97
100(2)
0.71073
Орторомбическая
P2(1)2(1)2(1)
10.2292(8)
18.9411(15)
22.7168(18)
90
90
90
4401.4(6)
4
1.218
0.480
37306
8642 [R(int) = 0.0938]
500
0.0556/0.1096
0.0840/0.1174
1.013
Zn(3,6-SQ)2L(II).0.5C7H8
(12.0.5C7H8)
C50.50H67NO4Zn
817.42
100(2)
0.71073
Триклинная
P-1
10.3944(2)
13.3925(3)
18.2028(4)
81.7639(17)
76.902(2)
69.2526(19)
2302.48(9)
2
1.179
0.576
40454
11076 [R(int) = 0.0601]
546
0.0393/0.0621
0.0639/0.0664
1.010
Co(3,6-SQ)2L(VI).Et2O
(13.Et2O)
C52H74CoN2O6
882.06
298(2)
0.71073
Моноклинная
P121/n1
9.9528(17)
28.906(3)
17.576(4)
90
93.199(18)
90
5048.6(15)
4
1.16
0.387
20161
10215 [R(int) = 0.0745]
550
0.0635/0.1172
0.1733/0.1366
0.889
0.691/-0.490
0.431/-0.371
0.385/-0.281
121
Продолжение таблицы 3.1
Соединение
Формула
Молекулярная масса
Температура, К
Длина волны, Å
Сингония
Пространственная группа
a, Å
b, Å
c, Å
α, град
β, град
γ, град
Объем, Å3
Z
dвыч, г/см3
Коэффициент адсорбции, мм-1
Общее число измеренных отражений
Число независимых отражений
Число уточняемых параметров
R1/wR2 [I>2σ(I)]
R1/wR2 (по всем данным)
GOF(F2)
Остаточная электронная
плотность, e.Å-3
(3,6-Cat)(4-Py-(Me2Ph)-FormH)SbPh3.C7H8
(30а)
C59H62N5O2Sb
994.89
100(2)
0.71073
Моноклинная
P2(1)/c
16.06742(18)
16.3782(2)
19.7511(3)
90
101.1886(12)
90
5098.83(12)
4
1.296
0.588
38980
14779 [R(int) = 0.0466]
617
0.0396/0.0641
0.0712/0.0696
0.949
(3,6-Cat)(4-Py-(Me2Ph)-FormH)SbPh3
(30б)
C52H54N5O2Sb
902.75
100(2)
0.71073
Моноклинная
P2(1)/c
23.6371(8)
10.4595(3)
18.0271(3)
90
93.984(2)
90
4446.1(2)
4
1.349
0.667
60979
7805 [R(int) = 0.1604]
529
0.0697/0.1358
0.1044/0.1494
1.052
Co(3,6-SQ)(Ph-Form)
(37)
C33H35CoN4O2
578.58
100(2)
0.71073
Триклинная
P-1
9.6090(9)
10.7936(11)
14.8816(15)
99.022(2)
103.509(2)
103.094(2)
1425.4(2)
2
1.348
0.639
19004
8246 [R(int) = 0.0236]
367
0.0358/0.0881
0.0443/0.0912
1.066
0.707/-0.688
0.790/-0.797
0.897/-0.417
122
Синтез бис-о-семихиноновых комплексов кобальта, марганца и железа с
нейтральными N-донорными лигандами
Co(3,6-SQ)2L(I) (1)
Метод 1. К навеске 0.140 г (0.41 ммоль) карбонила кобальта добавляли
навеску 0.177 г (0.82 ммоль) L(I). Затем в эту ампулу приливали раствор
0.360 г (1.64 ммоль) 3,6-ди-трет-бутил-о-бензохинона в диэтиловом эфире.
Содержимое ампулы перемешивали в течение 20 мин, периодически удаляя
из нее выделяющийся в ходе реакции оксид углерода(II). После окончания
реакции раствор сутки выдерживали при температуре ~0ºС. Выпавший
мелкокристаллический порошок темно-зеленого цвета отфильтровывали и
сушили в вакууме. Выход 0.523 г (89 %).
Метод 2. К раствору 0.100 г (0.14 ммоль) трис(3,6-ди-трет-бутил-обензосемихинон)кобальта в ~ 20 мл диэтилового эфира приливали раствор
0.015 г (0.14 ммоль) L(I) в ~ 15 мл диэтилового эфира. Полученный раствор
после упаривания до момента начала кристаллообразования раствор
выдерживали при температуре ~0ºС. Выпавшие кристаллы отфильтровывали
и сушили в вакууме. Выход 0.075 г (75 %).
Метод 3. Вакуумированную ампулу, содержащую 0.17 г (0.77 ммоль)
3,6-ди-трет-бутил-о-бензохинона в ~30 мл ТГФ и избыток амальгамы
таллия интенсивно встряхивали до тех пор, пока цвет раствора не переставал
изменяться (цвет менялся с зеленого на оранжевый). Полученный раствор
катехолата таллия осторожно декантировали в другую ампулу. Амальгаму
промывали тетрагидрофураном. К полученному раствору катехолата таллия
при перемешивании добавляли еще одну порцию раствора 3,6-ди-третбутил-о-бензохинона. Полученный раствор семихинолята таллия окрашен в
сине-зеленый цвет. В ампулу, содержащую 0.1 г (0.77 ммоль) безводного
дихлорида кобальта в ~15 мл ТГФ добавляли раствор 0.166 г (0.77 ммоль)
L(I) в ~ 15 мл ТГФ и туда же при перемешивании приливали полученный
раствор семихинолята таллия. Реакционную смесь встряхивали в течение
123
получаса, отфильтровывали осадок TlCl, заменяли ТГФ на толуол и
фильтровали
повторно.
кристаллообразования
После
раствор
упаривания
выдерживали
до
при
момента
начала
температуре
~0ºС.
Выпавшие темно-зеленые кристаллы отфильтровывали и сушили в вакууме.
Маточный раствор упаривали и выставляли на холод. Вновь выпавшие
кристаллы выделяли аналогично. Выход 0.473 г (86 %).
Темно-зеленые кристаллы пригодные для РСА были выращены из
толуола.
Вычислено для C41H53CoNO4S (%): C, 68.89; H, 7.47; Co, 8.24; N, 1.96;
O, 8.95; S, 4.49. Найдено (%): C, 68.59; H, 7.23; Co, 8.51; N+S, 6.60
ИК (ваз. масло, ν, см-1): 1656 сл., 1603 с., 1591 сл., 1580 с., 1544 с., 1442
с., 1414 сл., 1387 с., 1355 ср., 1337 с., 1275 ср., 1244 ср., 1218 ср., 1208 сл.,
1180 сл., 1164 сл., 1114 сл., 1089 сл., 1027 сл., 964 сл., 955 с., 876 сл., 844 с.,
829 с., 805 сл., 791 сл., 768 с., 733 с., 696 ср., 675 сл., 654 с., 609 сл., 571 сл.,
546 сл., 507 сл., 494 сл., 466 сл., 438 сл.
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 396 (3900), 505 (1100), 601 (1000),
784 (1500), 826 (1500).
Co(3,6-SQ)2L(II) (2)
Комплекс был получен при взаимодействии 0.228 г (0.67 ммоль)
карбонила кобальта с 0.353 г (1.33 ммоль) L(II) и раствором 0.587 г (2.67
ммоль) 3,6-ди-трет-бутил-о-бензохинона в диэтиловом эфире по методу 1
аналогичному для комплекса 1. Выделенный комплекс представляет собой
зеленый мелкокристаллический порошок. Выход 0.923 г (91 %)
Вычислено для C47H63CoNO4 (%): C, 73.80; H, 8.30; Co, 7.70; N, 1.83; O,
8.37. Найдено (%): C, 73.41; H, 8.21; Co, 7.53; N, 2.15.
ИК (ваз. масло, ν, см-1): 1553 сл., 1432 с., 1425 с., 1391 ср., 1358 сл.,
1350 ср., 1289 сл., 1279 сл., 1211 сл., 1201 сл., 1184 сл., 1030 сл., 978 ср., 961
с., 831 с., 808 сл., 728 сл., 688 сл., 650 ср., 579 ср., 500 ср.
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 396 (3600), 600 (1200), 695 (1100).
124
Co(3,6-SQ)2L(III) (3)
Комплекс был получен при взаимодействии 0.140 г (0.41 ммоль)
карбонила кобальта с 0.172 г (0.82 ммоль) L(III) и раствором 0.360 г (1.64
ммоль) 3,6-ди-трет-бутил-о-бензохинона в диэтиловом эфире по методу 1
аналогичному для комплекса 1. Выделенный комплекс представляет собой
мелкие кристаллы черного цвета. Выход 0.515 г (88 %)
Вычислено для C42H54CoN2O4 (%):C, 71.07; H, 7.67; Co, 8.30; N, 3.95; O,
9.02. Найдено (%): C, 71.36; H, 8.01; Co, 7.99; N, 3.73.
ИК (ваз. масло, ν, см-1): 1632 сл., 1598 ср., 1542 сл., 1467 с., 1445 с.,
1386 ср., 1362 сл., 1355 ср., 1341 ср., 1304 сл., 1274 сл., 1201 сл., 1183 сл.,
1119 сл., 1093 сл., 1017 сл., 964 ср., 953 с., 907 сл., 825 с., 771 ср., 764 с., 748
сл., 723 сл., 670 сл., 652 с., 505 сл., 484 сл., 436 сл.
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 340 (11700), 586 (2300), 699
(2800), 806 (2400).
Co(3,6-SQ)2L(IV) (4)
Комплекс был получен при взаимодействии 0.100 г (0.14 ммоль) трисо-семихинолята кобальта и 0.036 г (0.15 ммоль) L(IV) по методу 2
аналогичному для комплекса 1. Комплекс выделен в виде темных синезеленых игольчатых кристаллов. Выход 0.075 г (73 %).
Вычислено для C44H58CoN2O4 (%):C, 71.62; H, 7.92; Co, 7.99; N, 3.80; O,
8.67. Найдено (%): C, 71.87; H, 8.19; Co, 7.70; N, 3.62.
ИК (ваз. масло, ν, см-1): 1631 ср., 1595 с., 1571 сл., 1543 с., 1440 с., 1356
ср., 1340 ср., 1304 ср., 1273 ср., 1225 сл., 1204 ср., 1177 ср., 1157 сл., 1105 ср.,
1050 ср., 1017 ср., 998 сл., 978 сл., 963 сл., 953 с., 930 сл., 908 сл., 851 сл., 779
сл., 770 с., 754 ср., 723 сл., 699 сл., 671 сл., 654 с., 637 сл., 569 сл., 533 сл., 504
ср., 488 ср., 439 сл., 421 ср.
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 335 (9200), 580 (1400), 699 (1800),
807 (1400).
125
Co(3,6-SQ)2L(V) (5)
Комплекс был получен при взаимодействии 0.072 г (0.10 ммоль) трисо-семихинолята кобальта и 0.035 г (0.12 ммоль) L(V) по методу 2
аналогичному для комплекса 1. Выделенный комплекс представляет собой
мелкие игольчатые кристаллы темно-зеленого цвета. Выход 0.064 г (81 %).
Вычислено для C48H66CoN2O4 (%):C, 72.61; H, 8.38; Co, 7.42; N, 3.53; O,
8.06. Найдено (%): C, 72.30; H, 8.11; Co, 7.20; N, 3.32.
ИК (ваз. масло, ν, см-1): 1627 ср., 1594 с., 1570 сл., 1542 ср., 1497 сл.,
1466 с., 1440 с., 1386 с., 1363 с., 1354 с., 1338 ср., 1304 сл., 1295 сл., 1275 сл.,
1266 сл., 1253 сл., 1226 сл., 1203 ср., 1179 сл., 1157 сл., 1149 сл., 1135 сл.,
1106 сл., 1067 сл., 1053 сл., 1024 сл., 1015 ср., 1000 сл., 979 сл., 963 сл., 952 с.,
900 ср., 877 сл., 821 с., 772 с., 748 сл., 700 сл., 670 сл., 651 с., 586 с., 541 ср.,
504 ср., 483 сл., 435 сл.
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 341 (12000), 586 (1900), 721
(2500), 804 (2300).
Mn(3,6-SQ)2L(I) (6)
В ампулу, содержащую 0.126 г (1 ммоль) безводного дихлорида
марганца, добавляли навеску 0.215 г (1 ммоль) L(I). После чего, содержимое
ампулы растворяли в ~30 мл ТГФ и при перемешивании приливали туда
свежеприготовленный раствор о-семихинолята таллия. Реакционную смесь
интенсивно
перемешивали
в
течение
нескольких
суток.
Затем
отфильтровывали осадок TlCl и заменяли ТГФ на толуол, еще раз
отфильтровывали TlCl и заменяли толуол на гексан. После упаривания до
момента
начала
температуре
~
кристаллообразования
0°C.
Выпавший
раствор
темный
выдерживали
при
зелено-коричневый
мелкокристаллический осадок отфильтровывали и сушили в вакууме.
Маточный раствор упаривали и выставляли на холод. Вновь выпавшие
кристаллы выделяли аналогично. Выход 0.598 г (84 %).
126
Вычислено для C41H53MnNO4S(%): C, 69.27; H, 7.51; Mn, 7.73; N, 1.97;
O, 9.00; S, 4.51. Найдено (%): C, 69.59; H, 7.23; Mn, 7.91; N+S, 6.60.
ИК (ваз. масло, ν, см-1): 1658 сл., 1607 с., 1591 сл., 1553 с., 1483 сл.,
1466 с., 1427 сл., 1414 ср., 1393 сл., 1364 сл., 1335 сл., 1284 сл., 1240 ср., 1217
ср., 1205 сл., 1165 сл., 1149 сл., 1114 сл., 1090 сл., 1057 сл., 1028 сл., 1004 сл.,
978 с., 953 с., 922 ср., 870 сл., 836 с., 810 сл., 793 ср., 770 ср., 744 с., 729 сл.,
702 сл., 650 с., 622 ср., 601 ср., 556 сл., 502 ср.
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 342 (7300), 411 (3900), 677 (800),
807 (1600), 883 (1300).
Mn(3,6-SQ)2L(III) (7)
Комплекс был получен при взаимодействии о-семихинолята таллия с
0.150 г (1.19 ммоль) безводного дихлорида марганца и 0.210 г (1 ммоль)
L(III) по методу аналогичному для комплекса 6. Комплекс выделен из
толуола в виде зелено-коричневых игольчатых кристаллов. Выход 0.563 г (80
%).
Вычислено для C42H54MnN2O4 (%): C, 71.47; H, 7.71; Mn, 7.78; N, 3.97;
O, 9.07. Найдено (%): C, 71.69; H, 7.78; Mn, 8.19; N, 3.52.
ИК (ваз. масло, ν, см-1): 1622 сл., 1589 ср., 1569 сл., 1548 сл., 1399 сл.,
1368 сл., 1355 сл., 1342 сл., 1301 сл., 1282 сл., 1264 сл., 1241 ср., 1203 сл.,
1174 сл., 1154 сл., 1142 сл., 1093 сл., 1079 сл., 1043 сл., 1028 сл., 1014 ср., 980
ср., 953 сл., 936 сл., 920 сл., 910 сл., 833 сл., 808 сл., 792 ср., 767 с., 728 с., 695
с., 675 сл., 652 с., 639 сл., 592 ср., 552 сл., 535 сл., 502 сл., 485 сл., 457 сл.
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 410 (2900), 740 (400), 800 (400),
925 (300).
Mn(3,6-SQ)2L(V) (8)
Комплекс был получен при взаимодействии о-семихинолята таллия с 0.064 г
(0.50 ммоль) безводного дихлорида марганца и 0.150 г (0.51 ммоль) L(V) по
127
методу аналогичному для комплекса 6. Комплекс выделен из толуола в виде
мелких черно-коричневых кристаллов. Выход 0.271 г (69 %).
Вычислено для C48H66MnN2O4 (%): C, 72.98; H, 8.42; Mn, 6.95; N, 3.55;
O, 8.10. Найдено (%): C, 73.20; H, 8.61; Mn, 7.20; N, 3.34.
ИК (ваз. масло, ν, см-1): 1633 сл., 1591 ср., 1570 сл., 1545 сл., 1485 сл.,
1365 сл., 1353 сл., 1343 сл., 1304 сл., 1266 сл., 1202 сл., 1156 сл., 1149 сл.,
1103 сл., 1050 сл., 1013 ср., 951 ср., 938 сл., 897 ср., 870 сл., 820 с., 695 сл.,
670 сл., 649 с., 636 сл., 584 сл., 537 сл., 500 сл., 478 сл., 463 сл., 434 сл.
Fe(3,6-SQ)2L(I) (9)
К
раствору
0.130
г
(0.18
ммоль)
трис(3,6-ди-трет-бутил-о-
бензосемихинон)железа в ~ 20 мл гексана приливали раствор 0.041 г (0.19
ммоль) L(I) в ~ 15 мл гексана. Полученный раствор после упаривания до
момента начала кристаллообразования выдерживали при температуре ~0ºС.
Выпавшие темно-зеленые кристаллы отфильтровывали и сушили в вакууме.
Выход 0.096 г (75 %).
Вычислено для C41H53FeNO4S(%): C, 69.18; H, 7.51; Fe, 7.85; N, 1.97; O,
8.99; S, 4.50. Найдено (%): C, 69.29; H, 7.43; Fe, 7.91; N+S, 6.60
ИК (ваз. масло, ν, см-1): 1679 сл., 1657 сл., 1549 с., 1435 с., 1389 ср.,
1358 ср., 1279 с., 1200 ср., 1182 ср., 1026 ср., 969 с., 957 с., 930 сл., 898 сл.,
844 ср., 836 с., 829 с., 806 ср., 721 сл., 700 сл., 678 с., 650 с., 551 с., 492 с., 441
ср., 418 сл., 408 сл.
Fe(3,6-SQ)2L(III) (10)
Комплекс был получен при взаимодействии 0.130 г (0.18 ммоль)
трис(3,6-ди-трет-бутил-о-бензосемихинон)железа и 0.040 г (0.19 ммоль)
L(III) по методу аналогичному для комплекса 9. Комплекс выделен в виде
темного мелкокристаллического осадка. Выход 0.085 г (67 %).
Вычислено для C42H54FeN2O4 (%): C, 71.38; H, 7.70; Fe, 7.90; N, 3.96; O,
9.06. Найдено (%): C, 71.69; H, 7.68; Fe, 8.19; N, 3.82.
128
ИК (ваз. масло, ν, см-1): 1675 ср., 1656 с., 1632 ср., 1596 ср., 1571 сл.,
1550 сл., 1482 с., 1436 с., 1359 с., 1304 сл., 1285 ср., 1259 сл., 1199 сл., 1181
ср., 1155 сл., 1093 сл., 1047 сл., 1020 ср., 979 сл., 970 сл., 956 ср., 939 с., 924
сл., 907 сл., 898 сл., 833 сл., 808 сл., 793 ср., 767 с., 747 сл., 722 сл., 698 сл.,
679 ср., 652 с., 580 сл., 547 ср., 492 ср., 463 сл.,445 сл.
Zn(3,6-SQ)2L(II) (12)
К избытку амальгамированного цинка последовательно приливали
раствор 0.220 г (1 ммоль) 3,6-ди-трет-бутил-о-бензохинона в ~ 30 мл толуола
и раствор 0.133 г (0.50 ммоль) L(II) в ~ 15 мл толуола. При интенсивном
перемешивании при комнатной температуре в течение нескольких часов
окраска реакционной смеси изменялась от красно-зеленой до темной синезеленой. Раствор отделяли от избытка цинка фильтрованием. Полученный
раствор после упаривания до момента начала кристаллообразования
выдерживали
при
температуре
~0ºС.
Выпавшие
темно-зеленые
палочковидные кристаллы отфильтровывали и сушили в вакууме. Выход
0.212 г (55 %).
Вычислено для C47H63ZnNO4 (%): C, 73.18; H, 8.23; Zn, 8.48; N, 1.82; O,
8.30. Найдено (%): C, 73.27; H, 8.19; Zn, 8.34; N, 1.97.
ИК (ваз. масло, ν, см-1): 1625 c., 1598 ср., 1592 ср., 1578 сл., 1547 сл.,
1504 с., 1490 с., 1445 с., 1361 сл., 1356 ср., 1343 ср., 1322 сл., 1305 сл., 1286
сл., 1272 сл., 1254 сл., 1204 с., 1189 ср., 1180 сл., 1159 сл., 1103 сл., 1096 сл.,
1080 сл., 1056 сл., 1027 сл., 990 сл., 954 с., 892 с., 824 с., 802 ср., 774 с., 755 с.,
730 с., 711 сл., 688 ср., 673 ср., 654 с., 545 ср., 498 ср.
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 339 (5700), 399 (2100).
Co(3,6-SQ)2L(VI) (13)
Комплекс был получен при взаимодействии о-семихинолята таллия с
0.1 г (0.77 ммоль) безводного дихлорида кобальта и 0,237 г (0,77 ммоль)
L(VI) по методу 3 аналогичному для комплекса 1. Выход 0.513 г (83 %).
129
Кристаллы пригодные для РСА получены медленной кристаллизацией
из диэтилового эфира.
Вычислено для C48H64CoN2O5(%): C, 71.35; H, 7.98; Co, 7.29; N, 3.47; O,
9.90. Найдено (%): C, 71.64; H, 8.13; Co, 7.53; N, 3.29.
ИК (ваз. масло, ν, см-1): 1627 сл., 1573 сл., 1550 ср., 1446 с., 1365 с.,
1353 ср., 1343 ср., 1310 сл., 1292 сл., 1274 сл., 1241 сл., 1205 ср., 1179 сл.,
1154 сл., 1132 ср., 1087 сл., 1042 сл., 1025 сл., 1009 сл., 955 с., 929 сл., 916 с.,
892 сл., 875 ср., 837 ср., 825 с., 791 сл., 741 сл., 728 с., 703 сл., 671 сл., 653 с.,
633 сл., 620 сл., 597 сл., 532 сл., 521 сл., 504 сл., 495 ср., 487 ср., 463 сл., 432
ср., 413 ср.
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 483 (2100), 541 (2000), 796 (3100).
Mn(3,6-SQ)2L(VI) (14)
Комплекс был получен при взаимодействии о-семихинолята таллия с
0.126 г (1 ммоль) безводного дихлорида марганца и 0.308 г (1 ммоль) L(VI)
по методу аналогичному для комплекса 6. Комплекс выделен из гексана в
виде темно-зеленого мелкокристаллического осадка. Выход 0.576 г (72 %).
Вычислено для C48H64MnN2O5(%): C, 71.71; H, 8.02; Mn, 6.83; N, 3.48; O,
9.95. Найдено (%): C, 71.84; H, 8.38; Mn, 6.26; N, 3.68.
ИК (ваз. масло, ν, см-1): 1658 сл., 1626 сл., 1578 сл., 1553 ср., 1488 с.,
1443 с., 1373 с., 1353 ср., 1342 ср., 1295 сл., 1264 сл., 1240 сл., 1201 сл., 1180
сл., 1149 сл., 1129 ср., 1087 сл., 1046 сл., 966 сл., 954 с., 876 ср., 835 сл., 820
ср., 790 ср., 745 сл., 729 сл., 704 с., 672 сл., 653 ср., 633 сл., 526 сл., 503 сл.,
480 сл.
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 406 (6300), 590 (300).
Fe(3,6-SQ)2L(VI) (15)
В ампулу, содержащую навеску 0.050 г (0.39 ммоль) безводного
дихлорида железа, добавляли раствор 0.122 г (0.39 ммоль) L(VI) в ~ 10 мл
ТГФ (цвет раствора менялся с желтого на синий). После чего, при
130
перемешивании приливали туда же свежеприготовленный раствор осемихинолята таллия. Реакционную смесь интенсивно перемешивали в
течение нескольких суток. Затем отфильтровывали осадок TlCl и заменяли
ТГФ на толуол, еще раз отфильтровывали TlCl и заменяли толуол на гексан.
После упаривания до момента начала кристаллообразования раствор
выдерживали
при
температуре
~
0°C.
Выпавший
фиолетовый
мелкокристаллический осадок отфильтровывали и сушили в вакууме.
Маточный раствор упаривали и выставляли на холод. Вновь выпавшие
кристаллы выделяли аналогично. Выход 0.213 г (67 %).
Вычислено для C48H64FeN2O5(%): C, 71.63; H, 8.01; Fe, 6.94; N, 3.48; O,
9.94. Найдено (%): C, 71.46; H, 8.08; Fe, 6.72; N, 3.32.
ИК (ваз. масло, ν, см-1): 1626 сл., 1571 сл., 1551 с., 1480 с., 1442 с., 1365
с., 1357 ср., 1350 ср., 1281 ср., 1263 ср., 1241 сл., 1202 ср., 1158 сл., 1132 с.,
1088 сл., 1042 сл., 1028 сл., 1017 сл., 1006 сл., 978 ср., 974 ср., 958 ср., 939 с.,
923 сл., 873 ср., 831 ср., 809 сл., 793 с., 749 ср., 721 сл., 706 с., 679 ср., 652 ср.,
636 сл., 586 сл., 545 ср., 494 с., 466 ср.
Co(3,6-SQ)2L(VII) (16)
Комплекс был получен при взаимодействии о-семихинолята таллия с
0.1 г (0.77 ммоль) безводного дихлорида кобальта и 0.241 г (0.77 ммоль)
L(VII) по методу 3 аналогичному для комплекса 1. Комплекс выделен в виде
темного сине-зеленого мелкокристаллического осадка. Выход 0.493 г (79 %).
Вычислено для C47H63CoNO5S (%):C, 69.43; H, 7.81; Co, 7.25; N, 1.72; O,
9.84; S, 3.94. Найдено (%): C, 68.99; H, 7.53; Co, 7.40; N+S, 5.31.
ИК (ваз. масло, ν, см-1): 1566 ср., 1546 сл., 1508 сл., 1441 с., 1367 с.,
1342 сл., 1303 сл., 1287 сл., 1271 сл., 1244 сл., 1228 сл., 1203 сл., 1171 сл.,
1086 сл., 1070 ср., 1027 сл., 966 сл., 955 с., 869 сл., 854 сл., 842 сл., 825 сл.,
723 с., 708 сл., 674 сл., 653 сл., 505 сл., 495 сл.
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 400 (5500), 591 (1700), 769 (3300),
803 (3200).
131
Co(3,6-SQ)2Biq (17)
Комплекс был получен при взаимодействии 0.072 г (0.10 ммоль) трисо-семихинолята кобальта и 0.030 мг (0.12 ммоль) 2,2`-бихинолина по методу
2 аналогичному для комплекса 1. Комплекс выделен в виде зеленого
мелкокристаллического порошка. Выход 0.054 г (72 %).
Вычислено для C46H52CoN2O4 (%): C, 73.10; H, 6.93; Co, 7.80; N, 3.71; O,
8.47. Найдено (%): C, 73.41; H, 6.98; Co, 7.93; N, 3.65.
ИК (ваз. масло, ν, см-1): 1619 сл., 1595 ср., 1546 сл., 1508 ср., 1481 ср.,
1448 с., 1365 сл., 1353 сл., 1343 сл., 1273 сл., 1207 сл., 1201 сл., 1179 сл., 1142
сл., 1096 сл., 1023 сл., 963 ср., 950 с., 869 сл., 816 с., 783 с., 749 с., 723 ср., 669
сл., 652 с., 626 сл., 529 сл., 503 ср., 487 ср., 432 сл.
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 591 (1900), 725 (2800), 808 (2500).
Mn(3,6-SQ)2(Biq) (18)
К навеске 0.195 г (0.50 ммоль) карбонила марганца добавляли раствор
0.320 г (1.25 ммоль) 2,2`-бихинолина в толуоле. Затем в эту ампулу
приливали раствор 0.440 г (2 ммоль) 3,6-ди-трет-бутил-о-бензохинона в
толуоле. Ампулу с реакционной смесью облучали в течение трех суток
видимым светом. Выпавший мелкокристаллический осадок темно-зеленого
цвета отфильтровывали и сушили в вакууме. Выход 0.647 г (86 %).
Вычислено для C46H52MnN2O4 (%): C, 73.48; H, 6.97; Mn, 7.31; N, 3.73;
O, 8.51. Найдено (%): C, 73.61; H, 6.99; Mn, 7.59; N, 3.66.
ИК (ваз. масло, ν, см-1): 1620 сл., 1597 с., 1548 сл., 1511 с., 1489 с., 1471
с., 1445 с., 1432 с., 1363 ср., 1354 ср., 1344 ср., 1298 сл., 1273 сл., 1201 сл.,
1180 сл., 1145 сл., 1095 ср., 1025 сл., 976 сл., 964 сл., 948 с., 818 с., 787 с., 776
сл., 751 с., 728 сл., 695 сл., 669 сл., 652 ср., 617 сл., 525 сл., 502 сл., 480 сл.
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 405 (4900), 585 (400).
132
Fe(3,6-SQ)2(Biq) (19)
Комплекс был получен при взаимодействии о-семихинолята таллия с
0.127 г (1 ммоль) безводного дихлорида железа и 0.256 г (1 ммоль) 2,2`бихинолина по методу аналогичному для комплекса 15. Комплекс выделен из
толуола в виде темного мелкокристаллического сине-зеленого осадка. Выход
0.683 г (91 %).
Вычислено для C46H52FeN2O4 (%): C, 73.40; H, 6.96; Fe, 7.42; N, 3.72; O,
8.50. Найдено (%): C, 73.52; H, 6.85; Fe, 7.59; N, 3.52.
ИК (ваз. масло, ν, см-1): 1620 сл., 1595 ср., 1547 сл., 1511 с., 1478 с.,
1438 с., 1365 с., 1352 ср., 1300 сл., 1283 сл., 1200 сл., 1181 сл., 1146 сл., 1096
сл., 1025 сл., 979 сл., 968 сл., 950 сл., 940 сл., 925 сл., 872 сл., 833 сл., 818 с.,
783 ср., 751 ср., 722 ср., 649 ср., 620 сл., 536 сл., 492 сл.
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 360 (13000), 421 (3200), 643
(4000).
Co(3,6-SQ)2DAD (20)
Комплекс был получен при взаимодействии о-семихинолята таллия с
0.1 г (0.77 ммоль) безводного дихлорида кобальта и 0.168 г (0.77 ммоль) 1,4ди-трет-бутил-1,4-диазабутадиена
комплекса
1.
Комплекс
по
методу
выделен
в
3
аналогичному
виде
для
темно-зеленого
мелкокристаллического осадка. Выход 0.384 г (75 %).
Вычислено для C38H60CoN2O4 (%): C, 68.34; H, 9.06; Co, 8.82; N, 4.19; O,
9.58. Найдено (%): C, 68.41; H, 8.98; Co, 8.93; N, 4.25.
ИК (ваз. масло, ν, см-1): 1650 сл., 1548 с., 1439 с., 1362 ср., 1353 с., 1341
с., 1278 ср., 1238 с., 1223 сл., 1203 с., 1182 сл., 1065 сл., 1035 сл., 1027 сл., 979
с., 965 с., 954 с., 927 ср., 895 ср., 882 сл., 826 с., 805 сл., 761 сл., 721 сл., 700
сл., 672 ср., 654 с., 533 сл., 506 с., 485 ср., 436 сл.
133
Mn(3,6-SQ)2DAD (21)
Комплекс был получен при взаимодействии 0.130 г (0.33 ммоль)
карбонила марганца с 0.294 г (1.34 ммоль) 3,6-ди-трет-бутил-о-бензохинона и
0.224 г (1.34 ммоль) 1,4-ди-трет-бутил-1,4-диазабутадиена по методу
аналогичному для комплекса 18. Комплекс выделен из смеси диэтиловый
эфир/гексан в виде темно-зеленого мелкокристаллического осадка. Выход
0.415 г (63%).
Вычислено для C38H60MnN2O4 (%): C, 68.75; H, 9.11; Mn, 8.28; N, 4.22;
O, 9.64. Найдено (%): C, 68.48; H, 9.18; Mn, 8.03; N, 4.35.
ИК (ваз. масло, ν, см-1): 1546 сл., 1487 с., 1448 с., 1413 сл, 1353 ср., 1345
ср., 1276 сл, 1237 сл., 1205 ср., 1179 сл., 1034 сл, 1024 сл., 976 ср., 952 с., 929
сл., 901 сл., 880 сл., 823 ср., 760 сл., 720 сл., 670 сл., 654 ср., 526 сл., 503 сл.,
476 сл.
Fe(3,6-SQ)2DAD (22)
Комплекс был получен при взаимодействии о-семихинолята таллия с
0.1 г (0.79 ммоль) безводного дихлорида железа и 0.133 г (0.79 ммоль) 1,4-дитрет-бутил-1,4-диазабутадиена по методу аналогичному для комплекса 15.
Комплекс выделен из гексана в виде темно-зеленого мелкокристаллического
осадка. Выход 0.373 г (71 %).
Вычислено для C38H60FeN2O4 (%): C, 68.66; H, 9.10; Fe, 8.40; N, 4.21; O,
9.63. Найдено (%): C, 68.61; H, 9.12; Fe, 8.73; N, 4.30.
ИК (ваз. масло, ν, см-1): 1550 ср., 1479 с., 1466 с., 1440 с., 1396 ср., 1387
с., 1365 ср., 1354 ср., 1283 ср., 1259 сл., 1239 ср., 1202 с., 1114 сл., 1068 сл.,
1038 сл., 1026 сл., 979 с., 970 ср., 954 ср., 941 ср., 926 сл., 901 сл., 881 сл., 835
сл., 808 сл., 792 ср., 765 сл., 721 сл., 701 сл., 678 сл., 652 с., 544 сл., 539 сл.,
491 с., 465 сл., 440 сл.
134
Co(3,6-SQ)2(DABCO) (23)
Комплекс был получен при взаимодействии 0.188 г (0.26 ммоль) трисо-семихинолята кобальта и 0.030 мг (0.27 ммоль) DABCO по методу 2
аналогичному для комплекса 1. Комплекс выделен из диэтилового эфира в
виде серо-зеленого мелкокристаллического осадка. Выход 0.144 г (91 %).
Вычислено для C34H52CoN2O4 (%): C, 66.76; H, 8.57; Co, 9.63; N, 4.58; O,
10.46. Найдено (%): C, 66.63; H, 8.48; Co, 9.92; N, 4.75.
ИК (ваз. масло, ν, см-1): 1648 сл., 1549 ср., 1443 с., 1365 сл., 1350 сл.,
1341 с., 1317 сл., 1277 сл., 1238 сл., 1204 сл., 1181 сл., 1057 ср., 1028 сл., 998
ср., 966 ср., 955 с., 925 сл., 822 с., 784 ср., 722 сл., 673 сл., 654 с., 503 сл., 409
сл.
Синтез фенилгидразонов ароматических альдегидов
Общая методика [115]: Фенилгидразин (0.04 моль; 4.33 г; 3.9 мл)
растворили в 100 мл метанола и охладили смесь до 0 °C. При постоянном
перемешивании к реакционной смеси добавляли по каплям ароматический
альдегид (0.04 моль). При этом температура смеси не превышала 5 °C. После
добавления альдегида реакционную смесь перемешивали около часа при
температуре 0 °C. Далее выпавший осадок отфильтровывали и сушили в тяге.
Маточный раствор сутки выдерживали при температуре −18 °C. Вновь
выпавший осадок выделяли аналогично.
Фенилгидразон бензальдегида
Получен из 4.25 г (4.1 мл) бензальдегида в виде бледно-розового
мелкокристаллического порошка. Выход 84% (6.57 г).
Фенилгидразон 4-пиридинкарбальдегида
Получен из 4.28 г (3.8 мл) 4-пиридинкарбальдегида в виде желтого
мелкокристаллического порошка. Выход 93% (7.33 г).
135
Синтез формазановых лигандов
Общая методика [101-102]:
Предварительно был получен раствор
соли диазония. Для этого ароматический амин (5.08 ммоль) растворили в 2
мл концентрированной HCl и добавили 0.5 г льда. После этого смесь
диазотировали при температуре 0 - 5 оС прикапыванием раствора 0.35 г (5.08
ммоль) NaNO2 в 1.0 мл воды. Для поддержания необходимой температуры
использовали баню со смесью льда и поваренной соли.
К раствору фенилгидразона ароматического альдегида (5.08 ммоль) в 4
мл пиридина и 8 мл метанола добавили 1 мл уксусной кислоты и при
интенсивном
перемешивании
и
охлаждении
прикапывали
раствор
полученной соли диазония. При этом скорость прикапывания соблюдали
такой, чтобы температура не превышала 5 оС. В процессе взаимодействия
наблюдалось постоянное пенообразование. После прекращения добавления
соли диазония смесь перемешивали при 5 оС еще в течение 30 мин. Затем
непродолжительное время нагрели при 50-60 оС и охладили до комнатной
температуры. К смеси добавили 10 мл воды (в случае получения 3пиридилзамещенных формазанов при постоянном перемешивании довели рН
смеси до 9 прикапыванием 2 М раствора NaOH). При этом интенсивно
выпадает
осадок
в
виде
бордовой
кашицы.
Образовавшуюся
кристаллическую кашицу отфильтровывали и несколько раз промывали
дистиллированной
водой.
После
высушивания
в
вакууме
осадок
перекристаллизовывали.
1-(4-фторфенил)-3,5-дифенилформазан (25)
Получен из 0.996 г фенилгидразона бензальдегида и 0.56 г (0.49 мл) 4фторанилина в виде темно-красного аморфного порошка. Выход 1.261 г
(78%).
Вычислено для C19H15N4F (%): C, 71.68; H, 4.75; N, 17.60; F, 5.97.
Найдено (%): C, 71.53; H, 4.78; N, 17.75; F, 5.94.
136
ИК (ваз. масло, ν, см-1): 1597 с., 1589 с., 1579 сл., 1512 ср., 1493 с., 1445
ср., 1418 ср., 1360 сл., 1350 ср., 1310 сл., 1293 сл., 1284 сл., 1255 сл., 1228 с.,
1179 с., 1166 сл., 1160 сл., 1133 ср., 1091 с., 1074 сл., 1043 с., 1018 с., 997 сл.,
985 сл., 956 сл., 939 сл., 919 ср., 893 сл., 860 сл., 839 с., 829 сл., 806 сл., 767
ср., 754 ср., 736 сл., 690 с., 670 ср., 642 сл., 632 с., 614 сл., 602 сл., 589 сл., 573
ср., 546 сл., 539 сл., 521 сл., 511 ср., 505 ср., 476 сл., 460 сл.
Спектр 1H ЯМР (CDCl3, м. д.): 7.12–7.27 (м., 3H, Ph); 7.30–7.52 (м., 5H,
Ph); 7.53–7.64 (м., 2H, Ph); 7.73–7.87 (м., 2H, Ar); 8.08–8.20 (м., 2H, Ar); 15.33
(с., 1Н, NH).
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 490 (13000).
1-фенил-3-(4-пиридил)-5-(2,6-диметилфенил)формазан (29)
Получен из 1.002 г фенилгидразона 4-пиридинкарбальдегида и 0.616 г
(0.63 мл) 2,6-диметиланилина в виде темно-красного аморфного порошка.
Выход 1.054 г (63%).
Вычислено для C20H19N5 (%): C, 72.93; H, 5.81; N, 21.26. Найдено (%): C,
73.05; H, 5.91; N, 21.04.
ИК (ваз. масло, ν, см-1): 1594 с., 1575 ср., 1551 с., 1534 сл., 1504 ср., 1493
ср., 1411 ср., 1364 сл., 1347 сл., 1335 сл., 1314 сл., 1303 сл., 1290 сл., 1273 ср.,
1264 ср., 1225 ср., 1209 сл., 1193 сл., 1180 сл., 1163 сл., 1145 сл., 1105 сл.,
1083 сл., 1074 ср., 1063 ср., 1058 сл., 1030 сл., 991 ср., 963 сл., 914 сл., 903 сл.,
893 сл., 880 сл., 831 с., 818 сл., 795 сл., 768 с., 758 сл., 742 ср., 716 сл., 692 сл.,
685 ср., 669 ср., 647 сл., 638 с., 614 сл., 579 сл., 532 сл., 521 сл., 507 ср., 490
сл., 482 сл., 465 сл.
Спектр 1H ЯМР (CDCl3, м. д.):2.59 (с., 6H, CH3); 7.14–7.22 (м., 3H, Ar);
7.33 (т., 3JH–H = 7.4 Гц, 1H, Ph); 7.49 (т., 3JH–H = 7.3 Гц, 2H, Ph); 7.71 (д., 3JH–H =
8.0 Гц, 2H, Ph); 7.96 (д. м., 3JH–H = 6.2 Гц, 2H, py); 8.64 (д. м., 3JH–H = 6.2 Гц,
2H, py); 15.54 (с., 1H, NH).
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 477 (21300).
137
(3,6-Cat)(4-Py-(Me2Ph)-FormH)SbPh3 (30)
К
раствору
3,6-ди-трет-бутилкатехолата
трифенилсурьмы(V),
полученному по методике [116], (0.42 ммоль) в 15 мл толуола прилили
раствор формазана 29 (0.42 ммоль) в 10 мл толуола. Полученную
реакционную смесь перемешивали около часа. После упаривания до момента
начала кристаллообразования раствор выставляли на холод (~0°С) на сутки.
Выпавший
ярко-красный
кристаллический
осадок
отфильтровывали,
промывали гексаном и сушили на воздухе. Выход 0.36 г (86%).
Вычислено для C52H54N5O2Sb·СН3С6Н5 (%):С, 71.23; Н, 6.28; N, 7.04; Sb,
12.24. Найдено (%): С, 71.08; Н, 6.34; N, 6.85; Sb, 12.03.
ИК (ваз. масло, ν, см-1): 1700 сл., 1622 сл., 1597 сл., 1537 сл., 1497 ср.,
1430 с., 1403 с., 1351 сл., 1307 сл., 1282 сл., 1261 сл., 1242 ср., 1216 сл., 1200
сл., 1182 сл., 1146 сл., 1069 ср., 1024 сл., 1008 ср., 997 сл., 976 с., 939 ср., 924
сл., 841 сл., 810 сл., 793 сл., 753 ср., 729 с., 694 с., 681 ср., 659 сл., 648 ср., 461
с.
Синтез гетеролигандных комплексов кобальта и марганца на основе 3,6ди-трет-бутил-о-бензохинона и формазанов
Co(3,6-SQ)2(Ph-Form) (31)
Метод 1. К навеске 0.100 г (0.29 ммоль) карбонила кобальта добавляли
навеску 0.180 г (0.60 ммоль) 1,3,5-трифенилформазана. Затем в эту ампулу
приливали раствор 0.257 г (1.17 ммоль) 3,6-ди-трет-бутил-о-бензохинона в
толуоле. Содержимое ампулы перемешивали в течение часа, периодически
удаляя из нее выделяющийся в ходе реакции оксид углерода(II). Цвет
реакционной смеси при этом изменился с бордового до темно-синего. После
окончания реакции упаривали часть растворителя и добавляли гексан, затем
раствор
сутки
выдерживали
при
температуре
-18ºС.
Выпавший
мелкокристаллический порошок черного цвета отфильтровывали и сушили в
вакууме. Выход 0.384 г (83 %).
138
Метод 2. К раствору 0.150 г (0.21 ммоль) трис(3,6-ди-трет-бутил-обензосемихинон)кобальта в ~ 20 мл толуола приливали раствор 0.063 г (0.21
ммоль) 1,3,5-трифенилформазана в ~ 15 мл толуола. После смешивания
ампулу с полученным раствором нагревали несколько часов на водяной бане,
затем упаривали часть растворителя и добавляли гексан. Полученный
раствор до момента начала кристаллообразования выдерживали при
температуре
~0ºС.
Выпавший
черный
мелкокристаллический
осадок
отфильтровывали и сушили в вакууме. Выход 0.082 г (49 %).
Вычислено для C47H55CoN4O4 (%): C, 70.66; H, 6.94; Co, 7.38; N, 7.01; O,
8.01. Найдено (%): C, 70.80; H, 7.05; Co, 7.24; N, 6.94.
ИК (ваз. масло, ν, см-1): 1601 ср., 1593 ср., 1552 ср., 1498 сл., 1485 ср.,
1426 с., 1419 с., 1357 ср., 1344 ср., 1331 ср., 1307 с., 1280 с., 1248 сл., 1198 с.,
1167 сл., 1154 сл., 1082 сл., 1072 сл., 1026 ср., 993 ср., 976 ср., 957 ср., 910 ср.,
893 сл., 831 ср., 809 сл., 766 ср., 756 с., 692 с., 681 ср., 665 ср., 652 ср., 620 сл.,
565 сл., 542 ср., 523 сл., 506 сл., 488 ср., 482 ср., 452 ср.
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 593 (11200), 750 (7700), 955 (3000).
Co(3,6-SQ)2(F-Form) (32)
Комплекс был получен при взаимодействии 0.100 г (0.29 ммоль)
карбонила кобальта с 0.257 г (1.17 ммоль) 3,6-ди-трет-бутил-о-бензохинона и
0.186 г (0.58 ммоль) 1-(4-фторфенил)-3,5-дифенилформазана по методу 1
аналогичному для комплекса 31. Комплекс выделен из смеси толуол/гексан в
виде черного мелкокристаллического осадка. Выход 0.396 г (84%).
Вычислено для C47H54CoN4O4F (%): C, 69.10; H, 6.66; Co, 7.21; N, 6.86;
O, 7.83; F, 2.33. Найдено (%): C, 68.84; H, 6.32; Co, 6.94; N, 6.77; F, 2.45.
ИК (ваз. масло, ν, см-1):1680 ср., 1657 с., 1599 ср., 1552 ср., 1500 с., 1481
сл., 1427 с., 1416 с., 1358 сл., 1344 сл., 1331 сл., 1308 ср., 1281 с., 1232 с., 1198
с., 1151 ср., 1093 сл., 1072 сл., 1026 ср., 993 ср., 976 ср., 957 ср., 939 сл., 924
сл., 899 сл., 831 с., 808 сл., 786 сл., 766 сл., 758 с., 692 с., 679 ср., 652 с., 598
сл., 563 ср., 528 с., 505 сл., 482 сл., 460 сл.
139
Co(3,6-SQ)2(I-Form) (33)
Комплекс был получен при взаимодействии 0.095 г (0.28 ммоль)
карбонила кобальта с 0.245 г (1.12 ммоль) 3,6-ди-трет-бутил-о-бензохинона и
0.337 г (0.56 ммоль) 1-(4-иодфенил)-3,5-дифенилформазана по методу 1
аналогичному для комплекса 31. Комплекс выделен из диэтилового эфира в
виде черного мелкокристаллического осадка. Выход 0.431 г (83%).
Вычислено для C47H54CoN4O4I (%): C, 61.04; H, 5.89; Co, 6.37; N, 6.06; O,
6.92; I, 13.72. Найдено (%): C 61.14; H 5.98; Co 6.13; N 5.77; I 14.05.
ИК (ваз. масло, ν, см-1): 1667 сл., 1599 сл., 1552 с., 1428 ср., 1307 сл.,
1277 с., 1207 с., 1111 сл., 1068 сл., 1035 сл., 1016 ср., 989 сл., 974 с., 918 сл.,
825 с., 764 с., 687 с., 648 сл., 575 сл., 552 сл., 542 сл., 495 ср.
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 600 (6100), 751 (5800), 911 (1700),
951 (1400).
Co(3,6-SQ)(3,6-Cat)(4-Py-FormH) (34)
Комплекс был получен при взаимодействии 0.150 г (0.21 ммоль)
трис(3,6-ди-трет-бутил-о-бензосемихинон)кобальта с 0.063 г (0.21 ммоль) 3(4-пиридил)-1,5-дифенилформазана
по
методу
2
аналогичному
для
комплекса 31. Комплекс выделен из диэтилового эфира в виде аморфного
порошка темно-красного цвета. Выход 0.094 г (56%).
Вычислено для C46H55CoN5O4 (%): C, 68.98; H, 6.92; Co, 7.36; N, 8.74; O,
7.99. Найдено (%): C, 68.55; H, 6.69; Co, 7.53; N, 8.97.
ИК (ваз. масло, ν, см-1): 1612 с, 1599 сл, 1549 ср, 1495 ср, 1476 сл, 1420
ср, 1353 ср, 1315 сл, 1281 ср, 1270 ср, 1240 ср, 1213 сл, 1202 ср, 1180 сл, 1164
ср, 1157 ср, 1092 сл, 1074 сл, 1065 сл, 1045 сл, 1028 ср, 991 сл, 972 ср, 952 ср,
822 сл, 802 ср, 763 ср, 748 ср, 737 сл, 700 ср, 684 ср, 648 сл, 635 ср, 608 ср,
591 сл, 559 ср, 546 сл, 488 ср, 472 ср, 450 ср.
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 479(10000), 780(4600).
140
Co(3,6-SQ)(3,6-Cat)(4-Py-NO2-FormH) (35)
Комплекс был получен при взаимодействии 0.095 г (0.28 ммоль)
карбонила кобальта с 0.245 г (1.12 ммоль) 3,6-ди-трет-бутил-о-бензохинона и
0.192 г (0.56 ммоль) 5-(4-нитрофенил)-3-(4-пиридил)-1-фенилформазана по
методу 1 аналогичному для комплекса 31. Комплекс выделен из смеси
толуол/гексан в виде коричневого мелкокристаллического осадка. Выход
0.408 г (86%).
Вычислено для C46H54CoN6O6 (%): C, 65.31; H, 6.43; Co, 6.97; N, 9.94; O,
11.35. Найдено (%): C, 65.45; H, 6.59; Co, 6.64; N, 8.97.
ИК (ваз. масло, ν, см-1): 1602 с., 1559 ср., 1537 ср., 1522 ср., 1492 ср.,
1422 сл., 1349 ср., 1339 сл., 1321 ср., 1300 ср., 1289 ср., 1272 с., 1260 с., 1211
сл., 1188 сл., 1156 сл., 1106 ср., 1063 сл., 1031 сл., 974 ср., 951 ср., 861 сл., 835
сл., 802 сл., 772 сл., 753 с., 731 с., 706 ср., 693 с., 609 ср., 550 сл., 488 ср.
Co(3,6-SQ)(3,6-Cat)(4-Py-(Me2Ph)-FormH) (36)
Комплекс был получен при взаимодействии 0.086 г (0.25 ммоль)
карбонила кобальта с 0.220 г (1 ммоль) 3,6-ди-трет-бутил-о-бензохинона и
0.165 г (0.50 ммоль) 5-(2,6-диметилфенил)-3-(4-пиридил)-1-фенилформазана
по методу 1 аналогичному для комплекса 31. Комплекс выделен в виде
аморфного порошка темно-красного цвета. Выход 0.366 г (88 %).
Вычислено для C48H59CoN5O4 (%): C, 69.55; H, 7.71; Co, 7.11; N, 8.45; O,
7.72. Найдено (%): C, 69.66; H, 7.82; Co, 6.97; N, 8.27.
ИК (ваз. масло, ν, см-1): 1614 с., 1549 с., 1500 сл., 1481 сл., 1421 ср., 1408
сл., 1351 сл., 1315 ср., 1288 сл., 1270 с., 1236 с., 1207 сл., 1198 сл., 1155 с.,
1096 ср., 1066 сл., 1056 сл., 1026 ср., 933 сл., 974 с., 951 с., 928 сл., 847 сл.,
822 сл., 802 сл., 769 ср., 739 сл., 685 с., 636 с., 611 с., 553 с., 537 сл., 488 с.,
476 с., 422 с.
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 473 (27500), 740 (2000).
141
Co(3,6-SQ)(Ph-Form) (37)
К навеске 0.145 г (0.42 ммоль) карбонила кобальта добавляли навеску
0.252 г (0.84 ммоль) 1,3,5-трифенилформазана. Затем в эту ампулу приливали
раствор 0.185 г (0.84 ммоль) 3,6-ди-трет-бутил-о-бензохинона в толуоле.
Содержимое
ампулы
перемешивали
в
течение
нескольких
часов,
периодически удаляя из нее выделяющийся в ходе реакции оксид
углерода(II). Цвет реакционной смеси при этом изменился с бордового до
коричневого. После окончания реакции упаривали часть растворителя, затем
раствор
сутки
выдерживали
при
температуре
~
0ºС.
Выпавший
мелкокристаллический осадок коричневого цвета отфильтровывали и
сушили в вакууме. Выход 0.371 г (76 %).
Вычислено для C33H35CoN4O2 (%): C, 68.50; H, 6.10; Co, 10.19; N, 9.68; O,
5.53. Найдено (%): C, 68.23; H, 6.07; Co, 9.94; N, 9.78.
ИК (ваз. масло, ν, см-1): 1587 сл., 1552 ср., 1480 ср., 1341 сл., 1278 сл.,
1218 ср., 1201 с., 1111 сл, 1081 сл., 1028 ср., 980 ср., 960 сл., 906 сл., 832 сл.,
759 с., 721 сл., 686 с., 673 ср., 651 сл., 638 сл., 584 сл., 569 сл., 534 сл., 506 сл.,
488 сл.
Co(3,6-SQ)(Ph-Form)2 (38)
К раствору 0.050 г (0.076 ммоль) Co(Ph-Form)2 в ~20 мл толуола прилили
раствор 0.063 г (0.076 ммоль) 3,6-ди-трет-бутил-орто-бензохинона в ~20 мл
толуола. После смешивания ампулу с полученным раствором нагревали
несколько часов на водяной бане. Комплекс 38 был охарактеризован in situ в
растворе с помощью ЭПР-спектроскопии.
Mn(3,6-SQ)2(Ph-Form) (39)
К навеске 0.045 г (0.115 ммоль) карбонила марганца прилили раствор
0.069 г (0.230 ммоль) 1,3,5-трифенилформазана в ~20 мл толуола. Затем к
этой смеси добавили раствор 0.102 г (0.460 ммоль) 3,6-ди-трет-бутил-обензохинона в ~10 мл толуола. Полученный раствор несколько суток
142
облучали видимым светом, периодически перемешивая реакционную смесь и
удаляя из нее образующийся монооксид углерода. Образовавшийся черный
мелкокристаллический осадок отфильтровывали и сушили в вакууме.
Маточный раствор упаривали и выдерживали при −18 °C. Вновь выпавший
осадок выделяли аналогично. Выход 0.138 г (76%).
Вычислено для C47H55MnN4O4 (%): C, 71.02; H, 6.97; Mn, 6.91; N, 7.05; O,
8.05. Найдено (%): C, 71.09; H, 6.83; Mn, 6.45; N, 7.34.
ИК (ваз. масло, ν, см-1): 1678 сл., 1657 ср., 1605 ср., 1550 сл., 1526 ср.,
1477 ср., 1440 c., 1426 ср., 1357 ср., 1309 сл., 1291 сл., 1279 сл., 1254 ср., 1238
с., 1233 с., 1224 ср., 1202 ср., 1180 сл., 1154 сл., 1145 с., 1079 сл., 1075 сл.,
1026 сл., 997 сл., 972 с., 951 сл., 932 ср., 918 с., 843 ср., 826 сл., 809 ср., 786
ср., 762 ср., 727 с., 701 сл., 693 с., 654 ср., 623 сл., 607 сл., 588 ср., 573 ср., 557
сл., 536 сл., 514 ср., 506 ср., 500 ср., 483 сл., 465 сл., 453 сл.
Mn(3,6-SQ)2(4-Py-FormH) (40)
Комплекс был получен при взаимодействии 0.130 г (0.33 ммоль)
карбонила марганца с 0.294 г (1.34 ммоль) 3,6-ди-трет-бутил-о-бензохинона и
0.202 г (0.67 ммоль) 3-(4-пиридил)-1,5-дифенилформазана по методу
аналогичному для комплекса 39. Комплекс выделен в виде аморфного
порошка темно-красного цвета. Выход 0.448 г (84 %).
Вычислено для C46H55MnN5O4 (%): C, 69.33; H, 6.96; Mn, 6.89; N, 8.79; O,
8.03. Найдено (%): C, 69.47; H, 6.83; Mn, 6.42; N, 8.51.
ИК (ваз. масло, ν, см-1): 1611 с., 1599 ср., 1584 сл., 1549 сл., 1495 с., 1481
сл., 1420 с., 1352 с., 1328 сл., 1316 ср., 1281 с., 1268 с., 1239 сл., 1233 с., 1211
сл., 1201 с., 1191 сл., 1165 ср., 1145 сл., 1098 сл., 1073 ср., 1065 с., 1045 ср.,
1026 с., 1001 сл., 990 ср., 976 с., 953 сл., 938 ср., 924 ср., 915 сл., 893 ср., 856
ср., 840 с., 819 сл., 810 сл., 893 с., 764 с., 748 с., 712 сл., 700 с., 683 ср., 652 сл.,
644 ср., 633 ср., 615 сл., 592 с., 549 сл., 523 сл., 508 с., 476 ср., 464 сл.
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 475 (25700), 850 (1300).
143
.
Синтез 6-(4-пиридил)-2,4-дифенилвердазильного радикала (Verd )
[102]
К
хорошо
перемешиваемому
раствору
3-(4-пиридил)-1,5-
дифенилформазана (0.33 ммоль) в 5.23 мл ДМФА при 20 C медленно
добавляли 0.50 мл 37% водного раствора формалина. Раствор перемешивали
30 мин в открытом сосуде, после чего к нему добавили 0.75 мл 2 М раствора
NaOH. Реакционную смесь перемешивали в течение 4 часов с хорошим
доступом воздуха (O2). Цвет раствора при этом изменялся с пурпурного на
ярко изумрудный. Смесь вылили в избыточное количество воды и
отфильтровали ярко-зеленый осадок, который затем сушили в вакууме.
.
Co(3,6-SQ)(3,6-Cat)Verd (41)
К
раствору
0.100
г
(0.139
ммоль)
трис(3,6-ди-трет-бутил-о-
бензосемихинон)кобальта в эфире при перемешивании прилили раствор
0.050 г (0.159 ммоль) 6-(4-пиридил)-2,4-дифенилвердазила в толуоле.
Образующийся черный осадок отфильтровывали и сушили в вакууме. Выход
0.091 г (81 %).
Вычислено для C47H56CoN5O4 (%): C, 69.36; H, 6.93; Co, 7.24; N, 8.60; O,
7.86. Найдено (%): C, 69.75; H, 6.76; Co, 7.40; N, 8.35.
ИК (ваз. масло, ν, см-1): 1624 ср., 1614 ср., 1599 сл., 1546 сл., 1491 ср.,
1340 сл., 1276 сл., 1203 сл., 1151 ср., 1121 сл., 1096 сл., 1075 сл., 1061 ср.,
1027 ср., 990 сл., 972 ср., 952 ср., 799 сл., 747 с., 729 с., 686 ср., 646 ср., 618 с.,
605 с., 554 ср., 485 с.
УФ-спектр, толуол λ (ε, л.см-1.моль-1): 447 (3100), 722 (2100).
.
Mn(3,6-SQ)2Verd (42)
К навеске 0.050 г (0.128 ммоль) карбонила марганца прилили раствор
0.080 г (0.255 ммоль) 6-(4-пиридил)-2,4-дифенилвердазила в толуоле. Затем к
этой смеси добавили раствор 0.112 г (0.51 ммоль) 3,6-ди-трет-бутил-о144
бензохинона толуоле. Полученный раствор несколько суток облучали
видимым светом, периодически перемешивая реакционную смесь и удаляя из
нее
образующийся
монооксид
углерода.
Образовавшийся
черный
мелкокристаллический осадок отфильтровывали и сушили в вакууме. Выход
0.128 г (62 %).
Вычислено для C47H56MnN5O4 (%): C, 69.70; H, 6.97; Mn, 6.78; N, 8.65; O,
7.90. Найдено (%): C, 69.68; H, 7.14; Mn, 6.62; N, 8.51.
ИК (ваз. масло, ν, см-1): 1624 ср., 1614 ср., 1600 сл., 1591 сл., 1569 сл.,
1528 сл., 1504 ср., 1494 ср., 1483 ср., 1425 сл., 1355 сл., 1340 ср., 1280 сл.,
1258 сл., 1247 сл., 1230 ср., 1204 ср., 1147 сл., 1121 сл., 1075 сл., 1060 сл.,
1031 сл., 976 с., 937 сл., 921 сл., 842 сл., 791 сл., 752 ср., 719 с., 686 ср., 643
сл., 610 сл.
145
Выводы
1.
Для
широкого
ряда
шестикоординационных
вновь
синтезированных
пяти-
и
бис-3,6-ди-трет-бутил-о-бенхосемихиноновых
комплексов кобальта, марганца и железа вида M(3,6-SQ)2L, где L –
нейтральный донорный лиганд, исследованы магнитные свойства и
проведена количественная оценка энергии обмена между парамагнитными
центрами. Показано, что характер температурной зависимости эффективного
магнитного момента значительно меняется в зависимости от строения
дополнительного лиганда.
2. Впервые выделен в индивидуальном виде и охарактеризован с
помощью
метода
РСА
плоско-квадратный
моно-о-семихинон-
формазанатный комплекс кобальта(II) вида Co(3,6-SQ)(Ph-Form).
3. Разработан удобный синтетический подход для получения смешаннолигандных комплексов переходных металлов первого d-ряда на основе 3,6ди-трет-бутил-о-бензохинона и формазанов, включающий взаимодействие
нейтральной формы формазанового лиганда с карбонилом металла в
присутствии о-хинона.
4. Установлено, что 3-фенилзамещенные 1,5-диарилформазаны образуют
с металлом хелатный формазанатный цикл, в то время как 3-(4-пиридил)замещенные формазановые лиганды координируются в нейтральной форме
через атом азота 4-пиридильной группы, при этом происходит образование
соответственно
бис-о-семихиноновых
или
семихинон-катехолатных
комплексов.
5. Впервые получены смешаннолигандные комплексы кобальта и
марганца, одновременно содержащие в своем составе два типа радикальных
лигандов: семихиноновый и вердазильный.
146
Список литературы
1. Rohrscheid, F. Potential electron transfer complexes of the [M-O,] type:
synthesis and properties of complexes derived from pyrocatechol and
tetrachloropyrocatechol / F. Rohrscheid, A.L. Balch, R.H. Holm // Inorg.
Chem. - 1966. - V.5. - N 9. - P. 1542-1551.
2. Floriani, C. 9,10-Phenanthrenequinone binary complexes of iron, cobalt, and
nickel / C. Floriani, R. Henzi, F. Calderazzo // J.C.S. Dalton. - 1972. - V.23. P. 2640-2642.
3. Pierpont, C.G. Coordination properties of o-benzoquinones. Structure and
bonding in tris(tetrachloro-1,2-benzoquinone)chromium(0) / C.G. Pierpont,
H.H. Downs // J. Am. Chem. Soc. - 1976. – V.98. - P. 4834-4838.
4. Pierpont, C.G. Bridging and terminal o-benzoquinone coordination. The
crystal
and
molecular
structure
of
hexakis(tetrachloro-1,2-
benzoquinone)dimolybdenurn / C.G. Pierpont, H.H. Downs //J. Am. Chem.
Soc. - 1975. – V.97. - P. 2123-2127.
5. Buchanan, R.M. Intramolecular antiferromagnetic exchange in tris(osemiquinone) complexes of vanadium(III), chromium(III), and iron(III) / R.M.
Buchanan, H.H. Downs, W.B. Shorthill, C.G. Pierpont // J. Am. Chem. Soc. 1978. - V.100. - N 13. - P. 4318-4320.
6. Лобанов, А.В. Комплексы переходных металлов с о-семихиноновым
лигандом / А.В. Лобанов, Г.А. Абакумов, Г.А. Разуваев // Докл. АН
СССР. - 1977. - 235. - № 4. - C. 824-827.
7. Lynch, M. W. Intramolecular two-electron transfer between manganese(II)
and semiquinone ligands. Synthesis and characterization of manganese 3,5di-tert-butylquinone complexes and their relationship to the photosynthetic
water oxidation system / M. W. Lynch, D.N. Hendrickson, B.J. Fitzgerald // J.
Am. Chem. Soc. - 1984. - V. 106. - N 7. - P. 2041-2049.
8. Jung, O.-S. Bistability and molecular switching for semiquinone and catechol
complexes of cobalt. Studies on redox isomerism for the bis(pyridine) ether
147
series Co(py2X)(3,6-DBQ)2, X = O, S, Se, and Te / O.-S. Jung, D.H. Jo, Y.-A.
Lee, B.J. Conklin, C.G. Pierpont // Inorg. Chem. - 1997. – V. 36. - P. 19-24.
9. Абакумов, Г.А. Синтез, кристаллическая структура и поляризованные
электронные спектры поглощения кристаллов μ-4,4’-дипиридил-бис(3,5ди-трет.-бутилбензосемихиноно) меди (II) / Г.А. Абакумов, А.В. Лобанов,
В.К. Черкасов, Р.И. Бочкова, Л.Н. Захаров, Ю.Н. Сафьянов, Э.А. Кузьмин
// Докл. АН СССР. - 1985. - 285. - № 4. - C. 906-911.
10. Мураев, В.А. Орто-семихиноновые комплексы одновалентной меди и
серебра / В.А. Мураев, В.К. Черкасов, Г.А. Абакумов, Г.А. Разуваев //
Докл. АН СССР. - 1977. - 236. - № 3. - C. 620-623.
11. Myраев, В.A. Спектры ЭПР о-семихинолятов одновалентного таллия /
В.A. Myраев, Г.А. Абакумов, Г.А. Разуваев // Докл. АН СССР. - 1974. 217. - №5. - C. 1083-1086.
12. Разуваев, Г.А. Нейтральные трис-о-хиноновые комплексы переходных
металлов или лантанидов и способ их получения / Г.А. Разуваев, Г.А.
Абакумов, А.В. Лобанов // Авт. свид. №527434. - 1975.
13. Abakumov, G.A. The synthesis and properties of o-semiquinolate copper
complexes / G.A. Abakumov, A.V. Lobanov, V.K. Cherkasov, G.A. Razuvaev
// Inorg. Chim. Acta. - 1981. – V. 49. - P. 135-138.
14. Razuvaev, G.A. ESR investigation of copper(I) complexes with osemiquinolate ligands / G.A. Razuvaev, V. K. Cherkasov, G. A. Abakumov //
J. Organometall. Chem. - 1978. – V. 160. - N 1. - P. 361-371.
15. Разуваев, Г.А. Пирокатехинолятные и семихинолятные комплексы
переходных металлов / Г.А. Разуваев, К.Г. Шальнова, Л.Г. Абакумова,
Г.А. Абакумов // Изв. АН СССР, Сер. Хим. - 1977. - № 7. - C. 1642-1645.
16. Nevodchikov, V.I. ESR investigation of the substitution reactions in
rhodium(I) complexes with spin-labeled ligands / V.I Nevodchikov, G.A.
Abakumov, V.K. Cherkasov, G.A. Razuvaev //J.Organometall.Chem. - 1981. –
V. 214. - P. 119-124.
148
17. Бубнов, М.П. Синтез. Физико-химические свойства полисемихиноновых
комплексов кобальта и никеля. Обратимый внутримолекулярный перенос
электрона в бис-семихиноновых комплексах кобальта: дис. … канд. хим.
наук: 02.00.08 / Бубнов Михаил Павлович. – Нижний Новгород, 1993. с.74.
18. Buchanan, R.M. Tautomeric catecholate-semiquinone interconversion via
metal-ligand electron transfer. Structural, spectral, and magnetic
properties
of
(3,5-di-tert-butylcatecholato)-(3,5-di-tert-
butylsemiquinone)(bipyridyl)cobalt(III), a complex containing mixed-
valence organic ligands / R.M. Buchanan, C.G. Pierpont // J. Am. Chem. Soc.
- 1980. – V. 102. - N 15. - P. 4951-4957.
19. Абакумов, Г.А. Редокс-изомерия парамагнитных о-семихиноновых
комплексов кобальта в твердой фазе. Исследование
Co(SQ)2Dipy методами РСА, магнетохимии, ЭПР и
комплексов
сканирующей
калориметрии / Г.А. Абакумов, В.К. Черкасов, М.П. Бубнов, О.Г. Эллерт,
Ж.В. Доброхотова, Л.Н. Захаров, Ю.Т. Стручков // Докл. РАН. - 1993. 328. - № 3. - C. 332-335.
20. Adams,
D.M.
Bistability
in
the
[CoII(semiquinonate)2]
to
[CoIII(catecholate)(semiquinonate)] valence-tautomeric conversion / D.M.
Adams, A. Dei, A. L. Rheingold, D. N. Hendrickson // J. Am. Chem. Soc. 1993. – V. 115. - P. 8221-8229.
21. Бубнов, М.П. Исследование (1,10-фенантролин)(бис-(3,6-ди-трет-бутилo-бензосемихинон))кобальта методами РСА, ИК- и ЭПР-спектроскопии,
магнетохимии и точной калориметрии / М.П. Бубнов, Н.А. Скородумова,
А.С. Богомяков, Г.В. Романенко, А.В. Арапова, К.А. Кожанов, Н.Н.
Смирнова, Г.А. Абакумов, В.К. Черкасов // Изв. АН. Сер. хим. - 2011. № 3. - C. 440-446.
22. Jung, O.-S. Bistability and low-energy electron transfer in cobalt complexes
containing catecholate and semiquinone ligands / O.-S. Jung, C.G. Pierpont //
Inorg. Chem. - 1994. – V. 33. - P. 2227-2235.
149
23. Pierpont, C.G. Transition metal complexes of o-benzoquinone, o-semiquinone,
and catecholate ligands / C.G. Pierpont // Coord. Chem. Rev. - 1981. – V. 38. P. 45-87.
24. Jung, O.-S. Chelate-ring-dependent shifts in redox isomerism for the
Co(Me2N(CH2)nNMe2)(3,6-DBQ)2 (n = 1-3) series, where 3,6-DBQ is the
semiquinonate or catecholate ligand derived from 3,6-di-tert-butyl-1,2benzoquinone / O.-S. Jung, D.H. Jo, Y.-A. Lee, S.Y. Sohn, C.G. Pierpont //
Inorg. Chem. - 1998. – V. 37. - P. 5875-5880.
25. Jung, O.-S. Ancillary ligand dependent shifts in charge distribution for cobaltquinone complexes / O.-S. Jung, D.H. Jo, Y.-A. Lee, S.Y. Sohn, C.G. Pierpont
// Angew. Chem. Int. Ed. - 1996. – V. 35. - P. 1694-1695.
26. Sato, O. Photo-induced reverse valence tautomerism in a metastable Co
compound / O. Sato, S. Hayami, Z. Gu, K. Takahashi, R. Nakajima, A.
Fujishima // Chem. Phys. Lett. - 2002. – V. 355. - P. 169-174.
27. Kiriya, D. Molecule-based valence tautomeric bistability synchronized with a
macroscopic crystal-melt phase transition / D. Kiriya, H.-C. Chang, S.
Kitagawa // J. Am. Chem. Soc. - 2008. – V. 130. - P. 5515-5522.
28. Kiriya, D. Polymorph-dependent molecular valence tautomerism synchronized
with crystal-melt phase transitions / D. Kiriya, H.-C. Chang, K. Nakamura, D.
Tanaka, K. Yoneda, S. Kitagawa // Chem. Mater. - 2009. – V. 21. - P. 19801988.
29. Schmidt, R.D. Magnetic bistability in a cobalt bis(dioxolene) complex: longlived photoinduced valence tautomerism / R.D. Schmidt, D.A. Shultz, J.D.
Martin // Inorg. Chem. - 2010. – V. 49. - P. 3162-3168.
30. Schmidt, R.D. Goldilocks effect in magnetic bistability: remote substituent
modulation and lattice control of photoinduced valence tautomerism and lightinduced thermal hysteresis / R.D. Schmidt, D.A. Shultz, J.D. Martin, P.D.
Boyle // J. Am. Chem. Soc. - 2010. – V. 132. - P. 6261-6273.
31. Mulyana ,Y. Solvation effects on the valence tautomeric transition of a cobalt
complex in the solid state / Y. Mulyana, G. Poneti, B. Moubaraki, K.S. Murray,
150
B.F. Abrahams, L. Sorace, C. Boskovic // Dalton Trans. - 2010. – V. 39. - P.
4757-4767.
32. Hui, L. Dinuclear valence tautomeric 1,2-semiquinonato/catecholatocobalt
complexes containing 1,1,4,7,10,10-hexamethyltriethylenetetramine / L. Hui,
M.N. Young, C. In Sung, K. Soon Sik, Y.-A. Lee, O.-S. Jung // Bull. Chem.
Soc. Jpn. - 2007.- V. 80. - P. 916-921.
33. Imaz, I. Valence-Tautomeric Metal–Organic Nanoparticles / I. Imaz, D.
Maspoch, C. Rodriguez-Blanco, J. Manuel Perez-Falcon, J. Campo, D. RuizMolina // Angew. Chem. Int. Ed. - 2008. – V. 47. - P. 1857-1860.
34. Jung, O.-S. Photomechanical polymers. Synthesis and characterization of a
polymeric pyrazine-bridged cobalt semiquinonate-catecholate complex / O.-S.
Jung, C.G. Pierpont // J. Am. Chem. Soc. - 1994. – V. 116. - P. 2229-2230.
35. Li, B. Thermally Induced and Photoinduced Valence Tautomerism in a TwoDimensional Coordination Polymer / B. Li, L.-Q. Chen, R.-J. Wei, J. Tao, R.B. Huang, L.-S. Zheng, Z. Zheng // Inorg. Chem. - 2011. – V. 50. - P. 424-426.
36. Lunch, M.W. Ligand-induced valence tautomerism in manganese-quinone
complexes / M.W. Lunch, D.N. Hendrickson, B.J. Fitzgerald, C.G. Pierpont //
J. Am. Chem. Soc. - 1981. – V. 103. - P. 3961-3963.
37. Attia, A. S. Valence tautomerism for quinone complexes of manganese:
members of the MnIV(N-N)(Cat)2-MnIII(N-N)(SQ)(Cat)-MnII(N-N)(SQ)2 series
/ A. S. Attia, C.G. Pierpont // Inorg. Chem. - 1995. – V. 34. - P. 1172-1179.
38. Attia, A.S. Valence tautomerism for catechol/semiquinone complexes of the
trans-M(Bupy)2(3,6-DBQ)2 (M = Mn, Fe, Co) series / A.S. Attia, O.-S. Jung,
C.G. Pierpont // Inorg. Chim. Acta. - 1994. – V. 226. - P.91-98.
39. Attia, A.S. Valence tautomerism within a linear polymer consisting of
pyrazine-bridged manganese-quinone subunits. Synthesis and characterization
of [MnIII(μ-pyz)(3,6-DBSQ)(3,6-DBCat)]n / A.S. Attia, C.G. Pierpont // Inorg.
Chem. - 1997. – V. 36. - P.6184-6187.
40. Attia, A. S. New semiquinone/catecholate complexes that exhibit valence
tautomerism. Synthesis and characterization of Mn III(thf)2(3,6-DBSQ)(3,6151
DBCat) and observations on the MnIV(3,6-DBSQ)2(3,6-DBCat)/MnIII(3,6DBSQ)3 equilibrium in the solid state / A.S. Attia, C.G. Pierpont // Inorg.
Chem. - 1998. – V. 37. - P. 3051-3056.
41. Kiriya, D. Bimodal three-membered valence tautomerism of an alkyl chainfunctionalized manganese dioxolene complex / D. Kiriya, K. Nakamura, H.-C.
Chang, S. Kitagawa // Chem. Commun. - 2009. - P. 4085-4087.
42. Shaikh, N. Syntheses, crystal structures, and spectroscopic and magnetic
properties
.
[Mn2III(H2L1)(Cl4Cat)4 2H2O]∞
of
.
.
[Mn2III(H2L2)(Cl4Cat)4 2CH3CN 2H2O]
∞:
temperature-dependent
and
valence
tautomerism in solution / N. Shaikh, S. Goswami, A. Panja, H.-L. Sun, F. Pan,
S. Gao, P. Banerjee // Inorg. Chem. - 2005. – V. 44. - P. 9714-9722.
43. Goswami, S. Ligand-to-ligand electron transfer and temperature induced
valence tautomerism in o-dioxolene chelated manganese complexes / S.
Goswami, A. Panja, R.J. Butcher, N. Shaikh, P. Banerjee // Inorg. Chim. Acta.2011. – V. 370. - P. 311-321.
44. Lynch, M.W. Mixed-valence semiquinone-catecholate-iron complexes /
M.W. Lynch, M. Valentine, D.N. Hendrickson // J. Am. Chem. Soc. - 1982. V. 104. - P. 6982-6989.
45. Zirong, D. Studies on bis(catecholato)iron(III) complexes. Structure and
-
bonding in members of the Fe(bpy)(C14SQ)(Cl4Cat)/Fe(bpy)(C14Cat)2 redox
couple / D. Zirong, S. Bhattacharya, J.K. McCusker, P.M. Hagen, D.N.
Hendrickson, C.G. Pierpont // Inorg. Chem. - 1992. – V. 31. - P.870-877.
46. Cohn, M.J. Valence localization in iron complexes with o-quinone-derived
ligands studied by high magnetic field Mossbauer spectroscopy / M.J. Cohn,
C.-L. Xie, J.-P.M. Tuchagues, C.G. Pierpont, D.N. Hendrickson // Inorg.
Chem. - 1992. – V. 31. - P.5028-5033.
47. Attia, A.S. Potential for redox isomerism by quinone complexes of iron(III).
Studies on complexes of the FeIII(N-N)(DBSQ)(DBCat) series with 2,2'bipyridine and N,N,N',N'-tetramethylethylenediamine coligands / A.S. Attia, S.
Bhattacharya, C. G. Pierpont // Inorg. Chem. - 1995. – V. 34. - P. 4427-4433.
152
48. Attia, A.S. Iron-semiquinone, semiquinone-semiquinone, and iron-iron
magnetic exchange in monomeric and dimeric ferric complexes containing the
3,6-di-tert-butyl-1,2-semiquinonate ligand / A.S. Attia, B.J. Couklin, C.W.
Lange, C. G. Pierpont // Inorg. Chem. - 1996. - 35. - P. 1033-1038.
49. Chiari, B. Exchange interaction in multinuclear transition-metal complexes.
Nature of metal-metal coupling in dinuclear iron(III) systems containing Fe-OFe-O bridging units / B. Chiari, O. Piovesana, T. Tarantelli, P.F. Zanazzi //
Inorg. Chem. - 1984. – V. 23. - P. 3398-3404.
50. Shaikh, N. New route to the mixed valence semiquinone-catecholate based
mononuclear FeIII and catecholate based dinuclear MnIII complexes: first
experimental evidence of valence tautomerism in an iron complex / N. Shaikh,
S. Goswami, A. Panja, X.-Y. Wang, S. Gao, R.J. Butcher, P. Banerjee // Inorg.
Chem. - 2004. – V.43. - P. 5908-5918.
51. Липунова, Г.Н. Прогресс в химии формазанов: синтез-строение-свойства
/ Б.И. Бузыкин, Г.Н. Липунова, И.Г. Первова, В.М. Островская, И.Н.
Липунов, Т.И. Маслакова, Н.Ю. Стожко, В.А. Барачевский, Г.И.
Сигейкин; под ред. И.Н. Липунова, Г.И. Сигейкина. - М.: Научный мир,
2009. - 296 с.
52. Gilroy, J.B. Synthesis and characterization of 3-cyano- and 3-nitroformazans,
nitrogen-rich analogues of β-diketimine ligands / J.B. Gilroy, P.O. Otieno, M.J.
Ferguson, R. McDonald, R.G. Hicks // Inorg. Chem. - 2008. – V. 47. - P. 12791286.
53. Hiura, H. Resonance Raman and absorption studies of the configurations of
photochromic 3-alkylsubstituted 1,5-diphenylformazans: steric effect of the
substituent / H. Hiura, H. Takahashi // Journal of Mol. Struct. - 1989. – V. 212.
- P. 221-233.
54. Hunter, L. The associating effects of the hydrogen atom. Part LX. The N H-N
bond. Virtual tautomerism of the formazyl compaunds / L. Hunter, C. B.
Roberts // J. Chem. Soc. - 1941. - P. 820-823.
153
55. Hunter, L. The azo-group as a chelating group. Part V. Metallic derivatives of
arylazo-oximes and of formazyl compounds / L. Hunter, C. B. Roberts // J.
Chem. Soc. - 1941. - P. 823-826.
56. Gilroy, J.B. Transition metal complexes of 3-cyano- and 3-nitroformazans /
J.B. Gilroy, B.O. Patrick, R. McDonald, R.G. Hicks // Inorg. Chem. - 2008. –
V. 47. - P. 1287-1294.
57. Siedle, A.R. Formazanylpalladium compounds. Synthesis and structure of
bis(1,3,5-tri-p-tolylformazanyl) palladium / A.R. Siedle, L.H. Pignolet // Inorg.
Chem. - 1980. – V. 19. - P. 2052-2056.
58. Irving, H. The Structure of some di-(3-methyl-1,5-diarylformazyl)-nickel(II)
complexes / H. Irving, G.B. Gill, W.R. Cross // J. Chem. Soc. - 1960. - P.20872095.
59. Ермакова, М.И. К вопросу о строении формазанов. Изучение магнитной
восприимчивости комплексных соединений меди, кобальта и никеля с
формазанами / М.И. Ермакова, Е.И. Крылов, И.Я. Постовский // Журн.
общ. химии. - 1960. - 30. - С.849-854.
60. Липунова, Г.Н. Комплексные соединения никеля, меди и кобальта с
формазанами ряда бензазолов / Г.Н. Липунова, Е.И. Крылов, Н.П.
Беднягина, В.А. Шаров // Журн. общ. химии. - 1969. - 39. - С. 1293-1299.
61. Johnson, P.R. Infrared spectra of metal(II) 1,3,5-triarylformazan complexes /
P.R. Johnson, D.A. Thornton // Spectrosc. Lett. - 1974. - 7. P. 293-301.
62. Balt,
S.
Structure
and
redox
properties
of
the
bis(1,5-
diphenylformazan)copper(I) cation / S. Balt, W.E. Renkema, C. Cappelleveen,
C.H. Stam // J. Inorg. Nucl. Chem. - 1976. – V. 38. - P. 459-462.
63.Gilroy, J.B. The Design, Synthesis, and Chemistry of Stable Verdazyl Radicals
and Their Precursors: Thesis for the Degree of D.Ph / J.B. Gilroy - University
of Victoria, 2008. - 248 p.
64. Renkema,
copper(II),
W.E.
Ammine[l-(2-hydroxyphenyl)-3,5-diphenylformazanato]
C19H17CuIIN5O,
and
Ammine[1-(2-hydroxyphenyl)-3,5-
154
diphenylformazanato]nickel(II), C19H17N5NiIIO / W.E. Renkema, C.L. Lute,
C.H. Stam // Acta Crystallogr., B. - 1979. – V. 35. - P. 75-79.
65. Шмелев,
Л.В.
Строение
1-арил-3-алкил(фенил)-5-(2-бензтиазолил)
формазанатов цинка(II) и кадмия(II) / Л.В. Шмелев, И.Г. Первова, Г.Н.
Липунова,
Л.И.
Русинова,
А.В.
Кессених,
И.Н.
Липунов
//
Координационная химия. - 1992. - 18. - № 3. - С. 312-318.
66. Шмелев,
Л.В.
Строение
1-арил-3-фенил(алкил)-5-(2-бензтиазолил)
формазанатов никеля(II) / Л.В. Шмелев, Г.Н. Липунова, А.В. Кессених,
И.Г. Первова, И.Н. Полякова, З.А. Старикова, И.Н. Липунов //
Координационная химия. - 1993. - 19. - № 3. - С. 215-222.
67. Шмелев,
Л.В.
Строение
1-арил-3-фенил(алкил)-5-(2-бензтиазолил)
формазанатов кобальта(II) / Л.В. Шмелев, И.Г. Первова, Г.Н. Липунова,
А.В. Кессених, И.Н. Полякова, З.А. Старикова, И.Н. Липунов //
Координационная химия. - 1993. - 19. - № 12. - С. 904-910.
68. Brown, D. Iron and manganese complexes of benzothiazoiylformazans / D.
Brown, H. Bogge, G. Lipunova, A. Muller, W. Plass, K. Walsh // Inorg. Chim.
Acta. - 1998. – V. 280. - P. 30-38.
69. Balt,
S.
[l-(2-Carboxyphenyl)-3,5-diphenylformazanato](pyridine)
palladium(II), [Pd(C20H14N402)(C5H5N)] / S. Balt, C. Klok, J. Meuldijk, J.S.A.
De Boer // Acta Crystallogr. C. - 1985. – V. 41. - P. 528-530.
70. Kawamura, Y. An ESR study of 5-formazanyl copper(II) complexes as an
analogy to three types of copper-containing proteins / Y. Kawamura, Y.
Deguchi, J. Yamauchi // Bull. Chem. Soc. Jpn. - 1988. – V. 61. - P. 181-184.
71. Meuldijk,
J.
Ammine[l-(2-hydroxyphenyl)-3,5-diphenylformazanato]
nickel(II), [Ni(C19H14N4O)-(NH3)] , and [l-(2-hydroxyphenyl)-5-phenyl-3-(ptolyl)formazanato](pyridine)nickel(II), [Ni(C5H5N)(C20H16N4O)] / J. Meuldijk,
W.E. Renkema, A.M. Van Herk, C.H. Stam // Acta Crystallogr. C. - 1983. – V.
39. - P. 1536-1538.
155
72. Balt, S. Square planar complexes of nickel(II), palladium(II) and platinum(II)
with 1-(2-hydroxyphenyl)-3,5-diphenylformazan / S. Balt, J. Meuldijk, W.E.
Renkema // Transit. Met. Chem. - 1980. - 5. - P. 357-361.
73. Chang, M.-Ch. The
formazanate ligand
as
an
electron
reservoir:
bis(formazanate) zinc complexes isolated in three redox states / M.-Ch. Chang,
T. Dann, D.P. Day, M. Lutz, G.G. Wildgoose, E. Otten // Angew. Chem. Int.
Ed. - 2014. – V. 53. - P. 4118-4122.
74. Наканиси,
К.
Инфракрасные
спектры
и
строение
органических
соединений, пер. с англ. / К. Наканиси. - М.: Мир, 1965. - 220 с.
75. Pierpont, C.G Unique properties of transition metal quinone complexes of the
MQ3 series / C.G Pierpont // Coord. Chem. Rev. - 2001. – V. 219-221. - P. 415433.
76. Арапова,
А.В.
Термодинамические
свойства
о-семихиноновых
комплексов кобальта, никеля и меди в интервале от Т 0 до 350 К / А.В.
Арапова, М.П. Бубнов, Н.А. Протасенко, А.В. Черкасова, Н.Н. Смирнова,
А.В. Маркин, А.С. Богомяков, Г.А. Абакумов // Журнал физической
химии. - 2013. - 87. - № 4. - С. 562-569.
77. Adams, D.M. Controlling valence tautomerism of cobalt complexes containing
the benzosemiquinone anion as ligand / D.M. Adams, A. Dei, A.L. Rheingold,
D.M. Hendrickson // Angew. Chem. Int. Ed. - 1993. – V. 32. - P. 880-882.
78. Jung, O.-S. Intramolecular change distribution and related properties in a
series
of
3,6-di-tert-butylbenzoquinonatocobalt
complexes
containing
piperidine / O.-S. Jung, Y.-A Lee, S.H. Park, Y.J. Kim, K.H. Yoo, D.Ch. Kim
// Bull. Chem. Soc. Jpn. - 2001. – V. 74. - P. 305-309.
79. Пискунов, А.В. Kомплексы цинка и кадмия на основе 3,6-ди-третбутил-о-бенхохинона / А.В. Пискунов, А.В. Малеева, Г.А. Абакумов, В.К.
Черкасов, Г.К. Фукин, А.С. Богомяков // Коорд. химия. - 2011. - 37. - № 3.С. 1-13.
80. Lange, C.W. Radical superexchange in semiquinone complexes containing
diamagnetic metal ions. 3,6-Di-tert-butyl-1,2-semiquinonate complexes of
156
zinc(II), cobalt(III), gallium(III), and aluminum(III) / C.W. Lange, B.J.
Couklin, C.G. Pierpont // Inorg. Chem. - 1994. – V. 33. - P. 1276-1283.
81. Vinsova, J. Synthesis and antimicrobial evaluation of new 2-substituted 5,7-ditert-butylbenzoxazoles / J. Vinsova, K. Cermakova, A. Tomeckova, M.
Ceckova, J. Jampilek, P. Cermak, J. Kunes, M. Dolezale, F. Staudb // Bioorg.
Med. Chem. - 2006. - 14. - P. 5850-5865.
82. Ramalinghan, C. Synthesis and study of antibacterial and antifungal activities
of novel 1-[2-(benzoxazol-2-yl)ethoxy]- 2,6-diarylpiperidin-4-ones / C.
Ramalinghan, S. Balasubramanian, S. Kabilan, M. Vasudevan // Eur. J. Med.
Chem. - 2004. – V. 39. - P. 527-533.
83. Turan-Zitouni, G. Synthesis of some 2-[(benzazole-2-yl)thioacetylamino]
thiazole derivatives and their antimicrobial activity and toxicity / G. TuranZitouni, S. Demirayak, A. Ozdemir, Z.A. Kaplacikli, M.T. Yildiz // Eur. J.
Med. Chem. - 2004. – V. 39. - P. 267-272.
84. Rida, S.M. Synthesis of some novel benzoxazole derivatives as anticancer,
anti-HIV-1 and antimicrobial agents / S.M. Rida, F.A. Ashour, S.A.M. ElHawash, M.M. El-Semary, M.H. Badr, M.A. Shalaby // Eur. J. Med. Chem. 2005. – V. 40. - P. 949-959.
85. Kumar, D. Synthesis and evaluation of anticancer benzoxazoles and
benzimidazoles related to UK-1 / D. Kumar, M.R. Jacob, M.B. Reynolds, S.M.
Kerwin // Bioorg. Med. Chem. - 2002. - 10. - P. 3997-4004.
86. Kozich, V. Time-resolved resonance Raman scattering of the excited singlet
state of 2-(2′-hydroxyphenyl)benzoxazole after excited state intramolecular
proton transfer / V. Kozich, J. Dreyer, A. Vodchits, W. Werncke // Chem Phys.
Lett. - 2005. – V. 415. - P. 121-125.
87. Pierpont, C.G. Studies on charge distribution and valence tautomerism in
transition metal complexes of catecholate and semiquinonate ligands / C.G.
Pierpont // Coord. Chem. Rev. - 2001. - V. 216-217. - P. 99-125.
88. Sato, O. Control of magnetic properties through external stimuli / O. Sato, J.
Tao, Yu-Zh. Zhang // Angew. Chem. Int. Ed. - 2007. – V. 46. - P. 2152-2187.
157
89. Jung, O.-S. Low-energy cobalt(III)-catechol electron transfer. Subtle coligand
bonding effects for CoIII(N-N)(3,6-DBSQ)(3,6-DBCat) (N-N = 1,10phenanthroline,
5-Nitro-1,10-phenanthroline;
DBSQ
=
di-tert-
butylsemiquinonato; DBCat = di-tert-butylcatecholato) / O.-S. Jung, C.G.
Pierpont // J. Am. Chem. Soc. - 1994. – V. 116. - P. 1127-1128.
90. Caneschi, A. Antiferromagnetic coupling in a six-coordinate high spin
cobalt(II)-semiquinonato complex / A. Caneschi, A. Dei, D. Gatteschi, V.
Tangoulis // Inorg. Chem. - 2002. – V. 41. - P. 3508-3512.
91. Van Koten, G. 1,4-Diaza-1,3-butadiene (α-diimine) ligands: their coordination
modes and the reactivity of their metal complexes / G. Van Koten, K. Vrieze //
Adv. Organomet. Chem. - 1982. – V. 21. - P. 151-239.
92. Milione, S. Synthesis of α-diimine V(III) complexes and their role as ethylene
polymerisation catalysts / S. Milione, G. Cavallo, C. Tedesco, A. Grassi //
Dalton Trans. - 2002. - 8. - P. 1839-1846.
93. Schleis, T. Ethylene polymerization catalysts based on nickel(II) 1,4diazadiene complexes: the influence of the 1,4-diazadiene backbone
substituents on structure and reactivity / T. Schleis, T.P. Spaniol, J. Okuda, J.
Heinemann, R. Meulhaupt // J. Organomet. Chem. - 1998. – V. 569. - P. 159167.
94. Knisley, T.J. Volatility and high thermal stability in mid- to late-first-row
transition-metal diazadienyl complexes / T.J. Knisley, M.J. Saly, M.J. Heeg,
J.L. Roberts, C.H. Winter // Organometallics – 2011. – V. 30. - P. 5010-5017.
95. Kahn, O. Molecular Magnetism / O. Kahn - Weinheim: Wiley-VCH, 1993. 380 с.
96. Muresan, N. Neutral bis(1,4-diaza-1,3-butadiene)nickel complexes and their
corresponding monocations: molecular and electronic structures. A combined
experimental and density functional theoretical study / N. Muresan, T.
Weyhermueller, K. Wieghardt // Dalton Trans. - 2007. – V. 39. - P. 4390-4398.
97. Ghosh, M. A structural, spectroscopic and computational study of the
molecular and electronic structure of a [bis(α-diiminato)manganese(II)] π
158
radical complex / M. Ghosh, T. Weyhermueller, K. Wieghardt // Dalton Trans.
- 2008. - P. 5149-5151.
98. Kreisel, K.A. Synthesis, characterization, and electronic structure of diimine
complexes of chromium / K.A. Kreisel, G.P.A. Yap, K.H. Theopold // Inorg.
Chem. - 2008. – V. 47. - P. 5293-5303.
99. Khusniyarov, M.M. Tuning the oxidation level, the spin state, and the degree
of electron delocalization in homo- and heteroleptic bis(α-diimine)iron
complexes / M.M. Khusniyarov, T. Weyhermeuller, E. Bill, K. Wieghardt // J.
Am. Chem. Soc. - 2009. – V. 131. - P. 1208-1221.
100. Ovcharenko, V.I. Ligand effects on the ferro- to antiferromagnetic exchange
ratio in bis(o-semiquinonato)copper(II) / V.I. Ovcharenko, E.V. Gorelik, S.V.
Fokin, G.V. Romanenko, V.N. Ikorskii, A.V. Krashilina, V.K. Cherkasov,
G.A. Abakumov // J. Am. Chem. Soc. - 2007. – V. 129. - P. 10512-10521.
101. Ashley, J.N. Tetrazolium compounds. Part I. Tetrazolium compounds
containing substituted phenyl and heterocyclic rings / J.N. Ashley, B.M. Davis,
A.W. Nineham, R. Slack // J. Chem. Soc. - 1953. - P. 3881-3888.
102. Фролова, Н.А. Гетарилформазаны
как
исходные
соединения в
синтезе пяти- и шестичленных гетероциклов и металлациклов: дис. …
канд. хим. наук: 02.00.03 / Фролова Наталья Анатольевна. – Москва, 2006.
- с.172.
103. Dodonov, V.A. Synthesis and structural characterization of some complexes
of hexa-coordinated antimony / V.A. Dodonov, A.Yu. Fedorov, G.K. Fukin,
S.N. Zaburdyaeva, L.N. Zakharov, A.V. Ignatenko // Main Group Chem. –
1999. – V. 3. - № 1. – P. 15-22.
104. Фукин, Г.К. Синтез и строение шестикоординационных донорноакцепторных комплексов R3(C6H4O2)Sb…L (R = Ph, L = OSMe2, ONC5H5;
R = Me, L = ONC5H5, NC5H5) и R3(C2H4O2)Sb…L (R = Ph, L = ONC5H5; R =
Cl, C6F5, L= OPPh3) / Г.К. Фукин, Л.Н. Захаров, Г.А. Домрачев, А.Ю.
Федоров, С.Н. Забурдяева, В.А. Додонов // Изв. АН. Сер. хим. – 1999. - №
9. – С. 1744-1753.
159
105. Frolova, N.A. Pyridine-containing nickel(II) bis-formazanates: synthesis,
structure, and electrochemical study / N.A. Frolova, S.Z. Vatsadze, V.E.
Zavodnik, R.D. Rakhimov, N.V. Zyk // Russian Chemical Bulletin, Int. Ed. 2006. – V. 55. - P. 1810-1818.
106. Jameson, G.B. Cyclometalated formazan derivatives of ruthenium and
osmium: structure of Ru((o-C,H,)N=NC(Ph)=NNPh)(CO)(PPh3)2 / G.B.
Jameson, A. Muster, R.D. Robinson, J.N. Wingfield, J.A. Ibers // Inorg. Chem.
- 1981. – V. 20. - P.2448-2456.
107. Авраменко, Г.В. Боратетразины. II. О синтезе боратетразинов, не
содержащих у атома углерода ароматического остатка / Г.В. Авраменко,
Т.С. Колодина, Б.И. Степанов // Журнал общей химии. - 1983. - 53. - № 6.
- С. 1340-1344.
108. Зайцев, Б.Е. Рентгеноэлектронные спектры 2,3,5-триарил-Δ4-1,3,4,2триазаборолинов и 1,1-диацетокси-2,4,6-триарил-1,2,3,5,6-боратетразинов
/ Б.Е. Зайцев, З.В. Безуглая, Г.В. Авраменко, Т.М. Иванова, В.Н.
Лисютенко, Б.И. Степанов // Журнал общей химии. - 1985. - 55. - № 6. - С.
1398-1403.
109. Степанов, Б.И. Синтез борсодержащих комплексов на основе
гидроксизамещенных
триарилформазанов
/
Б.И.
Степанов,
Г.В.
Авраменко, Салех Хамуд, Ш.И. Мустафаева // Журнал общей химии. 1986. - 56. - № 2. - С. 390-392.
110. Гордон, А. Спутник химика / А. Гордон, Р. Форд. - М.: Мир, 1976. - С.
437-444.
111. Райхардт, К. Растворители и эффекты среды в органической химии / К.
Райхардт. - М.: Мир, 1991. – 763 с.
112. Пугачевич,
П.П.
Работа
со
ртутью
в
лабораторных
и
производственных условиях / П.П. Пугачевич. - М.: Химия, 1972. – 320 с.
113. Litvinenko, A.S. Effect of spin-orbit coupling on the magnetic susceptibility
of polynuclear complexes of 3d metals containing a Co2+ ion / A.S. Litvinenko,
160
E.A. Mikhaleva, S.V. Kolotilov, V.V. Pavlishchuk // Theoretical and
experimental chemistry. - 2011. – V. 46. - P. 422-428.
114. Polunin, R.A. Topology control of porous coordination polymers by
building block symmetry / R.A. Polunin, S.V. Kolotilov, M.A. Kiskin, O.
Cador, E.A. Mikhalyova, A.S. Lytvynenko, S. Golhen, L. Ouahab, V.I.
Ovcharenko, I.L. Eremenko, V.M. Novotortsev, V.V. Pavlishchuck // Eur. J.
Inorg. Chem. - 2010. - P. 5055-5057.
115. Бузыкин, Б. И. Химия гидразонов. / Б. И. Бузыкин. - М.: Наука, 1977. –
189 с.
116. Cherkasov,
V.K.
Oxidative
addition
reaction
of
o-quinones
to
triphenylantimony: novel triphenylantimony catecholate complexes / V.K.
Cherkasov, E.V. Grunova, A.I. Poddel’sky, G.K. Fukin, Yu.A. Kurskii, L.G.
Abakumova, G.A. Abakumov // J. Organomet. Chem. – 2005.- V. 690. - P.
1273-1281.
161
Нумерация соединений
№
Аббревиатура
№
Аббревиатура
1
Co(3,6-SQ)2L(I)
22
Fe(3,6-SQ)2DAD
2
Co(3,6-SQ)2L(II)
23
Co(3,6-SQ)2(DABCO)
3
Co(3,6-SQ)2L(III)
24
Ph-FormH
4
Co(3,6-SQ)2L(IV)
25
F-FormH
5
Co(3,6-SQ)2L(V)
26
I-FormH
6
Mn(3,6-SQ)2L(I)
27
4-Py-FormH
7
Mn(3,6-SQ)2L(III)
28
4-Py-NO2-FormH
8
Mn(3,6-SQ)2L(V)
29
4-Py-(Me2Ph)-FormH
9
Fe(3,6-SQ)2L(I)
30
(3,6-Cat)(4-Py-(Me2Ph)-FormH)SbPh3
10
Fe(3,6-SQ)2L(III)
31
Co(3,6-SQ)2(Ph-Form)
11
Co(3,6-SQ)2(PPh3)
32
Co(3,6-SQ)2(F-Form)
12
Zn(3,6-SQ)2L(II)
33
Co(3,6-SQ)2(I-Form)
13
Co(3,6-SQ)2L(VI)
34
Co(3,6-SQ)(3,6-Cat)(4-Py-FormH)
14
Mn(3,6-SQ)2L(VI)
35
Co(3,6-SQ)(3,6-Cat)(4-Py-NO2-FormH)
15
Fe(3,6-SQ)2L(VI)
36
Co(3,6-SQ)(3,6-Cat)(4-Py-(Me2Ph)-FormH)
16
Co(3,6-SQ)2L(VII)
37
Co(3,6-SQ)(Ph-Form)
17
Co(3,6-SQ)2Biq
38
Co(3,6-SQ)(Ph-Form)2
18
Mn(3,6-SQ)2Biq
39
Mn(3,6-SQ)2(Ph-Form)
19
Fe(3,6-SQ)2Biq
40
Mn(3,6-SQ)2(4-Py-FormH)
20
Co(3,6-SQ)2DAD
41
CoIII(3,6-SQ)(3,6-Cat)Verd
21
Mn(3,6-SQ)2DAD
42
Mn(3,6-SQ)2 Verd
·
·
162
Благодарности
Выражаю благодарность моему научному руководителю
Черкасову Владимиру Кузьмичу
Выражаю благодарность за помощь в проведении эксперимента:
Магнетохимические измерения
Богомяков А.С. (МТЦ РАН)
ЭСП
Лопатин М.А. (ИМХ РАН)
Лопатина Т.И. (ИМХ РАН)
ИК-спектроскопия
Кузнецова О.В. (ИМХ РАН)
Хамалетдинова Н.М. (ИМХ РАН)
РСА
Фукин Г.К. (ИМХ РАН)
Черкасов А.В. (ИМХ РАН)
Сомов Н.В. (ННГУ)
Элементный анализ
Новикова О.В. (ИМХ РАН)
Чулкова Т.И. (ИМХ РАН)
ЦВА
Отдельная
Смолянинов И.В. (АГТУ)
благодарность
Поддельскому
Андрею
Игоревичу
за
плодотворное обсуждение результатов и всему коллективу лаборатории
ХЭОС за моральную поддержку
163