Билибин Д.П. Атеросклероз (лекция)
advertisement

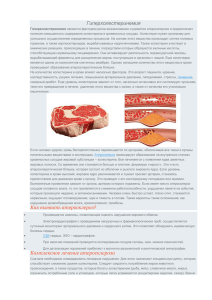
Частная патофизиология Лекция для студентов 3-го курса, специальности: «лечебное дело», «стоматология» Атеросклероз 1. План лекции 1. Определение понятия «атеросклероз». Место атеросклероза в сердечно-сосудистой патологии 2. Из истории изучения атеросклероза. Теории атеросклероза 3. Эндотелий. Факторы сохранения и повреждения 4. Строение и функции липопротеинов 5. Транспорт холестерина в субэндотелий 6. Атеросклеротическая бляшка 7. Патогенез атеросклероза 8. Исходы атеросклероза 9. Принципы патогенетической терапии атеросклероза 2. Определение понятия «атеросклероз» Одним из самых распространенных заболеваний, играющим важнейшую роль в развитии других патологических процессов, поражающих сердечно-сосудистую систему является атеросклероз. Термин атеросклероз происходит от двух греческих слов: athere - кашица (в данном случае липидный детрит) и sclerosis - затвердение, и означает разрастание соединительной ткани в стенке сосуда. Следует указать, что разрастание соединительной ткани в стенке артерии может быть следствием самых различных заболеваний. Существует патологический процесс, который носит название болезни Менненберга, или атерокальциноза. Он заключается в том, что в средней оболочке сосуда начинают откладываться соли кальция, вокруг которых развивается реактивное воспаление, и окружающая ткань склерозируется. В основе развития склеротических процессов в сосудистой стенке может лежать гиалиноз, который является следствием ее пропитывания плазматическими белками. Если в стенке артерии развился воспалительный процесс, то он тоже может завершиться склерозированием ткани. Например, при сифилитическом мезоаортите (сифилитическом воспалении средней оболочке аорты) в ней развивается склероз - разрастается соединительная ткань, и интима аорты становится морщинистой, приобретает вид “шагреневой кожи”. 2 Склероз сосудистой стенки может возникать и при аллергических васкулитах, когда она поражается антителами, и в очагах этого поражения начинается склеротический процесс. Таким образом, атеросклероз является одной из разновидностей артериосклероза, той его разновидностью, когда соединительная ткань разрастается в ответ на образование в стенке сосуда липидного детрита. Однако, следует подчеркнуть, что, хотя атеросклероз и находит свое выражение в поражении сосудистой стенки, тем не менее, он представляет собой заболевание организма в целом. Это положение можно проиллюстрировать одним ярким примером. Хирург Кристиан Барнард пересадил Филиппу Блайбергу - человеку пожилого возраста сердце от молодого донора, погибшего в результате кровоизлияния в мозг. Когда через восемнадцать месяцев Блайберг скончался, на секции было обнаружено, что коронарные сосуды пересаженного сердца сильно изменены атеросклерозом; состояние венечных артерий этого, полтора года назад молодого, сердца было таким же, как и остальных сосудов пожилого реципиента. Следовательно, дело заключается не столько в местных изменениях сосудистой стенки, сколько в общем нарушении обмена веществ организма. На основании современных представлений об этиологии, патогенезе и проявлениях атеросклероза можно дать следующее определение этому процессу: Атеросклероз - это заболевание, возникающее в результате первичной альтерации эндотелия сосудов, поражающее преимущественно артерии мышечного и мышечноэластического типа, в основе которого лежит воспалительный процесс и нарушение транспортной функции липопротеинов, проявляющееся имбибицией сосудистой стенки липидами с последующим развитием вокруг этих отложений реактивных изменений. Представленные ниже рисунки демонстрируют динамику смертности от сердечнососудистых заболеваний в России и США. Эта патология занимает ведущее место (около 60%) среди всех причин смерти людей в развитых странах мира. Если же проанализировать причины возникновения сердечно-сосудистых заболеваний, то можно констатировать, что атеросклероз лежит в основе не менее 90% всех случаев возникновения этой патологии. Таким образом, изучение этиологии, патогенеза и исходов атеросклероза является для современной медицины в высшей степени актуальной проблемой. 3 Динамика смертности от сердечно-сосудистых заболеваний в США (по О.П.Шевченко, О.Д.Мишнёв) 4 Динамика смертности в России по различным классам причин 3. Из истории изучения атеросклероза. Теории атеросклероза Описание истории изучения атеросклероза следует начать с трудов Альбрехта фон Галлера (1708 – 1777 гг.) – известного ученого-естествоиспытателя, анатома, физиолога, хирурга, химика – все направления деятельности этого замечательного человека трудно перечислить. Швейцарец по происхождению А.Галлер в период своей работы в Геттингенском университете описал (1755) жировые отложения в стенке сосудов, которым он присвоил название «атером». Систематические исследования атеросклероза относятся уже к XIX веку. Так Карл Рокитанский (1804 – 1878) известный австрийский патолог, чех по происхождению, в 1850 году опубликовал свои работы, в которых рассматривал атеросклеротические повреждения сосудов как результат проникновения («инкрустации») фибрина и тромботических компонентов в сосудистую стенку. Современник К.Рокитанского – великий немецкий патолог Рудольф Вирхов (1821 – 1902) считал, что атеросклеротиское повреждение сосудов связано с воспалительным процессом, в результате которого происходит раздражение и повреждение интимы, приводящее к дистрофии и жировой инфильтрации сосудистой стенки. Большой вклад в изучение атеросклероза внес ученик и ассистент Р.Вирхова – Ю.Конгейм (1839 – 1884), который считал, что в основе развития атеросклероза лежит хроническое воспаление сосудистой стенки, завершающееся жировой дистрофией, склерозом и кальцинозом. 5 Как мы увидим из дальнейшего изложения, гипотезы Р.Вирхова и Ю.Конгейма о роли воспалительного процесса в патогенезе атеросклероза оказались весьма прозорливыми. В 1911 году российские ученые Н.Н.Аничков (1885 – 1964) и С.С.Халатов (1884 – 1951) опубликовали результаты своих экспериментальных исследований, которые убедительно показали, что причиной атеросклероза является повышенное потребление с пищей продуктов, содержащих значительное количество холестерина. В дальнейшем, на основании данных своих исследований атеросклероза Н.Н.Аничков сформулировал инфильтрационную теорию этого заболевания, согласно которой атеросклероз развивается в результате повышенного накопления в сосудистой стенке холестерина при условии его недостаточного удаления и снижения метаболизма этого липида. В середине прошлого века Н.Н.Аничков и С.С.Халатов трансформировали свою инфильтрационную теорию атеросклероза в «инфильтрационнокомбинационную», согласно которой важную роль в развитии атеросклероза играет не только холестерин пищевых продуктов, но и эндогенный холестерин, отложение которого в сосудистой стенке связано с расстройством нейро-гуморальной регуляции метаболизма липидного и белкового обменов организма. Морфогенез атеросклероза был подробно описан в 1958 году российским патологом В.Д.Цинзерлингом и другими авторами (пять стадий атеросклероза: липоидоз, липосклероз, атероматоз, атерокальциноз, атероматозная язва). В дальнейшем А.Л.Мясниковым и А.М.Вихертом (1962 – 1965) была описана так называемая «долипидная стадия» атеросклероза, в процессе развития которой нет явных морфологических изменений сосудистой стенки, но имеется только альтерация эндотелия сосудов, являющаяся пусковым механизмом всех дальнейших стадий патогенеза этого заболевания. Представления о патогенезе атеросклероза были значительно расширены после появления исследований различных видов липопротеинов – сложных структур, образованных липидами (холестерином, эфирами холестерина, триглицеридами, фосфолипидами) и белками – апопротеинами, и их роли в транспорте холестерина как к сосудистой стенке и другим внесосудистым структурам, так и к печени для их утилизации и трансформации (Дж.Гофман, Д.С.Фредериксон, 1954, 1961, 1967). Схема транспортной функции липопротеинов различных видов получила законченный вид после открытия рецепторов липопротеинов двумя американскими учеными Дж.Л.Голдштейном и М.С.Брауном, получившим за открытие этих рецепторов и описание патогенеза семейной гиперхолестеринемии в 1985 году Нобелевскую премию. В целом, не смотря на все еще имеющиеся «белые пятна», к 90-м годам прошлого века схема патогенеза атеросклероза, примирившая различные теории его происхождения, была вырисована достаточно полно. Принципиальные положения этой схемы заключались в 6 следующем. Атеросклероз начинается с повреждения эндотелия сосудов («теория ответа на повреждение», Р.Росс, А.Гломсет, А.Готто, Р.Джексон, 1976). Далее, в результате измененных отношений между эндотелиоцитами, макрофагами и некоторыми липопротеинами происходит сначала внутриклеточное, а затем и внеклеточное накопление липидов (холестерина). В свою очередь, альтерация сосудистой стенки способствует как развитию воспаления, так и пролиферации гладкомышечных клеток и синтезу ими коллагена, эластина и гликозаминогликанов, образующих покрышку и другие соединительнотканные элементы атеросклеротической бляшки. Рост, развитие, а в последующем, и разрыв атеросклеротической бляшки способствует образованию и отрыву тромбов, выходу атероматозных масс в просвет сосуда, инициации тромбоэмболических повреждений. Среди этиологических факторов, способствующих первичному повреждению эндотелия сосудов, патологи и клиницисты основную роль отводят артериальной гипертензии, сахарному диабету 2-го типа, курению, некоторым микроорганизмам и вирусам, гомоцистеинемии. О последнем повреждающем факторе необходимо упомянуть отдельно. В начале 60-х годов американский патолог Kilmer MaCully связал увеличение концентрации в крови гомоцистеина и повреждение сосудистого эндотелия. В последующем, уже в конце прошлого века многие исследователи подтвердили его предположение. Гомоцистеин – аминокслота, образующаяся в результате метаболизма широко известной аминокислоты – метионина. Утилизация гомоцистеина в организме происходит при обязательном участии таких кофакторов как фолиевая кислота, витамины В6 и В12. Показано, что увеличение концентрации гомоцистеина на 5 – 10 мкмоль/л (норма: 5 – 15 мкмоль/л) приводит к увеличению риска развития атеросклероза на 80% у женщин и на 60% у мужчин (Boushey, 1995). Известно, что потере организмом витаминов группы В и фолиевой кислоты способствует гипергликемия – патология, характерная для сахарного диабета. Само повреждающее действие гомоцистеина на сосудистый эндотелий, по-видимому, связано с его способностью при окислении образовывать большое количество свободных радикалов, содержащих активный кислород. Кроме того, гомоцистеин способствует окислению липопротеинов низкой плотности и пролиферации гладкомышечных клеток сосудов. 4. Теории происхождения атеросклероза На представленном ниже рисунке в обобщенном виде изображены основные теории происхождения атеросклероза. Об их сущности и том времени, когда они были выдвинуты теми или иными учеными достаточно подробно было сказано в предыдущем разделе лекции. Следует только указать, что, как это часто и бывает в науке, каждая из этих теорий описывала какойнибудь конкретный этиопатогенетический механизм, лежащий в основе развития атеросклероза, 7 и, практически, каждая из них сыграла свою роль в формировании современных представлениях об этиологии и патогенезе этого заболевания. Теории этиопатогенеза атеросклероза Особое место среди теорий, объясняющих происхождение атеросклероза, занимает паразитарная теория. Действительно, многочисленные исследования выявили в атероматозных бляшках два вида инфекционных агентов – Chlamydia Pneumoniae и вируса цитомегалии, относящегося к семейству герпес-вирусов. Оба вида этих инфекционных агентов весьма широко распространены среди населения и их наличие в организме человека достоверно коррелируется с наличием атеросклеротических поражений сосудов. Так цитомегаловирус у пациентов, страдающих выраженным атеросклерозом, обнаруживается в макрофагах, фибробластах и эндотелиальных клетках. С другой стороны, Ch. Pneumoniae так же находят в макрофагах, эндотелиоцитах, гладкомышечных клетках сосудов. Кроме того, исследования показывают, что эти микроорганизмы резко увеличивают агрегацию тромбоцитов к сосудистой стенке за счет усиления экспрессии Р-селектина тромбоцитами. По-видимому, и цитомегаловирусы и хламидии способны индуцировать микровоспалительный процесс в сосудистой стенке, способствуют перекисной модификации макрофагов и превращению их в пенистые клетки, а также увеличивают агрегационные свойства тромбоцитов. Излишне 8 говорить, что все эти процессы являются различными звеньями патогенеза атеросклероза и, в конечном итоге, приводят к формированию атеросклеротических бляшек. 5. Повреждение сосудистого эндотелия – пусковой механизм развития атеросклероза В настоящее время подавляющее большинство патологов считает, что пусковым моментом для развития атеросклероза сосудов является повреждение (десквамация) сосудистого эндотелия. Основные повреждающие факторы представлены на рисунке. Основные этиологические факторы, вызывающие повреждение эндотелия сосудов Гипертензия является мощным фактором повреждения эндотелия сосудов, особенно в местах их бифуркации. Это явление хорошо иллюстрирует приводимый ниже рисунок. 9 Роль гипертензии в повреждении сосудистого эндотелия В участке «а» давление крови наибольшее, напряжение сдвига максимальное. Именно здесь и происходит разрушение эндотелиоцитов и их десквамация (слущивание) с поверхности сосуда. В участке «б» давление крови наименьшее. Повреждение эндотелия на этих участках не происходит. Как известно, гипертоническая болезнь и атеросклероз – это два патологических процесса, тесно связанные между собою, или, точнее, способствующие развитию друг друга. Связь между курением и атеросклерозом известна давно. Помимо приведенных на рисунке проатеросклеротических факторов, связанных с курением, следует иметь в виду, что у курильщиков усиленно продуцируются многие цитокины – активаторы воспаления. Таким образом, косвенно курение способствует поддержанию воспалительного процесса в местах повреждения сосудистого эндотелия. О возможном влиянии на повреждение эндотелия и развитие атеросклероза некоторых инфекционных агентов было уже сказано. Стоит добавить, что антигены микробов и вирусов, внедрившиеся в эндотелиоциты и гладкомышечные клетки, способствуют активации соответствующих клеточных и гуморальных факторов иммунитета, что, в свою очередь, провоцирует и поддерживает воспалительный процесс. В разделе лекции, посвященном истории изучения атеросклероза была уже описана роль гомоцистеина повреждающим (точнее, гипергомоцистеинемии) фактором в развитии атеросклероза. Основным гипергомоцистеинемии является значительное увеличение образования свободных радикалов. По отношению к сосудистому эндотелию этот фактор, безусловно, является повреждающим. 10 5.2. Эндогенные повреждающие и защитные факторы эндотелия сосудов Как видно из представленного рисунка, повреждающие факторы способны вызывать спазм сосудов, способствуют процессу тромбообразования, увеличивают пролиферация гладкомышечных клеток, входящих в состав сосудистой стенки, и, в целом, способствуют повреждению эндотелия. Более того, большинство этих факторов начинают продуцироваться в ненормально больших количествах именно клетками поврежденного эндотелия. Наоборот, факторы, защищающие эндотелий сосудов, обеспечивают вазодилатацию, препятствую тромбообразованию. Именно эти факторы выделяются неповрежденным сосудистым эндотелием. 6. Строение и функции липопротеинов По современным представлениям основной причиной возникновения атеросклероза являются нарушения в транспорте и утилизации холестерина клетками организма, в том числе – и клетками эндотелия сосудов. Холестерин в организме может транспортироваться только в виде сложных по своему строению высокомолекулярных соединений (комплексов), отличительной особенностью которых является их водорастворимость. К таким соединениям относятся хиломикроны и липопротеины. Последние играют основную роль в доставке холестерина к клеткам эндотелия сосудов, к клеткам печени и других органов и тканей организма. Липопротеины синтезируются и секретируются клетками печени и эпителиальными клетками тонкого кишечника. Все виды липопротеинов имеют мицеллярную структуру и, независимо от их величины и плотности, построены по одному и тому же принципу. В центре мицеллы находится жировая капля (ядро), состоящее из неполярных липидов (триглицеридов и 11 эфиров холестерина). Оболочка мицеллы образована фосфолипидным монослоем, в который встроены молекулы белков (апопротеинов) и свободного холестерина. Схема строения мицеллы липопртеинов Мицеллы липопротеинов имеют различные размеры и плотность и содержат различное количество белков (апопротеинов), холестерина и триглицеридов. Выделено три основные вида липопротеинов: липопротеины очень низкой плотности (ЛПОНП, пре-β-липопротеины), липопротеины низкой плотности (ЛПНП, β-липопротеины) и липопротеины высокой плотности (ЛПВП, α-липопротеины). Первые два вида липопротеинов переносятся кровотоком в соединении с β-глобулинами, ЛПВП – в соединении с γ-глобулинами плазмы крови. Таблица 1. Основные свойства липопротеинов Дополнительные сведения о различных видах липопротеинов дает представленная выше таблица. 7. Транспорт холестерина в субэндотелий Основным переносчиком холестерина (его в мицелле этого вида липопротеинов содержится более 50%) являются ЛПНП. В ЛПОНП холестерина содержится несколько меньше. Этот вид липопротеинов в основном является переносчиком триглицеридов. ЛПВП содержат очень мало холестерина и много белка и фосфолипидов. 12 ЛПНП доставляют холестерин к клеткам организма, в том числе – и к клеткам эндотелия сосудов. ЛПВП, наоборот, переносят холестерин от клеток различных органов и тканей к клеткам печени, где он и метаболизируется. Следует иметь в виду, что холестерин может проникнуть в клетку только благодаря рецепторам ЛПНП. При соединении ЛПНП с соответствующими рецепторами (рецепторы ЛПНП), холестерин выделяется из мицеллы, переносится в протоплазму клетки и там используется для ее нужд. С другой стороны, при переносе холестерина из клеток организма (в том числе – и из клеток сосудистого эндотелия) к клеткам печени с помощью ЛПВП он может проникнуть в гепатоциты только благодаря рецепторам ЛПВП, находящимся на мембране гепатоцитов. Таким образом, как усвоение холестерина клетками эндотелия сосудов, так и перенос излишков холестерина от клеток эндотелия сосудов к гепатоцитам и усвоение ими холестерина зависит от состояния и плотности соответствующих рецепторов на мембране клеток. В норме клетки способны увеличивать или уменьшать количество рецепторов как ЛПНП, так и ЛПВП. Однако, в значительной степени эта их особенность генетически детерминирована. Схема осуществления транспортной функции липопротеинов Весьма серьезную роль в контактах липопротеинов с рецепторным аппаратом клеток играют апопротеины, которые, как мы помним, встроены в липидный монослой мембраны липопротеиновой мицеллы. Именно молекулы апопротеинов мицеллы липопротеинов являются лигандами, связывающими соответствующий липопротеин с его рецептором. Они же в ряде случаев играют и роль кофакторов для соответствующих ферментов. В настоящее время выделено четыре вида апопротеинов. Апо-А – обеспечивает связь ЛПВП с соответствующим рецепторным аппаратом. Апо-В – обеспечивает связь ЛПНП с рецепторным аппаратом клеток печени и периферических тканей; 13 Апо-С-II – кофактор для липопротеиновой липазы, благодаря которой триглицериды удаляются из хиломикронов и ЛПОНП; Апо-Е – обеспечивает связь липротеинов с рецепторным аппаратом гепатоцитов. Описан и еще один вид апопротеинов – так называемый апопротеин (а), которому приписывают наибольшую атерогенность и входящий в состав ЛПНП. Атерогенность этого апопротеина объясняют несколькими его свойствами. Во-первых, он легко окисляется и поглощается макрофагами. Во-вторых, печеночные клетки имеют наименьшее количество рецепторов к ЛПНП, содержащим липопротеин (а). И, наконец, в-третьих, имеются данные о том, что ЛПНП, содержащие липопротеин (а), обладают повышенными антитромболитическими свойствами. Учитывая особенности транспорта холестерина липопротеинами (от печени к клеткам других органов и тканей и от клеток органов и тканей к клеткам печени) одни из них (ЛПОНП и, особенно, ЛПНП) получили название «атерогенных липопротеинов», а другие (ЛПВП) – «антиатерогенных липопротеинов». Однако, говорить о том, что патогенез атеросклероза определяется только уровнем концентраций в плазме крови атерогенных и антиатерогенных липопротеинов, конечно, нельзя. Нужно не забывать о достаточности (недостаточности) соответствующего рецепторного аппарата, а также о полноценной (или неполноценной) функции апопротеинов, входящих в состав мицеллы липротеинов. Кроме того, значительную роль в провокации атеросклероза играют и, так называемые, «модифицированные» липопротеины. Причин модификации (изменения) липопротеинов достаточно много1, однако основной из них является их перекисное окисление. В результате перекисного окисления «нормальные» липопротеины приобретают атерогенные свойства, которые объясняются двумя . Перекисное окисление ЛПНП и образование «пенистых» клеток причинами. 1 Мощным фактором, обеспечивающим перекисное окисление ЛПНП, является воспалительный процесс, в результате которого образуется значительное количество свободных радикалов. Сам же воспалительный процесс инициируется альтерацией сосудистого эндотелия. 14 Во-первых, модифицированные липопротеины могут без каких-либо ограничений накапливаться в макрофагах, что заставляет их превращаться в «пенистые клетки» - один из основных факторов морфогенеза атеросклероза. Известно, что макрофаги в норме поглощают избыток ЛПНП и, метаболизируя их, предотвращают перегрузку клеток эндотелия сосудов холестерином. Этот процесс регулируется по принципу обратной связи: при заполнении макрофага достаточным количеством ЛПНП чувствительность рецепторного аппарата макрофага к ЛПНП резко падает и он перестает их поглощать. Модифицированные ЛПНП нарушают эту регуляционную связь, и макрофаги поглощают эти липотротеины без каких-либо ограничений, вплоть до их полной перегрузки и превращения в пенистые клетки. модифицированные ЛПНП Захват модифицированных ЛПНП скевенджер-рецепторами макрофагов (по О.П.Шевченко, О.Д.Мишнёв) Роль макрофагов, трансформирующихся в пенистые клетки, в развитии атеросклероза Важную роль в захвате модифицированных ЛПНП макрофагами играют, так называемые, рецепторы-мусорщики (скевенджер-рецепторы), которые синтезируются в макрофагах, перегруженных модифицированными ЛПНП. Именно образование этих рецепторов и нарушает деятельность обратной регулирующей связи, которая была уже упомянута выше. 15 Во-вторых, белки, входящие в состав модифицированных липопротеинов, приобретают антигенные свойства, благодаря чему к ним начинается выработка аутоантител, повреждающих, в том числе, и клетки эндотелия сосудов и тромбоциты. Так запускается еще один патологический цикл, лежащий в основе развития атеросклероза. Таким образом, об «атерогенности» и «антиатерогенности» тех или иных липопротеинов, если мы имеем в виду нормальный организм, говорить не приходится. «Атерогенность», например, ЛПНП проявляется только тогда, когда в действие вступают другие факторы патогенеза атеросклероза. 7. Механизмы формирования атеросклеротической бляшки Представленная ниже схема иллюстрирует механизмы образования атеросклеротической бляшки. Из схемы следует, что основными пусковыми механизмами, обеспечивающими формирование атеросклеротической бляшки, являются альтерация сосудистого эндотелия, местный воспалительный процесс, возникающий в результате альтерации, концентрация пенистых клеток, содержащих ЛПНП, а, следовательно, и большое количество холестерина, в субэндотелии. Механизмы образования атеросклеротической бляшки Превратившиеся в пенистые клетки, перегруженные модифицированными ЛПНП макрофаги разрушаются за счет некроза и апоптоза, холестерин откладывается в субэндотелии. Процесс гибели пенистых клеток еще больше подстегивает воспаление за счет образования провоспалительных цитокинов (интерлейкина 1, фактора некроза опухолей и т.п.). В этот же период времени происходит активация гладкомышечных клеток. Под влиянием ряда ростовых факторов и провоспалительных цитокинов они приобретают подвижность, мигрируют из медии в интиму и субэндотелиальный слой и там становятся секреторно-активными. Продуцируемый 16 ими коллаген образует соединительнотканный слой покрышки атеросклеротической бляшки. Сформировавшаяся атеросклеротическая бляшка вступает в свой собственный цикл развития. Схема миграции и трансформации гладкомышечных клеток (по О.П.Шевченко, О.Д.Мишнёву) PDGF, α-FGF, TGF-β, IGF – ростовые факторы, IL-1 – интерлейкин 1 7.1. Разрушение атеросклеротической бляшки Как известно, одним из тяжелых исходов атеросклероза является изъязвление атеросклеротической бляшки (стадия атероматозной язвы), в результате которого бляшка становится мощным фактором тромбообразования, а детрит, содержащийся в ней, приобретает свойства микроэмболов. Именно поэтому изучение механизмов разрушения покрышки бляшки имеет важное значение для клиницистов и патологов. Помимо чисто физических механизмов разрушения бляшки (воздействие на покрышку тока крови), описаны и механизмы апоптоза, благодаря которым разрушаются такие клеточные составляющие покрышки как эндотелиоциты и гладкомышечные клетки. Роль апоптоза в разрушении атеросклеротической бляшки Для правильного понимания вышеприведенной схемы вспомним как развивается процесс «инструктивного апоптоза». Известно, что процесс апоптоза может инициироваться внешними сигналами, которые одна клетка передает другой. Роль сигнальных молекул в этом случае играют некоторые цитокины (фактор некроза опухолей альфа - ФНОα, фактор некроза опухолей бета, он же лимфотоксин - 17 ФНОβ, другие провоспалительные цитокины). Значение этого вида апоптоза, который получил название «инструктивного» весьма велико для нормальной деятельности, прежде всего, иммунной системы (регуляция воспалительного процесса, противоопухолевый иммунитет, защита естественных антигенов, например, семенников или хрусталика глаза от иммуноцитов организма и т.п.). Интересна история открытия цитокина ФНОα. В конце XVIII века врачами было замечено, что у некоторых пациентов исчезали злокачественные опухоли после перенесения ими инфекционного заболевания. В начале ХХ века американский врач W.Coley пытался лечить онкологических больных вводя им препараты, полученные фильтрованием культур граммположительных и грамм-отрицательных бактерий. В некоторых случаях эта терапия приводила к успеху. В дальнейшем, уже в середине ХХ века после открытия липополисахарида - вещества, входящего в состав мембран микробных клеток, было показано, что это вещество способно индуцировать некроз опухолей. Однако в 1975 году благодаря работам L.Old и его коллег стало ясно, что некроз опухолей вызывает не сам липополисахприд, но некий белковый фактор, который вырабатывается макрофагами при их контакте с бактериями. Этот белковый фактор и получил название «фактор некроза опухолей». К концу ХХ века стало ясно, что ФНО вырабатывается не только активированными макрофагами, но и Т-лимфоцитами, нейтрофилами, тучными клетками, астроцитами и клетками – натуральными киллерами (NKклетками). В настоящее время твердо установлено, что ФНО способен индуцировать апоптоз самых различных клеточных структур, в том числе – и опухолевых клеток. Кроме того, являясь провоспалительным цитокином, ФНО способен вызывать и некроз клеток как результат их гибели в очаге воспаления. Важным элементом механизма инструктивного апоптоза являются рецепторы клетки, способные соединяться с указанными цитокинами. Эти рецепторы (белковые макромолекулы) принадлежат к суперсемейству рецепторов фактора некроза опухолей альфа и, в силу их особой функции, получили название «рецепторов смерти» (Death Receptors). Внутрицитоплазматическая часть этих рецепторов получила название «доменов смерти». После соединения с этими рецепторами их лиганд (ФНОα, ФНОβ и других) активированный домен смерти при посредстве сложной ферментной системы (адапторного белка) осуществляет автокаталитический процессинг прокиназ, которые, в свою очередь, активирую киназы, входящие в состав каскада «казнящих киназ». Их ферментативное воздействие и осуществляет апоптоз. Следует иметь в виду, что определенную роль в активации киназного каскада играют ионы Са++, которые проникают в клетку через кальциевые каналы, открытию которых так же способствует активация рецепторов смерти. 18 8. Общая схема патогенеза атеросклероза Из предшествующего материала ясно, что основными звеньями патогенеза атеросклероза являются альтерация сосудистого эндотелия, развивающийся локальный воспалительный процесс, изменение свойств ЛПНП (перекисная модификация ЛПНП), накопление и, в дальнейшем, разрушение пенистых клеток в субэндотелии, формирование атеросклеротической бляшки и ее разрушение. Однако, на предрасположенность к атеросклерозу, интенсивность его развития большую роль играют разнообразные факторы риска, которые принято разделять на неуправляемые факторы риска (наследственность, возраст, пол) и управляемые факторы риска (гипертензия, стресс, гормональные нарушения, нерациональное питание, ожирение, гиподинамия и т.п.). Отрицательное воздействие факторов риска на организм можно проследить на протяжении всех стадий атеросклероза: от долипидной стадии и до стадии атероматозной язвы. Общее представление о патогенезе атеросклероза дает приводимая ниже схема. Общая схема патогенез атеросклероза 9. Принципы патогенетической терапии атеросклероза Терапия атеросклероза является весьма сложной задачей лечащих врачей, во-первых, потому, что об интенсивности развития атеросклеротического процесса можно судить в основном по данным лабораторного исследования крови (степень гиперхолистеринемии и соотношение фракций атерогенных и антиатерогенных липопротеидов), результаты которого далеко не всегда прямо коррелируют со степенью поражения сосудистой стенки. Во-вторых, фармакотерапевтический арсенал современной клиники в плане лечения атеросклероза не слишком широк. В-третьих, терапия этого заболевания затруднена и в связи с его волнообразным течением. Однако некоторые соображения по данному вопросу высказать можно. 19 При легкой степени гиперхолистеринемии (5.2 - 6.5 ммоль/л в плазме крови)2 рекомендуется диета со значительным уменьшением в пище жиров и продуктов, в большом количестве содержащих холестерин. При умеренной гиперхолистеринемии (6.5 - 7.8 ммоль/л) наряду с диетой применяются препараты, снижающие степень липидемии. То же самое рекомендуется и при высоком уровне гиперхолистеринемии (>7.8 ммоль/л). На этой стадии также применяются препараты, ингибирующие внутриорганный синтез холестерина, которые входят в группу статинов, благодаря которым уменьшается образование мевалоновой кислоты – предшественницы холестерина. Кроме того, статины обеспечивают нормализацию функций эндотелия сосудов, обладают противовоспалительными свойствами, тормозят образование пристеночных тромбоцитарных тромбов, способствуют стабилизации атеросклеротических бляшек. Однако, употребляя эти лекарства, человек попадает в пожизненную зависимость от их ежедневного приема, поскольку прекращение ингибиции образования эндогенного холестерина немедленно вызовет его гиперпродукцию и концентрация липопротеидов крови возрастет в несколько раз. Кроме того, для лечения и профилактики прогрессирования атеросклеротического процесса необходимо лечение тех заболеваний, на фоне которых атеросклероз развивается наиболее интенсивно (сахарный диабет, гипофункция щитовидной железы и др.). Следует иметь в виду, что в ряде случаев возможно и применение хирургических методов лечения проявлений атеросклероза в кровеносных сосудах жизненно важных органов (сердце, головной мозг). 10. Исходы атеросклероза Значение атеросклероза в развитии заболеваний сердца и сосудов трудно переоценить. Во-первых, атеросклероз резко повышает чувствительность кровеносных сосудов к спастическим влияниям. Это, по-видимому, связано с тем, что детрит, образующийся в сосудистых стенках, их плазматическое пропитывание могут раздражать заложенные там рецепторные окончания вазоконстрикторов, которые значительно чувствительнее к раздражению, нежели вазодилататоры. Кроме того, поврежденный атеросклерозом эндотелий перестает выделять биологически активные вещества, обеспечивающие в норме вазодилатацию и препятствующие тромбообразованию. Об этом обстоятельстве уже упоминалось в предшествующем материале. Поэтому даже слабые спастические влияния на фоне атеросклероза могут давать сильный прессорный эффект, что учащает и усиливает приступы стенокардии и гипертонические кризы. 2 Концентрации холестерина в крови и некоторые способы терапии атеросклероза даются на основании рекомендаций Европейской ассоциации по атеросклерозу / Национального комитета по обучению в области атеросклероза. 20 Во-вторых, атеросклеротические бляшки, а также диффузные утолщения стенки сосудов сужают просвет последних и нарушают поступление крови к органам, в том числе - к сердечной мышце и мозговой ткани. Атеросклеротическая бляшка может полностью закрыть просвет сосуда и вызвать инфарцирование соответствующего органа. В-третьих, поскольку атеросклеротический процесс повреждает сосудистый эндотелий, он создает основу для возникновения тромбов, так как один из важнейших моментов в процессе тромбообразования - это повреждение интимы. Тромбы в той или иной степени нарушают циркуляцию крови по сосудам, а также могут отрываться и превращаться в эмболы. В-четвертых, на стадии атероматозной язвы детрит, попадая в кровоток, также становится эмболом, который может переноситься кровью и закупоривать мелкие кровеносные сосуды. Особенно опасен этот процесс при изъязвлении атероматозной бляшки, локализованной в коронарных или мозговых артериях, являющихся функционально концевыми. Детрит током крови заносится в более мелкие разветвления этих сосудов, закупоривает их и может вызвать развитие инфаркта миокарда или ишемического инсульта. Возможны исходы и осложнения атеросклероза представлены на нижеследующей схеме. Исходы и осложнения атеросклероза В связи с изложенным, атеросклероз привлекает самое пристальное внимание как клиницистов, так и теоретиков. В решении проблемы атеросклероза лежит ключ к профилактике и лечению многих заболеваний сердечно - сосудистой системы.