(299.7 KБ)
advertisement

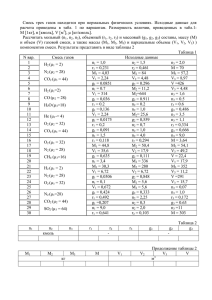
ЛАБОРАТОРНАЯ РАБОТА № 1 «Изучение физико-химических свойств активных атмосферных газов» Основными атмосферными газами являются N2 (78 %) и О2 (21 %). Остальные газы относятся к активным, т. к. изменение их концентрации существенно влияет на качество окружающей среды. Цель работы: изучение органолептических и физико-химических свойств активных атмосферных газов. Опыт 1. Получение газов и способы их обнаружения Порядок выполнения работы 1.1. Для получения заданного газа (табл. 1.1) поместите в пробирку 1 микрошпатель твердого реактива и добавьте к нему 0,5-1,0 мл жидкого реагента. Поднесите к отверстию пробирки полоски индикаторной бумаги и убедитесь, что газ выделяется. Если исследуемый газ тяжелее воздуха, наклоните пробирку под углом примерно 300, чтобы облегчить его выход в атмосферу. Отметьте цвет и запах газа. Пробирку тут же вымойте. Таблица 1.1 Реагенты для получения и обнаружения газов Реагенты для получения газа Ва риант Газ 1 твердый жидкий Н2 Zn в гранулах H2SO4 2 н. 2 Сl2 MnO2 (т) HCl конц. 3 HCl NaCl (крист.) H2SO4 конц. 4 NO2 медная стружка HNO3 конц. 5 CO2 СаСО3 (мел, мрамор) HCl конц. 6 SO2 Na2S2O3 (т) медная стружка H2SO4 конц. 7 H2S FeS2 (пирит) H2SO4 (1:3) 8 O3 KMnO4 (крист.) H2SO4 конц. 9 NH3 NH4Cl (крист.) NaOH конц. H2SO4 2 н. Аналитический эффект обнаружения газа выделение пузырьков газа белая иодидкрахмальная бумажка синеет синий лакмус краснеет буро-коричневый газ, синий лакмус краснеет синий лакмус краснеет синий лакмус краснеет запах, свинцовая бумажка чернеет запах, белая иодидкрахмальная бумажка синеет запах, красный лакмус синеет Продолжение табл. 1.1 10 HF NaF (крист.) 11 HBr KBr (крист.) 12 NO H2SO4 (3:1) или H3РO4 конц. H2SO4 (3:1) или H3РO4 конц. медная стружка HNO3 разб., нагревание синий лакмус краснеет синий лакмус краснеет побурение в присутствии кислорода на выходе из пробирки 1.2. В отчете по лабораторной работе характеристику свойств полученного Вами газа представьте в форме табл. 1.2. При описании свойств газа используйте прил. ** Таблица 1.2 Характеристика физико-химических свойств газа __________ Физические свойства газа Молярная масса Плотность относительно воздуха Цвет Запах Растворимость в воде Время пребывания в атмосфере Уравнение реакции получения газа в лабораторных условиях Источники поступления газа в атмосферу и уравнения протекающих при этом реакций Природные (абиогенные): Природные (биогенные): Техногенные: Опыт 2. Изучение химических свойств активных атмосферных газов К наиболее важным химическим свойствам активных атмосферных газов относят кислотно-основные, окислительно-восстановительные свойства, а также способность к образованию осадков и комплексов. Порядок выполнения работы 2.1. Приготовьте реагенты для изучения химических свойств газов в соответствии с рекомендациями табл. 1.3. Таблица 1.3 Реагенты для изучения химических свойств газов Определяемые свойства Кислотноосновные Окислительновосстановительные Реагент лакмусовая бумажка Способ приготовления реагента Аналитический сигнал смочите водой синяя бумажсинюю и красную ка покраснела лакмусовые бумажки красная бумажка посинела KMnO4 в на часовом стекле сернокислой смешайте среде 1-2 мл 2 н. H2SO4 и раствор KMnO4 до слаборозовой окраски Заключение кислотные свойства основные свойства бумажка восстанообесцветилась вительные свойства бумажка стала слабые буровосстанокоричневой вительные свойства бумажка не не проявизменилась ляет восстановительных свойств синяя йодо- на часовом стекле синяя бумажкрахмальная в 3-4 мл крахмально- ка обесцветибумажка го клейстера добавьте лась одну каплю раствора I2 белая иодидкрахмальная бумажка Обменные, СоСО3 способность к образованию Cu(OH)2 осадков и комплексов сильные восстановительные свойства на часовом стекле белая бумаж- окислив 3-4 мл крахмально- ка посинела тельные го клейстера раствосвойства рите 1/2 микрошпателя сухого KI густая суспензия СоСО3 в воде изменение образовацвета суспен- ние осадка зии или комплекса на часовом стекле изменение смешайте 1-2 мл рас- цвета суспентвора CuSO4 и 1-2 мл зии 2 н. NaOH образование осадка или комплекса 2.2. Полоски сухой фильтровальной бумаги размером 5 х 25 мм пронумеруйте простым карандашом и занесите присвоенные номера в табл. 1.4. Смочите бумажки жидкими и суспендированными реагентами. Закрепите их на внутренней части воронки (рис. 1). В зависимости от молекулярной массы исследуемого газа бумажки крепятся ближе к нижней или к верхней части воронки. Таблица 1.4 Результаты исследования химических свойств активных атмосферных газов № п/п Реагент Наблюдаемый эффект Уравнения реакций, подтверждающие химические свойства газов Вывод Рис. 1. Установка для изучения химических свойств газов 2.3. Соберите установку для получения газа (рис.1). Для этого на дно чашки Петри поместите маленький фарфоровый тигель, заполненный наполовину сухим реагентом, который Вы использовали для получения газа в опыте 1. В сухой реагент вставьте маленькую воронку диаметром 30 мм, в отвод которой на глубину 5-6 мм введен тампон, не слишком плотно свернутый из кусочка поролона, и вдавите почти до дна тигля. В воронку на 2/3 налейте жидкий реагент (табл. 1.1). Накройте тигель большой конической воронкой с закрепленными внутри нее полосками индикаторной бумаги и в течение 15-20 мин наблюдайте за скоростью и характером изменения их цветов. 2.4. После окончания опыта в чашку Петри на 1/2 ее высоты налейте раствор поглотителя и слегка приподнимите край большой воронки, чтобы погло- титель попал внутрь газовой камеры. Для газов кислотного характера в качестве поглотителя используется 1 н. раствор NaOH, а для основного – 1 н. раствор H2SO4. Через 10 мин коническую воронку снимите, установку разберите и вымойте. 2.5. В отчете по лабораторной работе приведите рисунок установки, используемой в опыте. Результаты исследований оформите в виде табл. 1.4. Запишите уравнение взаимодействия изучаемого газа с поглотителем. Задание к самостоятельной работе Используя литературные и справочные данные (прил.**), характеризуйте физико-химические свойства заданного в Вашем варианте газа (табл. 1.5) и представьте их в форме табл. 1.6. Таблица 1.5 Варианты заданий Вариант Газ Вариант 1 2 3 4 5 СО2 СH4 О3 РH3 Сl2 9 10 11 12 13 6 7 8 СH3NH2 Сl2О HBr 14 15 16 Газ HF NH3 SО2 СH2О пероксиацетилнитрат NО2 SО3 СОS Вариант Газ Вариант Газ 17 18 19 20 21 (СH3)2S HО2● OH● CСl2F2 СО 25 26 27 28 29 Rn B2H6 C2H2 CS2 H2Se 22 23 24 N2O NO H2S 30 31 32 AsH3 CHСl3 CСl4 Таблица 1.6 Характеристика физико-химических свойств газа ______ Физические свойства Химические свойства, уравнения реакций, их доказывающие Молярная Плотность Цвет масса Запах Кислотные: Основные: Окислительные: Восстановительные: Склонность к образованию осадков: Склонность к комплексообразованию: Способность к обмену: Время пребывания в атмосфере Физикохимические свойства Растворимость в воде: Растворимость в неполярных растворителях: Сорбция полярными сорбентами: Сорбция неполярными сорбентами: Источники поступления Природные (абиогенные): газа в атмосферу и Природные (биогенные): уравнения протекающих Техногенные: при этом реакций Выводы Сделайте выводы о доминирующих и слабовыраженных свойствах изученных газов. Приведите примеры влияния этих газов на качество окружающей среды.