Новые подходы к созданию фармакологических средств для
advertisement
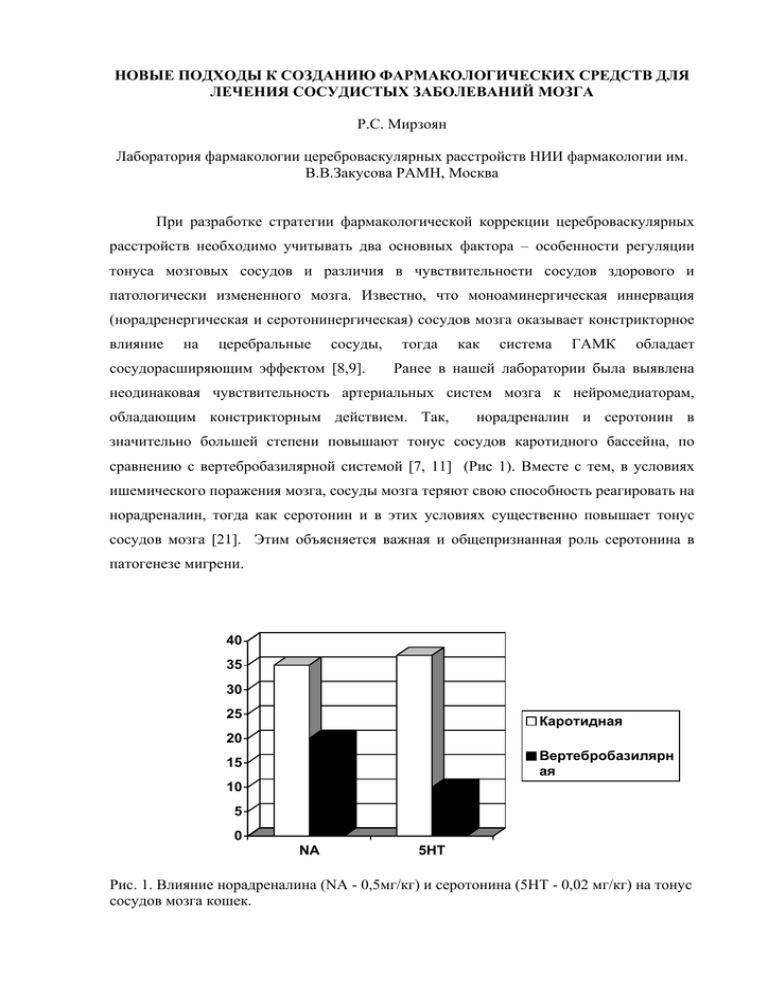
НОВЫЕ ПОДХОДЫ К СОЗДАНИЮ ФАРМАКОЛОГИЧЕСКИХ СРЕДСТВ ДЛЯ ЛЕЧЕНИЯ СОСУДИСТЫХ ЗАБОЛЕВАНИЙ МОЗГА Р.С. Мирзоян Лаборатория фармакологии цереброваскулярных расстройств НИИ фармакологии им. В.В.Закусова РАМН, Москва При разработке стратегии фармакологической коррекции цереброваскулярных расстройств необходимо учитывать два основных фактора – особенности регуляции тонуса мозговых сосудов и различия в чувствительности сосудов здорового и патологически измененного мозга. Известно, что моноаминергическая иннервация (норадренергическая и серотонинергическая) сосудов мозга оказывает констрикторное влияние на церебральные сосуды, сосудорасширяющим эффектом [8,9]. тогда как система ГАМК обладает Ранее в нашей лаборатории была выявлена неодинаковая чувствительность артериальных систем мозга к нейромедиаторам, обладающим констрикторным действием. Так, норадреналин и серотонин в значительно большей степени повышают тонус сосудов каротидного бассейна, по сравнению с вертебробазилярной системой [7, 11] (Рис 1). Вместе с тем, в условиях ишемического поражения мозга, сосуды мозга теряют свою способность реагировать на норадреналин, тогда как серотонин и в этих условиях существенно повышает тонус сосудов мозга [21]. Этим объясняется важная и общепризнанная роль серотонина в патогенезе мигрени. 40 35 30 25 Каротидная 20 Вертебробазилярн ая 15 10 5 0 NA 5HT Рис. 1. Влияние норадреналина (NA - 0,5мг/кг) и серотонина (5HT - 0,02 мг/кг) на тонус сосудов мозга кошек. В связи с этим, цереброваскулярная реакция на серотонин нами была использована для изучения известных противомигреневых препаратов и поиска новых средств для лечения мигрени. Было установлено, что антисеротониновая цереброваскулярная активность характерна для многих препаратов, используемых для лечения больных мигренью – ницерголина, метисергида, пропранолола, толфенамовой кислоты. Изыскание противомигреневых препаратов проводили среди ароматических и гетероароматических эфиров оксима тропинона, синтезированных Л.М.Косточкой. Проведенные опыты позволили выявить антисеротониновую активность у большинства из вновь синтезированных соединений. Наибольшую антисеротониновую активность и наименьшую токсичность среди изученных соединений проявило соединение, являющееся производным оксима тропинона и 3,4,5-триметоксибензойной кислоты, названное в дальнейшем тропоксином (Рис.2.) [2,4,13,25]. При изучении антисеротониновой активности тропоксина у животных было показано, что препарата значительно ослабляет цреброваскулярную реакцию на серотонин. Следует особо подчеркнуть, что на фоне действия тропоксина, в отличие от других противомигреневых препаратов, серотонин не только в меньшей степени уменьшает мозговой кровоток, но и вызывает его увеличение (Рис. 3). В настоящее время препарат проходит клиническое изучение. Предварительные результаты, полученные на кафедре неврологии и нейрохирургии Санкт-Петербургского медицинского университета им. акад. И. П. Павлова в результате двойного слепого, плацебо контролируемого исследования, свидетельствуют о высокой эффективности тропоксина при межприступном лечении больных мигренью [1]. Тропоксин снижает частоту приступов у 73% больных (Рис.2). OCH H 3 CN C N O H C OH 3 OCH OCH 3 3 Рис. 2. Тропоксин - оригинальный противомигреневый препарат 2 40 20 0 % -20 -40 Пропранолол 1мг/кг Ницерголин 200мкг/кг Метисергид 1 мг/кг Тропоксин 10 мг/кг -80 Толфенамовая к-та 5 мг/кг -60 Контроль Препарат Рис. 3. Влияние противомигреневых препаратов на изменения мозгового кровотока, вызванные серотонином. Расстройства мозгового кровообращения занимают одно из ведущих мест среди основных причин смертности и инвалидизации населения большинства стран. В мире регистрируется более 6 млн инсультов ежегодно, в Российской Федерации - более 450 000 случаев. Несмотря на существенные различия в этиологии и патогенезе ишемического и геморрагического инсультов, в обоих случаях, согласно результатам большинства исследователей, отмечается выраженное снижение уровня мозгового кровотока. Цереброваскулярные расстройства характеризуются сложным каскадом нейрохимических процессов в центральной нервной системе и, в первую очередь значительным высвобождением глутамата и других возбуждающих нейромедиаторных аминокислот, которые играют ключевую роль в развитии структурного поражения нервной ткани. Об этом свидетельствует также способность неконкурентного антагониста NMDA-рецепторов МК-801 (дизолципина) оказывать нейропротекторное действие в эксперименте, защищая мозг от ишемического поражения. Исследования этого направления продолжают развиваться, однако они не получило применения в клинической практике из-за тяжелых побочных эффектов антагонистов глутаматных рецепторов. С большим удовольствием хочу отметить, что в СССР на протяжении многих лет, а в последние годы и других странах, успешно разрабатывается другое направление фармакотерапии ишемических поражений мозга, которое связано с 3 системой ГАМК. Речь идет о сосудорасширяющем по отношению к сосудам мозга действии ГАМК. Считаю необходимым представить хронологию исследований, посвященных ГАМК и сосудам мозга: 1964-1967гг. - выявлена способность ГАМК усиливать кровоснабжение мозга, понижая тонус мозговых сосудов [15]. 1969-1974 гг. – в сосудах мозга обнаружена ГАМК, глутамат-декарбоксилаза и ГАМКтрансаминаза [17,18]. 1980 г. – выявлен высокий аффинитет связывания агониста ГАМК-А рецепторов мусцимола с одноименными рецепторами пиальных сосудов [24]. 1978 г.– обнаружено повышение содержания ГАМК в ткани мозга в условиях ишемии [16], эти данные были подтверждены [22, 23]. 1976-1980гг.- выявлено взаимодействие ГАМК с центральными адренергическими механизмами регуляции мозгового кровообращения [8,9]. 1977 – 1989 гг. – разработано оригинальное производное ГАМК - препарат Пикамилон с цереброваскулярный и ноотропной активностью [3, 10]. 60 50 40 30 Интакт. 20 Ишемиз. 10 0 -10 Комбинация Афобазол Пикамилон Конъюгат Рис. 4. Влияние лекарственной комбинации (пирролидон +пироглутаминовая кислота), афобазола, пикамилона и конъюгата ГАМК с докозагексаеноилдофамином на кровоснабжение интактного и ишемизированного мозга крыс. Исследование цереброваскулярной активности ГАМК-миметиков в нашей лаборатории получило дальнейшее развитие. Были исследованы афобазол, разработанный в НИИ фармакологии им.В.В.Закусова РАМН под руководством академика РАМН и НАН РА С.Б.Середенина, лекарственная комбинация, содержащая пирролидон и биоорганической пироглутаминовую химии им. кислоту Шемякина и и синтезированный Овчинникова в коньюгат Институте ГАМК с 4 докозагексаеноилдофамином. ГАМК-ергический механизм цереброваскулярной активности указанных веществ был установлен с помощью специфических блокаторов ГАМК-рецепторов – бикукуллина или пикротоксина [5,20]. При исследовании влияния афобазола на локальный мозговой кровоток у крыс, перенесших глобальную преходящую ишемию головного мозга, было показано, что препарат (5 мг/кг), введенный после ишемии вызывает значительное увеличение локального мозгового кровотока в среднем на 40±9,3%, тогда как у интактных животных увеличение мозгового кровотока под влиянием той же дозы препарата составило 19,4±2,9% (рис.3.) [19, 20]. Лекарственная комбинация, содержащая пирролидон и пироглутаминовую кислоту (по 20 мг/кг каждого компонента), также вызывает значительное улучшение состояния микроциркуляции в коре головного мозга у крыс после глобального преходящего ишемического поражения мозга. Цереброваскулярные эффекты комбинации у крыс в условиях глобальной ишемии выражены в значительно большей степени по сравнению с интактными животными (52,0 ± 12,7% и 27,0 ± 6,5% соответственно р<0,05) (рис.3.) [5, 12]. Проведенное на крысах с использованием коньюгата ГАМК докозагексаеноилдофамином (1 мг/кг, в/в) исследование показало, что с после глобальной преходящей ишемии головного мозга он вызывает усиление локального мозгового кровотока у наркотизированных животных в среднем на 29±3,9% (рис. 3). При этом следует подчеркнуть, что у интактных животных соединение не оказывает влияния на кровоснабжение мозга. Следовательно, проведенные эксперименты показали, что афобазол, лекарственная комбинация, содержащая пирролидон и пироглутаминовую кислоту, и коньюгат ГАМК с докозагексаеноилдофамином вызывают значительно более выраженное увеличение мозгового кровотока у крыс, перенесших глобальную преходящую ишемию головного мозга по сравнению с интактными животными. Следующий этап настоящего исследования был посвящен изучению влияния этих соединений на мозговое кровообращение в условиях геморрагического поражения мозга 5 по А.Н. Макаренко и соавт. [6].. Сразу же после моделирования геморрагического комбинация афобазол нимодипин конъюгат геморрагия d% 40 30 20 10 0 -10 0 5 10 15 20 25 30 40 t мин 90 60 -20 -30 -40 Рис. 5. Сводные данные о влиянии геморрагического поражения мозга, лекарственной комбинации, конъюгата ГАМК с докозагексаеноилдофамином и нимодипина на изменения локального кровотока (в %) в контралатеральном полушарии коры головного мозга крыс через 30 минут после «геморрагического инсульта». инсульта уровень локального мозгового кровотока начинал снижаться, а через 30 минут это снижение составило в среднем 30±6,6% к исходному уровню. Затем в течение всего эксперимента уровень кровотока продолжал оставаться сниженным. Изучение влияния афобазола на мозговое кровообращение в условиях модели геморрагического инсульта позволило выявить способность препарата значительно усиливать кровоснабжение пораженного головного мозга. Эксперименты с использованием лекарственной комбинации, содержащей пирролидон и пироглутаминовую кислоту (по 20 мг/кг каждого из компонентов), в этих условиях показали, что сразу же после введения комбинации в большинстве опытов наблюдается минутам достигает использованием максимальных коньюгата ГАМК увеличение мозгового кровотока, которое к 10-15 величин с и составляет 30±8,9%. докозагексаеноилдофамином Опыты показали, с что соединение при внутривенном введении в дозе 1мг/кг в большинстве опытов также вызывает увеличение локального мозгового кровотока у крыс, перенесших 6 геморрагическое поражение головного мозга. Увеличение кровотока в среднем составляет 27±7,6%. Таким образом, исследованные агонисты ГАМК оказывают выраженное влияние на кровоснабжение мозга как в условиях ишемического, так и геморрагического поражения мозга. Характерно, что цереброваскулярный эффект изученных веществ наиболее выражен в условиях экспериментальной патологии мозга. Можно полагать, что эта особенность действия исследованных веществ обусловлена их воздействием на ГАМК рецепторы сосудов мозга. Следующий этап исследований был посвящен экспериментальной кардионеврологии. Сочетанные нарушения кровоснабжения двух важнейших органов мозга и сердца нередкое явление в клинической практике. Вместе с тем, в экспериментальной фармакологии принято раздельное изучение состояний мозгового и коронарного кровообращения под влиянием известных и вновь синтезированных веществ. В доступной нам литературе мы не обнаружили экспериментальных данных о влиянии фармакологических веществ на кровоснабжение мозга, как при нарушениях коронарного кровообращения, так и при сочетанных нарушениях мозгового и коронарного кровообращения. Поэтому исследование было начато с известного цереброваскулярного препарата блокатора кальциевых каналов нимодипина, которое проводилось по следующему протоколу: 1.Изучение влияния нимодипина на локальный мозговой кровоток у интактных животных. 2. Изучение влияния препарата на локальный мозговой кровоток у животных, перенесших глобальную преходящую ишемию головного мозга. 3. Изучение влияния препарата на локальный мозговой кровоток у животных после геморрагического поражения головного мозга. 4. Изучение влияния нимодипина на локальный мозговой кровоток у животных через 3 суток после перевязки левой коронарной артерии. 5. Изучение влияния препарата на локальный мозговой кровоток у ложнооперированных животных. 6. Изучение влияния нимодипина на локальный мозговой кровоток у животных при сочетанных нарушениях коронарного и мозгового кровообращения, у которых через 3 суток после перевязки левой коронарной артерии вызывали глобальную преходящую ишемию головного мозга. 7 7. Изучение влияния препарата на ложнооперированных животных после локальный мозговой кровоток у глобальной преходящей ишемии головного мозга. Проведенные опыты позволили установить, что нимодипин в дозе 0,03 мг/кг при внутривенном введении оказывает существенное влияние на локальный мозговой кровоток в коре головного мозга крыс. Препарат в большинстве опытов вызывает усиление кровотока в коре в среднем на 38±5,0% (рис.7.). Цереброваскулярная 50 40 30 20 10 0 -10 -20 Иш.мозга Иш.миок. Сочет.иш. Рис. 6. Влияние нимодипина (0,03 мг/кг) на локальный мозговой кровоток у крыс в условиях глобальной преходящей ишемии головного мозга [Иш. мозга], окклюзии левой коронарной артерии [Иш.миок.] и сочетанных нарушений кровоснабжения сердца и мозга [Сочет.иш.] (черные столбцы) по сравнению с интактными и ложнооперированными животными. активность нимодипина не претерпевает существенных изменений в условиях ишемического поражения мозга, тогда как эффект препарата существенно ослабляется в условиях экспериментального инфаркта миокарда, а при сочетанной кардиоцеребральной патологии препарат не оказывает влияния на мозговое кровообращение. [14]. Таким образом, проведенное исследование позволяет предложить новую методологию изыскания и изучения лекарственных средств лечения больных как с цереброваскулярными расстройствами, так и с сочетанными нарушениями кровоснабжения мозга и сердца. 8 ЛИТЕРАТУРА 1. Амелин А.В., Игнатов Ю.Д., Скоромец А.А. Мигрень (патогенез, клиника и лечение) // Санкт-Петербургское мед. из-во - 2001. 2. Ганьшина Т.С. Разработка методологии поиска новых противомигреневых средств. Создание оригинального препарата – тропоксин . Автореферат дисс. докт. биол. наук. Москва - 2004. 3. Закусов В.В. и соавт. Вазоактивное и ноотропное средство «пикамилон». // Авторское свидетельство №1393428 от 8 января 1988 // Бюлл. Изобретения –1988. №17. 4. Косточка Л.М., Ганьшина Т.С., Волобуева Т.И., Мирзоян Р.С. и соавт. Соли ароматических и гетероароматических эфиров оксима тропинона, обладающие антисеротониновыми свойствами и противомигреневым действием. // Патент РФ № 1832683 от 24 января 1994 г. Бюлл. «Изобретения» №17, 1996. Приоритет 13 июля 1989. 5. Луньшина Е.В., Ганьшина Т.С., Макарова Л.М., Погорелый В.Е., Мирзоян Р.С. Нейропротекторные свойства пироглутаминовой кислоты в сочетании с пирролидоном.//Экспериментальная и клиническая фармакология. – 2003. – т. 66. №1 – стр. 20-22. 6. Макаренко А.Н, Косицын Н.С., Карпенко С.В., Мишина В.А. // Авторское свидетельство № 1767518 от 03.11.1990. 7. Мирзоян Р.С., О неодинаковой чувствительности артериальных систем мозга к норадреналину //Бюлл. экспер. биол. и мед.,1976, т.81, №1, стр.47-49. 8. Мирзоян Р.С. Пути фармакологической регуляции мозгового кровообращения // Эксперим. и клин. фармакол. – 1995. – Т. 58. - №4. – стр. 3-7. 9. Мирзоян Р.С. Нейропротекторные и цереброваскулярные эффекты ГАМКмиметиков. // Эксперим. и клин. фармакол. – 2003. - Т.66. - №2. – стр. 53-56. 10. Мирзоян Р.С., Ганьшина Т.С. Новый цереброваскулярный препарат пикамилон // Фармакол. и токсикол. – 1989 - т.52 - №1 - с.23-26. 11. Мирзоян Р.С., Н.А.Романычев а Т.С.Ганьшина В.В.Александрин Т.И.Волобуева П.Н.Александров Неодинаковая чувствительность сосудов мозга к серотонину //Экспер. и клин. фармакол.,1993,т.56, №3, стр.22-25. 12. Мирзоян Р.С., Середенин С.Б., Акопян В.П. и др. Лекарственная композиция. Патент на изобретение № 2213562 РФ, 10 октября 2003 г. приоритет от 14.03.2001. 13. Мирзоян Р.С., Середенин С.Б., Ганьшина Т.С., Косточка Л.М., Романычева Н.А., Русаков Д.Ю. Тропоксин - новый антагонист серотонина и потенциальное противомигреневое средство. // Экспер. и клин. фармакол. – 1998 - т.61- №2с.28-31. 14. Мирзоян Р.С., Хайлов Н.А., Цорин И.Б., Ганьшина Т.С. Нимодипин и сочетанные нарушения мозгового и коронарного кровообращения в эксперимента //Экспер. и клин. фармакол., 2009, т.72, №2, с.24-28. 15. Мирзоян С.А., Акопян В.П. Влияние γ-аминомаслянной кислоты на мозговое кровообращение и кислородное напряжение в мозге. //Фармакол. и токсикол. – 1967 - №5 – с. 572-573. 16.Мирзоян С.А., Акопян В.П. Система ГАМК как фактор, способствующий возникновению компенсации нарушенной мозговой гемодинамики. // Бюлл. экспер. биол. и мед. – 1978 - т.85 - №1 – с. 45-48. 9 17. Мирзоян С.А., Казарян Б.А., Акопян В.П. Декарбоксилазная активность глутаминовой кислоты в сосудах мозга. // Доклады АН СССР – 1970. – Т. 190. № 5. – стр. 1241-1243. 18. Мирзоян С.А., Казарян Б.А., Акопян В.П. Содержание и некоторые превращения аминокислот в тканях стенок артерий мозга. // Доклады АН СССР – 1974. - Т. 214. - № 2. – стр. 465-468. 19. Силкина И.В.,. Александрин В.В, Ганьшина Т.С., Середенин С.Б., Мирзоян Р.С. Усиление кровоснабжения ишемизированного мозга под влиянием афобазола.// Экспериментальная и клиническая фармакология. – 2004. – т. 67. - №5 – стр. 913. 20. Силкина И.В., Ганьшина Т.С., Середенин С.Б., Мирзоян Р.С. ГАМК-ергический механизм цереброваскулярного и нейропротекторного эффектов афобазола и пикамилона.// Экспериментальная и клиническая фармакология. – 2005. – т. 68. №1 – стр. 20-24. 21. Топчян А.В. Фармакологическая коррекция кровоснабжения и функционального состояния мозга при его локальном ишемическом поражении.// Дисс. докт. мед. наук. Москва - 1998. 22. Baldwin H.A.; Jones J.A.; Cross A.J.; Green A.R. Histological biochemical and behavioural evidence for the neuroprotective actions of chlormethiazole following prolonged carotid arteryocclusion. Neurodegeneration – 1993- v.2- p. 139–146. 23. Green A.R., Hainsworth A. H. and Jackson D. M. GABA potentiation: a logical pharmacological approach for the treatment of acute ischaemic stroke. // Neuropharmacol. - 2000 - v.39 - p.1483-1494. 24. Krause D.N., Wong E., Degener P., Roberts E. GABA receptors in bovine cerebral blood vessels: binding studies with [3H]muscimol. // Brain Res. - 1980 - v. 185. - p. 51-57. 25. Mirzoyan . R.S., Ganshina T.S., Kostochka L.M., Kozhechkin S.N., Topchyan A.V. Tropoxin- novel 5HT2 receptor antagonist as a promising drug for migraine treatment. Abstracts 2nd European congress of Pharmacology, Budapest, Hungary - 1999 - v.13 Suppl.1 - p.279s Elsevier. 10 НОВЫЕ ПОДХОДЫ К СОЗДАНИЮ ФАРМАКОЛОГИЧЕСКИХ СРЕДСТВ ДЛЯ ЛЕЧЕНИЯ СОСУДИСТЫХ ЗАБОЛЕВАНИЙ МОЗГА Р.С. Мирзоян Лаборатория фармакологии цереброваскулярных расстройств НИИ фармакологии им. В.В.Закусова РАМН, Москва Р Е ЗЮ М Е Установленные нами ранее неодинаковая чувствительность артериальных систем мозга к норадреналину и серотонину, а также различия в действии указанных нейромедиаторов в условиях ишемического поражения мозга, послужили основанием для разработки нового антагониста серотонина и противомигреневого препарата тропоксин. Способность ГАМК-миметиков – афобазола, лекарственной комбинации, содержащей пирролидон и докозагексаеноилдофамином пироглутаминовую оказывать более кислоту, выраженное коньюгата ГАМК с сосудорасширяющее действие в условиях ишемического и геморрагического поражения мозга, а также особенность цереброваскулярного эффекта нимодипина с условиях сочетанной сосудистой патологии мозга и сердца, указывают на необходимость нового подхода для изыскания и изучения средств для лечения больных с цереброваскулярными и кардионеврологическими расстройствами. Ключевые слова: фармакология мозгового кровообращения, инсульты, мигрень, антагонисты серотонина, ГАМК-миметики. Мирзоян Рубен Симонович, E-mail: cerebropharm@mail.ru, тел. (495) 601-24-19, факс - 601-24-19, 125315 Москва, Балтийская ул.д.8, НИИ фармакологии им.В.В.Закусова РАМН. 11